
- •В.Н. Захарченко Курс физической химии Москва
- •Часть 2. Электрохимические системы и электрохимические процессы
- •Глава 1. Термодинамика гальванического элемента
- •1.1.Гальванический элемент
- •1.2.Термодинамика гальванического элемента
- •1.3.Электродный потенциал. Электродные реакции
- •Глава 2.Основные типы электродов
- •2.1.Классификация электродов
- •2.2.Электроды 1-го рода
- •2.3.Электроды 2-го рода
- •2.4.Окислительно-восстановительные электроды
- •2.5.Газовые электроды
- •2.6.Ионоселективные электроды
- •Глава 3.Ионы в растворах электролитов
- •3.1.Классическая теория электролитической диссоциации
- •3.2.Взаимодействие растворяемого вещества с растворителем
- •3.3.Межионное взаимодействие в растворах
- •Глава 4.Термодинамика растворов электролитов
- •4.1.Формальные представления об активности ионов в растворах электролитов
- •4.2.Экспериментальные данные по коэффициентам активности
- •Глава 5.Явления переноса в растворах электролитов
- •5.1.Диффузия в растворах электролитов
- •5.2.Диффузионный потенциал
- •5.3.Электрическая проводимость растворов электролитов
- •Глава 6.Электрохимическая поляризация
- •6.1.Эдс поляризации и электродная поляризация
- •6.2.Теории электродной поляризации
- •Аллотропические цепи
- •Концентрационные цепи
- •7.3.Химические электрохимические цепи
- •Простые химические цепи
- •Сложные химические цепи
- •Глава 8.Химические источники тока
- •8.1.Эталонные гальванические элементы
- •8.2.Первичные гальванические элементы
- •Элемент Лекланше
- •Ртутнооксидный элемент
- •Индийсодержащие элементы
- •Элементы с твердыми электролитами
- •Резервные элементы
- •8.3.Вторичные гальванические элементы
- •Свинцовый аккумулятор
- •Щелочной аккумулятор
- •Серебряный аккумулятор
- •Часть 3. Химическая кинетика и катализ
- •Глава 9.Формальная кинетика
- •9.1.Основные понятия
- •9.2.Классификация химических реакций по их кинетике
- •9.3.Необратимая реакция первого порядка
- •9.4.Необратимая реакция второго порядка
- •9.5.Два случая бимолекулярной реакции
- •2A Продукты реакции,
- •9.6.Необратимая реакция n-ого порядка
- •9.7.Методы определения порядка реакции
- •Дифференцирование кинетической кривой
- •Глава 10.Кинетика сложных реакций
- •10.1.Параллельные реакции
- •10.2.Обратимая реакция
- •Последовательные реакции
- •Глава 11.Влияние температуры на скорость химических реакций
- •11.1.Эмпирические закономерности влияния температуры на скорость реакций
- •11.2.Уравнение Аррениуса
- •Глава 12.Элементарные акты химических превращений
- •12.1.Теория активных столкновений
- •12.2.Механизм мономолекулярных реакций по теории активных столкновений (схема Линдемана)
- •12.3.Теория переходного состояния (теория активного комплекса)
- •Глава 13.Химическая индукция
- •Глава 14.Фотохимические процессы
- •14.1.Основные законы фотохимии
- •14.2.Механизм фотохимических реакций
- •Глава 15.Цепные реакции
- •15.1.Общие сведения о цепных реакциях
- •15.2.Зарождение цепи и методы обнаружения свободных радикалов
- •15.3.Развитие и обрыв цепи
- •Глава 16.Катализ
- •16.1.Общие сведения
- •16.2.Гомогенный катализ
- •16.3.Кислотно-основной катализ
- •16.4.Ферментативный катализ
- •16.5.Гетерогенный катализ
- •Предметный указатель
- •Оглавление
- •Часть 3. Химическая кинетика и катализ 78
- •Глава 9. Формальная кинетика 79
16.4.Ферментативный катализ
Первые количественные результаты по кинетике ферментативных реакций были получены в начале ХХ в. В 1913 г. для их объяснения Л. Михаэлис предложил схему превращений с образованием промежуточных соединений в результате создания полноценной связи между субстратом S и ферментом, или энзимом E , действующим на этот субстрат.
Разработанная теория получила название главновалентной. Она предполагает, что фермент с субстратом могут образовывать комплекс, который способен распадаться как с образованием продуктов реакции, так и с образованием исходного вещества. Схема превращений может быть записана следующим образом:
k1 k2
S + E ES E + P,
k−1
где ES - комплекс, образуемый ферментом и субстратом.
Обозначив концентрации всех веществ, приведенных в схеме, через [S], [E] и [ES], запишем уравнение для скорости накопления фермент-субстратного комплекса:
![]() .
(16 - 2)
.
(16 - 2)
концентрация
несвязанного
фермента
При записи уравнения (16 - 2) специально отмечено, что в реакции с субстратом участвует только та часть фермента, которая не связана с субстратом в комплексе.
Начало
ферментативной реакции сопровождается
очень быстрым ростом концентрации
фермент-субстратного комплекса, а затем
после достижения максимума его
концентрация медленно падает. Таким
образом, по сравнению с начальной частью
кинетической кривой после достижения
максимума можно принять производную
концентрации фермент-субстратного
комплекса по времени очень малой, то
есть
![]() .
Подобный случай накопления промежуточного
соединения уже рассматривался при
объяснении первого порядка реакции по
схеме Линдемана. Состояние после
достижения максимума на кинетической
кривой промежуточного соединения
называется квазистационарным
состоянием.
Используя
условие квазистационарного состояния,
запишем:
.
Подобный случай накопления промежуточного
соединения уже рассматривался при
объяснении первого порядка реакции по
схеме Линдемана. Состояние после
достижения максимума на кинетической
кривой промежуточного соединения
называется квазистационарным
состоянием.
Используя
условие квазистационарного состояния,
запишем:
![]() .
(16 - 3)
.
(16 - 3)
В условиях квазистационарного состояния концентрация фермент-субстратного комплекса равна:
![]() .
(16 - 4)
.
(16 - 4)
Принимая, что скорость реакции в целом определяется скоростью образования продукта реакции по второй стадии:
![]() ,
(16 - 5)
,
(16 - 5)
получим зависимость скорости реакции от концентраций фермента и субстрата:
![]() .
(16 - 6)
.
(16 - 6)
Число констант в уравнении (16 - 6) можно уменьшить, введя новую величину
![]() .
(16 - 7)
.
(16 - 7)
Величина KM называется константой Михаэлиса. Константа Михаэлиса является индивидуальной характеристикой фермента. Ее размерность совпадает с размерностью концентрации. Значения константы Михаэлиса находятся в очень широких пределах и могут составлять от десятка до сотых долей ммоль/л.
С введением константы Михаэлиса уравнение (16 - 6) принимает более простой вид:
![]() .
(16 - 8)
.
(16 - 8)
Уравнению (16 - 8) можно придать другую форму, для чего рассмотрим условие: [S] >> KM. В этом случае скорость реакции достигает максимального значения Wmax.
![]() (16
- 9)
(16
- 9)
и перестает зависеть от концентрации субстрата. Следовательно, этому условию отвечает реакция нулевого порядка по субстрату.
Рис.
16 - 2.
Зависимость скорости ферментативной
реакции от концентрации субстрата.
![]() .
(16 - 10)
.
(16 - 10)
Уравнение (16 - 10) называется уравнением Михаэлиса - Ментен.
Зависимость скорости ферментативной реакции от концентрации субстрата показана на рис. 16 - 2.
Для нахождения максимальной скорости ферментативной реакции и константы Михаэлиса уравнение Михаэлиса - Ментен преобразуют следующим образом:
Рис.
16 - 3.
Графическое определение констант
уравнения Михаэлиса ‑ Ментен.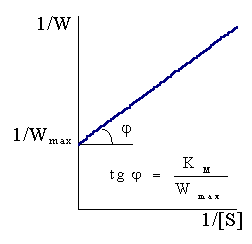
![]() .
(16 - 11)
.
(16 - 11)
Графические методы определения констант уравнения Михаэлиса - Ментен показаны на рис. 16 ‑ 3.
Ферменты являются наиболее специфическими и активными катализаторами из всех известных.
Влияние различных факторов (рН, солей и других веществ, температуры) на активность ферментов изучается в курсе биохимии.
