
- •Физико-химические свойства природных газов и конденсата ч. 1. Параметры природных газов. Определение типа залежи
- •1.1.3. Содержание тяжелых углеводородов в газе.
- •1.1.1. Газовые законы
- •1.1.2. Параметры газовых смесей
- •1.1.4. Критические и приведённые термодинамические параметры
- •1.1.2. Определение типа залежи
- •1.1.2.1. По составу углеводородов
- •1.1.2.2. Метод Коротаева, Карпова
- •1.3. Состав природных газов , добываемых из конкретных месторождений
- •1.4. Физико-термодинамические свойства
- •1.5. Физико-термодинамические свойства
- •1.6. Единицы измерения
- •1.7. Пример расчета
- •3. Многопараметрические зависимости
- •2.2. Методы определения
- •2.2. Расчет плотности природного газа и насыщенного конденсата
- •2.2.1. Графо-аналитический метод Катца и Стендинга
- •2.2.2. Корреляционная зависимость приведённой плотности пр от среднекритического коэффициента сверхсжимаемости zск.
- •2.3. Пример
- •Контрольные задания
- •3.1. Вязкость
- •3.2. Теплоёмкость
- •3.3. Дросселирование газа. Коэффициент Джоуля-Томсона
- •3.4. Теплопроводность газов
- •3.5. Таблицы термофизических свойств
1.6. Единицы измерения
Параметры |
Единицы измерения |
|||
|
СИ |
СГС |
Смешанная |
|
Газовая постоянная R |
Дж/кг К |
эрг/г К=10-4 Дж/кг К |
м/оС=9,81 Дж/кг К |
|
Температура |
К=273 + оС |
К |
оС |
|
Сила |
ньютон(н)= кг*м/с2= 105дн=0,1013кгс |
дина(дн)=г*м/с2= 105н |
кгс=9,81н |
|
Давление |
паскаль(Па)=н/м2 = 10дин(1МПа=106Па) |
дин/см2=0,1Па |
ата=кгс/см2= 9,81*104Па 0,1МПа |
|
Энергия |
Дж=кг м2/с2 |
эрг=г см2/с2= 10-7Дж |
кал=4,1868Дж |
|
1.7. Пример расчета
По данному массовому составу газа, величине пластового давления pпл определить:
-содержание в нем пропана, бутана и газового бензина;
- параметры смеси;
- критические и парциальные параметры;
-вид залежи.
Месторождение |
массовая концентрация, % |
|
||||||||
|
СН4 |
С2Н6 |
С3Н8 |
i C4Н10 |
n C4Н10 |
С5Н12 +выс. |
N2+ инерт |
СО2 |
Тпл К |
р Мпа |
1 пример |
19,5 |
11,8 |
37,95 |
3,25 |
12,05 |
8,15 |
7,3 |
-- |
353 |
23,0 |
Решение
1. Определяем среднюю молекулярную массу газа по (1.8)
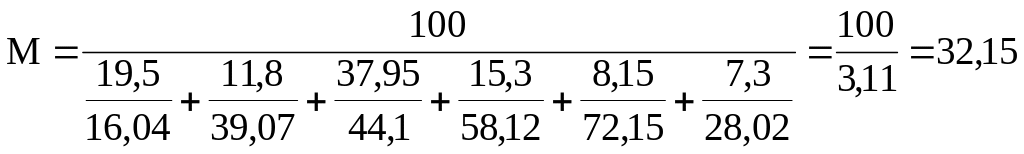
2. Находим плотность газа при нормальных условиях по (1.3)
см=32,15/22,41=1,43 кг/м3
3. Находим содержание тяжёлых углеводородов в газе по (1.10) в г/м3
пропана..............................10 . 37,95.1,43=542,0;
i - бутана.............................10 . 3,25.1,43= 46,5;
n -бутана.............................10 . 12,05.1,43=172,0;
пентана и высших...............10 . 8,15.1,43=117,0;
__________________________________________________________
Всего..............................................................877,5 г/м3
Т.о., газового бензина (пентан целиком) и n-бутана (по величине, равной половине пентана) в составе газа будет
117+117/2=175,5 г/м3;
пропана.............................. 542,0 г/м3;
i - бутана............................. 46,5 г/м3;
n -бутана............................. 172-58,5=113,5 г/м3.
Всего тяжелых углеводородов 877,5 г/м3.
Находим относительную плотность газа по (1.4.2)
0=1,43/1,293=1,106.
6. Определяем объёмные концентрации yi компонент по (1.5), парциальные давления pi по(1.6):
Компоненты |
СН4 |
С2Н6 |
С3Н8 |
i C4Н10 |
n C4Н10 |
С5Н12 +выс. |
N2+ инерт |
Пласт. давл. Р, МПа |
Мол. масса смеси,М |
Массов. конц.%, gi |
19,5 |
11,8 |
37,95 |
3,25 |
12,05 |
8,15 |
7,3 |
23,0 |
32,15 |
Молек. масса, Мi |
16,04 |
39,07 |
44,1 |
58,12 |
58,12 |
72,15 |
28,02 |
-- |
|
Объёмные конц.% yi=gi M/ Mi |
39,09 |
9,71 |
29,12 |
1,8 |
6,67 |
3,63 |
8,38 |
-- |
|
Парциал. давл. Рi=yip/100, МПа |
8,99 |
2,23 |
6,7 |
0,41 |
1,53 |
0,83 |
1,93 |
-- |
|
7. Определим тип залежи:
а) Имеем - =1,106; метана-39,09%; жидкого газа (пропан-бутановая фракция) - 31%, газ. Бензина 8%. Т.о. по разделу (3.1) месторождение можно считать газонефтяным.
в) по Коратаеву - g=0,27. Газ можно отнести к газонефтяному.
8. Найдем объём паров после испарения 702 кг пропан -бутановой фракции, в которой содержится: пропана - 542 кг, бутана - 160кг.
Находим процентное содержание пропана и бутана в данной фракции:
пропан - g = 542.100 / 702=77,2%;
бутан - g= 100-77,2= 22,8%.
Определим среднюю молекулярную массу смеси
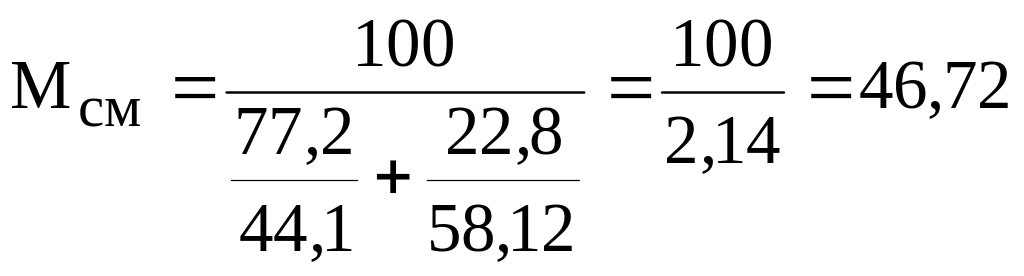
Объём паров (11)
Vп= 22,41.702 / 46,72=336,7 м3.
Найдём критические и приведенные параметры смеси:
Компоненты |
СН4 |
С2Н6 |
С3Н8 |
i C4Н10 |
n C4Н10 |
С5Н12 +выс.
|
N2+ инерт |
Отн. плотн. , кг/м3 |
Мол. масса смеси, М |
Молек. масса, Мi |
16,04 |
39,07 |
44,1 |
58,12 |
58,12 |
72,15 |
28,02 |
1,106 |
32,15 |
Объём. конц. yi |
0,391 |
0,0971 |
0,2912 |
0,018 |
0,0667 |
0,0363 |
0,0838 |
-- |
|
Крит. темп., К |
190,5 |
206 |
369,6 |
404 |
420 |
470,2 |
125,9 |
-- |
|
Крит. давл., МПа |
4,7 |
4,9 |
4,3 |
3,7 |
3,8 |
3,4 |
3,46 |
-- |
|
Т.к. объёмное содержание высококипящих и неуглеводородных компонент больше 10%, то для расчета критических параметров используем зависимости (1.12.1)
К= 128.46; К2= 16502,85; J=106,79; J2=11404,1041;
ркр=1,45 МПа; Ткр=154,5 К.
Рассчитаем критические параметры по (12):
ркр=4,3 МПа; Ткр=266,5 К.
Рассчитаем критические параметры по (14.1):
ркр=4,44 МПа; Ткр=262,3 К.
1.8. Проверочные задания
По данному составу газа, величине пластового давления pплопределить:
-содержание в нем пропана, бутана и газового бензина;
- параметры смеси;
- критические и парциальные параметры;
-вид залежи.
Состав газа взять из таблицы раздела (1.4).
2.1. Уравнения состояния природных газов
1. Уравнение состояния совершенного газа Клайперона-Менделеева
р= R T, (2.1)
где R - газовая постоянная (Дж/(кг К)).
2. Обобщённое уравнение состояния
р=z R T . (2.2)
Коэффициент сверхсжимаемости z является функцией приведенных значений давления рпр, температуры Тпр и для тяжелых углеводородов С5+ - ацентрического фактора , учитывающего нецентричность сил притяжения. Т.о. z=z(pпр,Tпр, ). Для смесей газов = (yii), а i изменяется в пределах от 0 до 0,4 и значение его можно определить из таблиц (часть1).
Значение z находят или по соответствующим таблицам, или графически, или по эмпирическим зависимостям, или на основе многопараметрических уравнений состояния. При этом необходимо вводить поправку на содержание азота N 2 z=yN zN+(1-yN) zу. Здесь zy - коэффициент сверхсжимаемости углеводородной части.
