
Реферат - Газы, изопроцессы, газовые формулы
.docГАЗЫ
Условные обозначения:
|
p |
Давление |
|
V |
Объем |
|
T |
Температура |
|
n |
Концентрация |
|
NА |
Постоянная Авогадро |
|
m |
Масса газа |
|
M |
Молярная масса |
|
R |
Универсальная газовая постоянная |
Формулы:
|
n= |
Концентрация газа |
|
pV= |
[Подставить kNA] |
|
pV= |
Уравнение состояния для произвольной массы идеального газа (уравнение Менделеева – Клапейрона) |
|
|
Уравнение для газа данной массы |
Газовые законы:
Изотермический процесс. Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называдт изотермическим.
pV=const при Т=const (закон Бойля – Мариотта)
Д

 ля
газа данной массы произведение давления
газа на его объем постоянно, если
температура газа не меняется.
ля
газа данной массы произведение давления
газа на его объем постоянно, если
температура газа не меняется.
Изобарный процесс. Процесс изменения отношения состояния термодинамической системы при постоянном давлении называют изобарным.
![]() =const
при p=const
(закон Гей-Люссака)
=const
при p=const
(закон Гей-Люссака)
Для данной массы отношение объема к температуре постоянно, если давление газа не меняется.
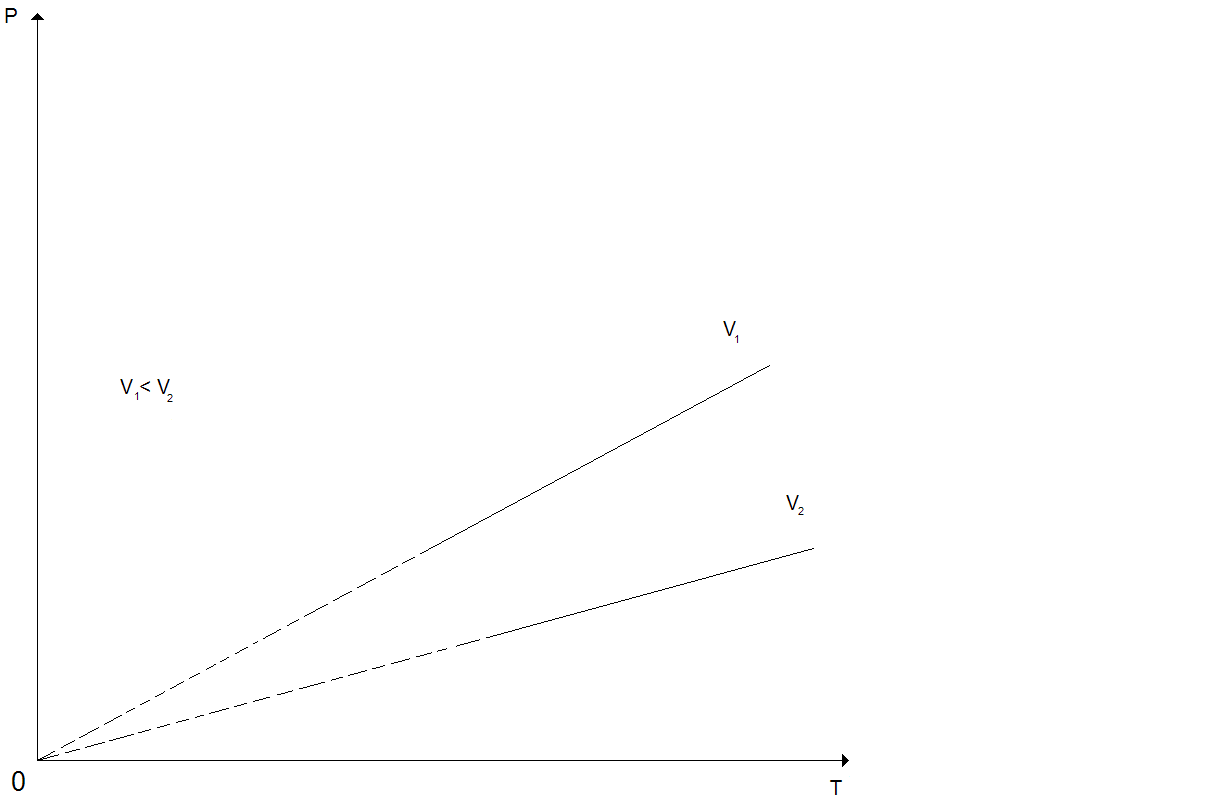
Изохорный процесс. Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным.
![]() =const
при V=const
(закон Шарля)
=const
при V=const
(закон Шарля)
Для газа данной массы отношение давления к температуре постоянно, если объем не меняется.
