Otvety_na_ekzamen_voprosy_po_Patofiziologii
.doc
|
№ 76 Принципы выявления, терапии и профилактики аллергии. Десенсибилизация (гипосенсибилизация) организма: виды, методы, возможные механизмы десенсибилизации.
Как и при большинстве болезней, лечение и профилактика аллергических реакций основана на реализации этиотропного, патогенетического, саногенетического и симптоматического принципов. Этиотропная терапия и профилактика. Этиотропная терапия направлена на устранение аллергена из организма, а профилактика — на предотвращение контакта организма с аллергеном. • При этиотропной терапии проводятся мероприятия по удалению из организма микробов, паразитов, грибов, простейших (санация) и выведению из организма аномальных белков и других аллергических соединений. • При этиотропной профилактике принимают меры по недопущению попадания в организм аллергенов: пыльцы, пыли, компонентов шерсти животных, органических и неорганических веществ, ЛС и прочих аллергенов. Патогенетическая терапия. Патогенетическая терапия направлена на разрыв основных звеньев патогенеза аллергии, а профилактика — на опережающую блокаду потенциальных механизмов её развития. Эти мероприятия называют гипо- или десенсибилизацией организма, поскольку они имеют целью блокаду иммуногенных сенсибилизирующих процессов, направлены на предотвращение образования и нейтрализацию медиаторов аллергии. С этой целью проводят специфическую и/или неспецифическую гипосенсибилизацию. • Специфическая гипосенсибилизация достигается путём парентерального введения (как правило, по определённым схемам) того аллергена, который предположительно вызвал сенсибилизацию (метод рассчитан на: образование комплекса аллергена с AT и снижение содержания соответствующих Ig). • Неспецифическая гипосенсибилизация применяется в тех случаях, когда специфическая по каким-либо причинам невозможна или неэффективна, либо когда не удаётся выявить аллерген. Её можно достичь применением некоторых Л С (например, антигистаминных и мембраноста-билизирующих) при аллергии немедленного типа; иммунодепрессантов (в том числе глюкокортикоидов) и иммуномодуляторов — при аллергии замедленного типа, а также используя некоторые виды физиотерапевтических воздействий. Саногенетическая терапия. Саногенетические воздействия направлены на активацию защитных, компенсаторных, репаративных, замещающих и других адаптивных процессов и реакций в тканях, органах и организме в целом. С этой целью применяют витамины, адаптогены (женьшень, элеутерококк), проводят немедикаментозные мероприятия: закаливание, физические нагрузки, лечебное голодание и другие. Симптоматическая терапия. Симптоматические средства используют для предотвращения или устранения неприятных, тягостных ощущений, усугубляющих течение аллергии: головной боли, головокружения, чувства тревоги, напряжения, подавленности и т.п. С этой целью применяют транквилизаторы, обезболивающие препараты, психоаналептики, проводят физиотерапевтические процедуры. |
№ 77 Болезни и состояния иммунной аутоагрессии: этиология, патогенез, проявления.
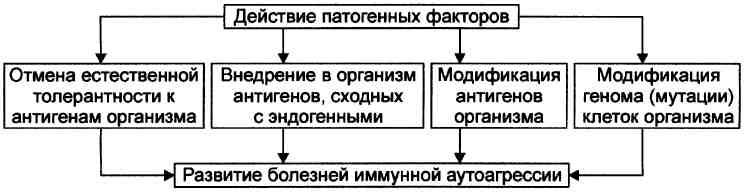
Состояния и болезни иммунной аутоагрессии — нарушения жизнедеятельности организма, вызванные развитием патогенных иммунных реакций, направленных против Аг собственных клеток и неклеточных структур. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ К наиболее вероятным и аргументированным механизмам происхождения болезней иммунной аутоагрессии относят заболевания, обусловленные изменениями в системе ИБН (иммунозависимые болезни) и вызванные изменениями вне системы ИБН (иммунонезависимые болезни). Иммунозависимые болезни иммунной аутоагрессии В основе возникновения и развития иммунозависимых, но антигеннезависимых болезней иммунной аутоагрессии лежит единый механизм — образование клонов Т- и В-лимфоцитов, а также Ig, действующих против собственных интактных структур. При них, как правило, выявляются признаки наследственной предрасположенности. Это однозначно показано для таких болезней как СКВ, иммуноагрессивные формы гемолитической анемии, тиреоидита, ревматоидного артрита. У многих пациентов с этими и другими болезнями иммунной аутоагрессии выявлены их маркёры.
Иммунонезависимые болезни иммунной аутоагрессии Патогенез иммунонезависимых (антигензависимых, ИБН-независимых) болезней иммунной аутоагрессии не отличается от естественного хода нормальных реакций иммунитета, но иммунологической атаке подвергаются генетически неизменённые аутологичные структуры собственного организма.
|
№ 78 Опухоли: характеристика основных понятий. Этитология опухолей: основные группы, конкретные примеры канцерогенных факторов и условий, способствующих реализации их действия. Понятия об этапах инициации и промоции опухолевого роста.
Опухоль — типовая форма нарушения тканевого роста, возникающая под действием канцерогена. Проявляется патологическим разрастанием структурных элементов ткани. Характеризуется атипизмом роста, обмена веществ, структуры и функции. ЦИТО- И ГИСТОДИФФЕРЕНЦИРОВКА Цитологическая и гистологическая дифференцировка опухолевых клеток и опухолей позволяет выделять доброкачественные и злокачественные опухоли. Доброкачественные опухоли. Клетки доброкачественной опухоли морфологически идентичны или похожи на нормальные клетки—предшественники и формируют характерные — высокодифференцированные для данной ткани структуры. Такие опухоли растут медленно, не метастазируют и с клинической и прогностической точек зрения их расценивают как доброкачественные. Злокачественные опухоли. Клетки злокачественной опухоли морфологически отличаются от нормальной клетки—предшественника, соседних опухолевых клеток и образуют искажённые тканевые структуры (или вовсе их не образуют) — низкодифференцированные, анапластические. Эти опухоли растут быстро, прорастают в соседние структуры, а отдельные опухолевые клетки формируют близко расположенные или отдалённые точки роста — метастазы. С клинической и прогностической точек зрения такие опухоли расценивают как злокачественные. Различают следующие типы злокачественных опухолей. • Карциномы — злокачественные опухоли, происходящие из эпителия. • Аденокарциномы — злокачественные опухоли, происходящие из эпителия и имеющие железистый компонент. • Саркомы — злокачественные опухоли, происходящие из тканей мезенхим-ного происхождения (соединительные, костные, хрящевые). Причиной опухолей являются канцерогенные агенты химической, биологической и физической природы, а главным условием, способствующим реализации их действия (фактором риска) — снижение эффективности антиканцерогенных механизмов противоопухолевой защиты организма. В значительной мере это определяется генетической предрасположенностью. Генетическая предрасположенность Существует не менее 300 так называемых семейных форм злокачественных заболеваний. В ряде случаев генетическая природа предрасположенности к возникновению опухолей определена. К числу наиболее значимых относятся: • Аномалии генов, осуществляющих репарацию ДНК. Это определяет повышенную чувствительность к канцерогенным эффектам ультрафиолетового облучения, химических воздействий, радиации и других факторов. • Аномалии генов-супрессоров опухолевого роста • Аномалии генов, ответственных за межклеточное взаимодействие ХИМИЧЕСКИЕ КАНЦЕРОГЕНЫ Более 75% случаев злокачественных опухолей человека вызвано воздействием химических факторов внешней среды. К возникновению опухолей приводят преимущественно факторы сгорания табака; химические агенты, входящие в состав пищи и соединения, используемые в различных сферах производства. Примеры: компоненты сгорания угля в печах часто вызывают рак мошонки у трубочистов; асбест — мезотелиому плевры, табакокурение — плоскоклеточную карциному лёгких. Наиболее опасные канцерогены относятся к нескольким классам химических веществ.
Этапы химического канцерогенеза Выделяют два взаимосвязанных этапа химического канцерогенеза: инициации и промоции. Этап инициации. На этапе инициации происходит взаимодействие конечного канцерогена с локусами ДНК, содержащими гены, контролирующие деление и созревание клетки (протоонкогенами). Возможны два варианта взаимодействия: геномный и эпигеномный. • Геномный механизм заключается в точковой мутации протоонкогена. • Эпигеномный механизм характеризуется дерепрессией неактивного протоонкогена. Под действием химических канцерогенов протоонкоген превращается в онкоген, который и обеспечивает в последующем процесс опухолевой трансформации клетки. И хотя такая клетка ещё не имеет опухолевого фенотипа (её называют латентной опухолевой клеткой), процесс инициации уже необратим. Этап промоции. Процесс промоции индуцируют различные канцерогенные агенты, а также клеточные факторы роста. На этапе промоции: осуществляется экспрессия онкогена; происходит неограниченная пролиферация клетки, ставшей генотипически и фенотипически опухолевой; формируется новообразование. КАНЦЕРОГЕНЫ БИОЛОГИЧЕСКОЙ ПРИРОДЫ К канцерогенам биологической природы относят онкогенные (опухолеродные) вирусы. Роль вирусов в канцерогенезе привлекает внимание, с одной стороны, как самостоятельная проблема, а с другой, в связи с тем, что большое число клеточных протоонкогенов сходны с онкогенами ретровирусов. Примеры. Вирус Эпстайна—Барр приводит к развитию лимфомы Беркетта и носоглоточной карциномы; вирус простого герпеса 2 — рака шейки матки; вирус Т-клеточного лейкоза человека типа 1 — Т-клеточного лейкоза у взрослых; вирус гепатита В — гепатоклеточной карциномы. Этапы вирусного канцерогенеза • Проникновение онкогенного вируса в клетку. • Включение вирусного онкогена в геном клетки. • Экспрессия онкогена. • Превращение клетки в опухолевую. • Образование опухолевого узла. ФИЗИЧЕСКИЕ КАНЦЕРОГЕННЫЕ ФАКТОРЫ К ним относятся, главным образом, радиационное и ультрафиолетовое излучения. Примеры: ультрафиолетовый спектр света может вызвать плоскоклеточную карциному кожи; ионизирующее излучение — рак лёгких у шахтёров урановых рудников, лейкозы у переживших атомную бомбардировку (Хиросима) и атомную катастрофу (Чернобыль); а папиллярный рак щитовидной железы возникает у больных, прошедших лучевую терапию области шеи. Этапы физического канцерогенеза Мишенью канцерогенных агентов физической природы также является ДНК. Допускается либо их прямое действие на ДНК, либо через посредники — своеобразные медиаторы канцерогенеза. К последним относят свободные радикалы кислорода, липидов и других органических и неорганических веществ. • Первый этап физического канцерогенеза — инициация опухолевого роста. Он заключается в прямом или опосредованном воздействии агентов физической природы на ДНК. Это вызывает либо повреждение её структуры, либо эпигеномные изменения. Как первое, так и второе может привести к активации протоонкогенов и последующую опухолевую трансформацию клетки. • Второй этап — промоции. На этом этапе канцерогенеза осуществляется экспрессия онкогена и модификация нормальной клетки в раковую. В результате последовательных циклов пролиферации формируется опухоль. |
|
|
||
|
|
|
№ 79 Основные этапы и механизмы трансформации нормальной клетки в опухолевую. Понятие об онкогенах и онкосупрессорах (“антионкогенах”).
Несмотря на большое число канцерогенных агентов и разнообразие клинических форм опухолевого роста на уровне клетки происходит общее закономерное изменение — трансформация нормальной генетической программы в программу формирования опухолевого атипизма. В основе опухолевой трансформации лежат стойкие изменения ДНК. При этом программа опухолевого роста становится фрагментом общей реализуемой клеткой программы, закодированной в её геноме. Единый конечный результат действия канцерогенов различной природы (химической, биологической, физической) на клетки и как результат — их опухолевая трансформация, обеспечивается нарушением взаимодействия в клеточном геноме онкогенов и антионкогенов. Стимуляция канцерогенными агентами экспрессии онкогенов и/или депрессия антионкогенов и обеспечивает опухолевую трансформацию клеток. Онкогены. Вирусные онкогены и контролирующие клеточный цикл и пролиферацию клеточные гены имеют как сходство, так и важные отличия. В связи с этим говорят о протоонкогенах и онкогенах. Протоонкоген — ген нормального генома человека; участвует в регуляции пролиферации клеток. Продукты экспрессии протоонкогенов во многих случаях важны для нормальной дифференцировки клеток и межклеточных взаимодействий. В результате соматических мутаций протоонкоген может стать онкогенным. Онкоген • Онкоген — один из генов, в обычных условиях (т.е. в качестве протоонкогена) кодирующий белок, обеспечивающий пролиферацию и диф-ференцировку клеточных популяций. У опухолевых ДНК-вирусов онкогены кодируют нормальные вирусные белки; онкогены, однако, могут спровоцировать — в случае их мутаций или активации ретровирусами — злокачественный рост. • Онкогены найдены в некоторых ДНКовых опухолевых вирусах. Они необходимы для репликации вируса (трансформирующий ген). • К онкогенам относятся также гены вируса или ретровируса, вызывающие злокачественное перерождение клетки-хозяина, но необязательные для репликации вируса. Онкосупрессоры. Трансформированные (опухолевые) клетки делятся бесконтрольно и неограниченно долго. Онкосупрессоры, или антионкогены тормозят их пролиферацию. ЭТАПЫ КАНЦЕРОГЕНЕЗА Вне зависимости от конкретной причины опухолевой трансформации клетки, гистологической структуры и локализации новообразования, в процессе онко-генеза можно условно выделить несколько общих этапов. • На первом этапе происходит взаимодействие канцерогенов химической, физической и биологической природы с протоонкогенами и антионкогенами (онкосупрессорами) генома нормальной клетки. • В результате такого взаимодействия на втором этапе канцерогенеза подавляется активность онкосупрессоров, а также происходит трансформация протоонкогенов в онкогены. Экспрессия онкогена — необходимое и достаточное условие для трансформации нормальной клетки в опухолевую. • В результате подавления активности онкосупрессоров и экспрессии онкогенов на третьем этапе синтезируются и реализуют свои эффекты (непосредственно или с участием клеточных факторов роста и рецепторов к ним) он-кобелки. С этого момента генотипически изменённая клетка приобретает опухолевый фенотип. • На четвёртом этапе опухолевая клетка начинает бесконтрольно проли-ферировать, что ведёт к формированию новообразования (опухолевого узла). |
№ 80 Характеристика опухолевого атипизма роста, обмена веществ, функции, структуры: механизмы, проявления, последствия.
Общая характерная черта трансформированных клеток — опухолевый атипизм. Опухолевый атипизм проявляется большим числом признаков, характеризующих рост, структуру, метаболизм и функции клеток. Атипизм роста. Атипизм клеточного роста характеризуется своеобразием пролиферации опухолевых клеток, расстройствами их дифференцировки, инвазивным ростом, метастазированием и рецидивированием.
Атипизм пролиферации. В опухоли значительно увеличено количество делящихся клеток. В опухолях число пролиферирующих клеток превышает в очень большое количество раз. Увеличение числа делящихся клеток ведёт к быстрому нарастанию массы солидной опухоли или суммарного количества клеток (например, лейкозных) при гемобластозах. Атипизм дифференцировки. Заключается в частичном или полном подавлении процесса созревания (дифференцировки) опухолевых клеток. Инвазивный рост. Характеризуется проникновением клеток опухоли в окружающие нормальные ткани. Сочетается с их деструкцией. Метаболический атипизм. Атипизм обмена веществ (метаболический, биохимический) заключается в существенном изменении всех видов обмена: нуклеиновых кислот, белков, углеводов, липидов, ионов, жидкости, витаминов. В связи с этим закономерно изменяются и физико-химические параметры опухолевых клеток и новообразования в целом. Атипизм обмена нуклеиновых кислот. В опухоли увеличен синтез ДНК и РНК. Атипизм белкового обмена. Проявления: - Усиление включения аминокислот в реакции протеосинтеза - Интенсификация синтеза различных классов белков (структурных, ферментов, онкобелков и других) при одновременном уменьшении или прекращении синтеза ряда иных белков. - Изменение антигенного профиля опухолей. Это обусловлено модификациями макромолекул белка. Нарушения метаболизма белка в новообразованиях, с одной стороны, обеспечивают реализацию большинства других проявлений их атипизма, лежащих в основе прогрессирующего опухолевого роста, а с другой — способствуют активации механизмов антибластомной защиты организма, обусловленной появлением у клеток опухоли Аг, не свойственных нормальным аутологичным клеткам. Атипизм обмена углеводов. Метаболизм углеводов в опухолях характеризуется рядом особенностей. Проявления: - Активация реакций транспорта и утилизации клетками бластомы глюкозы. - Уменьшение относительной доли тканевого дыхания при ресинтезе АТФ. - Интенсификация процесса прямого окисления углеводов в пентозофос-фатном цикле. Атипизм обмена липидов. Проявления: - Значительное усиление утилизации ВЖК и холестерина. - Активация синтеза липидных структур клеток. - Интенсификация процессов липопероксидации. Изменение липидного метаболизма в новообразованиях направлено на энергетическое и пластическое обеспечение усиленных анаболических процессов, реакций синтеза структур интенсивно делящихся бластомных клеток. Подобные отклонения в опухолях нередко сочетаются с торможением развития ате-росклеротических изменений в стенках сосудов у онкологических больных. Атипизм обмена ионов и воды. В новообразованиях наблюдается избыточное (в сравнении с нормальными аутологическими тканями) накопление ряда ионов и воды, а также изменение соотношения отдельных ионов как в цитозоле бластомных клеток, так и межклеточной жидкости. Отклонения характера обмена ионов и воды в новообразованиях способствует реализации других видов атипизма: роста, функции и структуры. Это, в свою очередь, повышает приспособляемость опухоли. Атипизм обмена витаминов. Особенности обмена витаминов в опухолевой ткани изучены недостаточно. Проявления: - Многие витамины интенсивно захватываются клетками бластомы. Полагают, что витамины в опухоли используются в качестве предшественников различных коферментов (как и в нормальных клетках), а также — субстратов обмена веществ и пластических процессов, обеспечивающих интенсивный рост и деление бластомных клеток. - Различные опухоли являются «ловушкой» жирорастворимого витамина Е. Он обладает антиоксидантной активностью в связи с его способностью нейтрализовать свободнорадикальные агенты и способствовать стабилизации клеточных мембран. По-видимому, это является одним из механизмов повышения устойчивости опухолевых клеток к цитотоксическим воздействиям. Атипизм функций. Обычно функции клеток новообразования снижены и/или качественно изменены, реже — повышены. Гипофункция. Как правило, отдельные опухолевые клетки и новообразование в целом характеризуются пониженным функционированием. Гиперфункция. Нередко наблюдаются признаки гиперфункции как отдельных раковых клеток, так и опухоли в целом. Обычно речь идет о неадекватной потребностям организма продукции каких-либо веществ. Дисфункция. В некоторых опухолях выявляются признаки, не свойственные для нормальных аутологичных тканей. Таким образом, атипизм функции опухолей обусловливает нарушение деятельности тканей и органов, которые они поражают, а также — расстройство жизнедеятельности организма-опухоленосителя. С учётом этого в онкологии сложилось представление об опухолевой болезни. Метастазирование — одно из фатальных проявлений атипизма опухолевого роста — перенос клеток бластомы на расстояние от основного (материнского) узла и развития опухоли того же гистологического строения в другой ткани или органе. Рецидивирование — повторное развитие новообразования того же гистологического строения на прежнем месте после его удаления или деструкции. |
№ 81 Понятие об опухолевой прогрессии. Характеристика механизмов противоопухолевой защиты организма. Принципы профилактики и лечения опухолей.
Опухолевая прогрессия — генетически закреплённое, наследуемое опухолевой клеткой и необратимое изменение одного или нескольких свойств клетки. ПРОТИВООПУХОЛЕВАЯ ЗАЩИТА ОРГАНИЗМА Различают антиканцерогенные, антимутационные и антицеллюлярные механизмы противоопухолевой защиты. Антиканцерогенные механизмы Антиканцерогенные механизмы обеспечивают торможение и/или блокаду проникновения канцерогенов в клетку, её ядро, действие их на геном и инактивацию и элиминацию бластомогенных агентов из клетки и организма. Механизмы, препятствующие действию химических канцерогенных факторов - Физико-химическая фиксация и удаление из организма - Поглощение канцерогенов в процессе фагоцитоза, сочетающееся с их инактивацией и разрушением. - Инактивация бластомогенных агентов как гаптенов при помощи AT и Т-лимфоцитов с последующей их деструкцией и элиминацей из организма. - Конкурентная блокада неканцерогенными метаболитами клеточных рецепторов, с которыми способны взаимодействовать истинные бластомогенные вещества. - Разрушение и/или инактивация канцерогенов в клетках и биологических жидкостях в процессе их окисления, восстановления, деметилирования, глюкуронизации, сульфатирования. - Ингибирование («гашение») свободных радикалов и гидроперекисей органических и неорганических соединений ферментативными и неферментными факторами антиоксидантной защиты. Механизмы, препятствующие действию онкогенных вирусов - Инактивация вирусов Ig, образуемыми плазматическими клетками под влиянием антигенных вирусных белков. - Ингибирование ИФН — белками, тормозящими или блокирующими процесс внутриклеточной репликации вирусов. - Обнаружение и разрушение вируссодержащих клеток организма неспецифическими цитолитическими клетками. Механизмы, препятствующие действию канцерогенов физической природы - Улавливание и/или инактивация свободных радикалов кислорода, липидов, других органических и неорганических веществ. - Разрушение перекисей и гидроперекисей различных веществ. Антимутационные механизмы Антимутационные механизмы обеспечивают обнаружение, устранение или подавление активности онкогенов. Реализуются антимутационные механизмы при участии онкосупрессоров и систем репарации ДНК. При недостаточности антимутационных механизмов и активации онкогенов нормальная клетка приобретает опухолевый генотип и характерные для него фенотипические признаки. Это служит сигналом для включения антицеллю-лярных механизмов противоопухолевой защиты. Антицеллюлярные механизмы Антицеллюлярные механизмы обеспечивают обнаружение и разрушение гено-типически и фенотипически чужеродных для организма опухолевых клеток или торможения их роста. Сигналом для активации антицеллюлярных механизмов противоопухолевой защиты организма является генетическая чужеродность клеток бластомы. Различают неиммунные (неспецифические) и иммунные (специфические) антицеллюлярные механизмы. Неиммунные механизмы. Эти механизмы осуществляют надзор за сохранением нормального (индивидуального и однородного) клеточного состава организма. Реализуют эти механизмы как клетки, так и гуморальные факторы. Иммунные механизмы. Эти механизмы реализуют клеточное и гуморальное звенья иммунитета. ПРОФИЛАКТИКА ОПУХОЛЕЙ Цель профилактики новообразований: предупредить действие на клеточный геном клеток канцерогенов, значительно снизить их бластомогенное действие и предотвратить тем самым возникновение опухолевой клетки. Мероприятия • Снижение содержания или устранение в окружающей человека среде канцерогенных агентов. • Индивидуальную защиту организма, особенно на производстве • Повышение общей и противоопухолевой устойчивости организма. • Своевременное (максимально раннее) обнаружение и ликвидацию так называемых предопухолевых состояний. ПРИНЦИПЫ ЛЕЧЕНИЯ ОПУХОЛЕЙ Общие подходы Лечение опухолей может быть радикальным и паллиативным. Радикальное лечение направлено на ликвидацию опухоли и предполагает возможность полного выздоровления либо длительной ремиссии. Паллиативное лечение применяют при невозможности проведения радикальной терапии. Лечение приводит к удлинению жизни и уменьшению страданий. Риск рецидива достаточно велик, хотя первоначально больной может чувствовать себя полностью здоровым. Большинство онкологических больных лечат хирургически и с применением лучевой терапии, химиотерапии и иммунотерапии. Выбор метода лечения зависит от характера заболевания, стадии, гистологического типа опухоли, возраста больного, наличия сопутствующих заболеваний и цели лечения (излечение или паллиативное вмешательство). Хирургическое вмешательство и лучевая терапия воздействует на первичную опухоль и регионарные лимфатические узлы. Ни тот, ни другой метод не влияет на области отдалённого распространения. Химиотерапия и иммунотерапия — системные методы лечения, способны воздействовать на области отдалённого распространения. Дополнительное лечение — системная терапия, применяемая после местного лечения (например, резекции) при высоком риске наличия микроскопического очага в лимфатических узлах или отдалённых органах. У значительной части таких больных развивается рецидив, цель дополнительного лечения — уничтожение этих удалённых и микроскопических очагов опухоли. Комплексное лечение использует преимущества каждого метода лечения для компенсации недостатков других. |
|
|