
ПРОЦЕССЫ И АППАРАТЫ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ(ЗАДАЧНИК) Авторы Р. Б. Комляшев, А. В. Вешняков, М. А. Носырев
.pdfМИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Российский химико-технологический университет имени Д. И. Менделеева
ПРОЦЕССЫ И АППАРАТЫ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ. ГИДРОДИНАМИКА И ТЕПЛООБМЕН.
ЗАДАЧНИК
Москва
2017
УДК 66.02(076.1) ББК 35.111: 35.113я7
П845
Авторы:Р. Б. Комляшев, А. В. Вешняков, М. А. Носырев
Рецензенты:
Процессы и аппараты химической технологии. Задачник: в 2 ч.:
П845 учеб. пособие / Р. Б. Комляшев, А. В. Вешняков, М. А. Носырев. – М.: РХТУ им. Д. И. Менделеева, 2016.
ISBN 978-5-7237-
Ч. 1. Гидродинамика и теплообмен. – 120 с. ISBN 978-5-7237-
Представлен ряд расчётных заданий для самостоятельной работы студентов на семинарах по курсу процессов и аппаратов химической технологии: гидродинамические и теплообменные процессы. Представлены основные расчётные формулы, рекомендуемый порядок расчёта, необходимые для расчёта справочные данные по физическим свойствам веществ и характеристикам оборудования. Предназначено для студентов, обучающихся по направлению подготовки бакалавров 240100, 240300, 241000, специалистов 240300, 240700.
|
УДК 66.021(075) |
|
|
ББК 35.111; 35.113я7 |
|
ISBN 978-5-7237- (ч. 1) |
© Российский химико-технологический |
|
ISBN 978-5-7237- |
||
университет им. Д. И. Менделеева, 2016 |
||
|
ПРЕДИСЛОВИЕ
Задачник по курсу «Процессы и аппараты химической технологии»
3

РАСЧЁТ ПЛОТНОСТИ И ВЯЗКОСТИ
Задача 1
Методом линейной интерполяции по табличным данным определить плотность и вязкость органической жидкости (бензол) при температуре
23,6 °C.
Решение
Плотность жидкостей находим по [1, с. 512, табл. IV; 2, с. 14].
Находим в таблице две температуры, ближайшие к заданной, и плотности заданного вещества при этих температурах:
при 20 °C ρ1 = 879,0 кг/м3, при 30 °C ρ2 = 868,4 кг/м3.
Как видно, плотность жидкостей убывает с ростом температуры. Линейную интерполяцию проиллюстрируем графиком (рис. 1), на котором схематично изобразим зависимость плотности от температуры.
ρ
879,0
ρ 
868,4
20 |
t = 23,6 |
30 |
t |
Рис. 1. Линейная интерполяция плотности по методу подобных треугольников
На рис. 1 мы получили два подобных прямоугольных треугольника: большой и малый (заштрихованный). Соотношения катетов в подобных тре-
угольниках равны: 879,0 |
868,4 |
|
868,4 . |
||||
|
|
|
30 |
20 |
|
30 t |
|
Выражаем искомую плотность: |
|
|
|||||
868,4 |
879,0 |
868,4 |
30 t 875,2кг м3 . |
||||
30 |
20 |
|
|||||
4

Вязкость жидкостей находим по [1, с. 516-517, табл. IX; 2, с. 15]. Находим в таблице две температуры, ближайшие к заданной, и вязкости заданного вещества при этих температурах:
при 20 °C μ1 = 0,649 мПа·с, при 30 °C μ2 = 0,559 мПа·с.
Как видно, вязкость жидкостей убывает с ростом температуры. Линейную интерполяцию проиллюстрируем графиком (рис. 1), на котором схематично изобразим зависимость вязкости от температуры.
μ
0,649
μ 
0,559
20 |
t = 23,6 |
30 |
t |
Рис. 2. Линейная интерполяция вязкости по методу подобных треугольников
На рис. 1 мы получили два подобных прямоугольных треугольника: большой и малый (заштрихованный). Соотношения катетов в подобных тре-
угольниках равны: |
0,649 |
0,559 |
|
0,559 . |
|
30 |
20 |
|
30 t |
Выражаем искомую вязкость:
0,559 0,649 0,559 30 t 0,617 мПа с. 30 20
Задача 2
Рассчитать плотность и вязкость бинарной смеси органических веществ при температуре 20 °C, если низкокипящий компонент смеси – бензол, высококипящий компонент – толуол. Мольная доля низкокипящего компонента в смеси 70 %.
Решение
Молярные массы жидкостей находим в [2, с. 13]:
5

MНК 78,114кг кмоль, MВК 92,141кг
кмоль, MВК 92,141кг кмоль. Пересчитываем мольную долю в массовую:
кмоль. Пересчитываем мольную долю в массовую:
xНК |
xНК МНК |
|
0,7 78,114 |
0,6641 |
|
xНК МНК 1 xНК МВК |
0,7 78,114 1 0,7 92,141 |
|
|||
Находим плотности компонентов при заданной температуре: ρНК = 879,0 кг/м3, ρВК = 866,9 кг/м3.
Плотность смесей органических жидкостей, не обладающих значительным объёмным эффектом смешения, находим по формуле:
|
|
|
|
1 |
|
|
|
|
|
1 |
|
|
|
|
|
1 |
|
|
|
874,9кг м3 . |
||
см |
|
x |
|
|
x |
|
1 x |
|
|
0,6641 |
|
|
1 0,6641 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
i |
|
|
|
НК |
|
НК |
|
|
|
|
|
|
|
|
|
||||
|
|
i |
|
|
|
НК |
ВК |
|
|
|
879,0кг м |
3 |
866,9кг м |
3 |
|
|
||||||
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Находим вязкости компонентов при заданной температуре: μНК = 0,649 мПа·с, μВК = 0,584 мПа·с.
Вязкость смесей органических жидкостей, не обладающих значительным объёмным эффектом смешения, находим по формуле:
|
|
xi lg i |
x |
lg |
|
1 x |
lg |
|
|
|
|
|
10 i |
|
ВК |
||||||
см |
10 НК |
|
НК |
|
НК |
|||||
100,7lg 0,649мПа с 1 0,7 lg 0,584мПа с |
0,629мПа с. |
|||||||||
Задача 3
Методом последовательных линейных интерполяций определить плотность и вязкость водного раствора этанола при температуре 14 °C, если массовая доля растворённого вещества в растворе 43 %.
Решение
По табл. 3 и 4 находим значения плотности и вязкости раствора, при тем-
пературах и составах, наиболее близких к заданным. |
|
|
|||||||
Плотность ρ, кг/м3 |
|
Вязкость μ, мПа·с |
|
||||||
|
|
, |
t, °C |
|
|
|
, |
|
t, °C |
|
x |
|
x |
|
|||||
% масс. |
10 |
20 |
% масс. |
10 |
20 |
||||
40 |
942,6 |
935,1 |
40 |
4,39 |
2,91 |
||||
50 |
921,8 |
914,0 |
50 |
4,18 |
2,87 |
||||
Последовательно производим линейную интерполяцию плотности и вязкости сначала по температуре, а потом по составу.
6

Плотность 40 %-го раствора при 14 °C:
40%,14 С 935,1 942,6 935,1 20 14 939,6кг м3 . 20 10
Плотность 50 %-го раствора при 14 °C:
50%,14 С 914,0 921,8 914,0 20 14 918,7 кг м3 . 20 10
Плотность 43 %-го раствора при 14 °C:
43%,14 С 918,7 939,6 918,7 50 43 933,3кг м3 . 50 40
Вязкость 40 %-го раствора при 14 °C:
40%,14 С 2,91 4,39 2,91 20 14 3,80мПа с. 20 10
Вязкость 50 %-го раствора при 14 °C:
50%,14 С 2,87 4,18 2,87 20 14 3,66мПа с. 20 10
Вязкость 43 %-го раствора при 14 °C:
43%,14 С 3,66 3,80 3,66 50 43 3,76мПа с. 50 40
Задача 4
Определить плотность и вязкость азота, при температуре 25 °C и давление 0,2 МПа.
Решение
Молярная масса, вязкость при нормальных условиях и константа Сазерленда для газов [1, с. 513, табл. V; 2, с. 12]:
MN2 28,013кг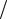 кмоль, 0 N2 16,52мкПа с, C 103,9К.
кмоль, 0 N2 16,52мкПа с, C 103,9К.
Считая газ идеальным, определяем плотность через молярный объём:
|
|
|
МN |
2 |
Т |
0 |
|
р |
|
|
28,013кг кмоль |
273К |
|
0,2 106 Па |
2,261 |
кг |
, |
||||||
N2 |
V0 |
|
Т |
р |
|
22,4м3 |
кмоль |
|
(273 25) К 101325Па |
м3 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
m |
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
или через универсальную газовую постоянную: |
|
|
|
|
|||||||||||||||||||
N2 |
|
|
р МN |
2 |
|
|
0,2 106 |
Па 28,013 |
кг кмоль |
2,261 |
кг |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
м3 . |
|
|
|
|||||||||||
|
R T |
|
|
|
8314 |
кДж |
|
(273 |
25) К |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
кмоль×К |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Вязкость газа рассчитываем, пренебрегая влиянием давления:
7

|
|
273 103,9 |
|
273 25 |
1,5 |
|
|||
N2 |
16,52мкПа с |
|
|
|
|
|
|
17,67 мкПа с. |
|
273 |
25 |
103,9 |
273 |
||||||
|
|
|
|
|
|||||
Задача 5
Определить плотность и вязкость паров, полученных испарением 43 %-го (массовые %) раствора этанола. Температура паров 100 °С, давление нормальное атмосферное.
Решение
Пересчитываем массовые доли в молярные:
x |
|
x МНК |
|
|
|
0,43 |
46,069 |
0,2278. |
x |
МНК 1 x |
МВК |
0,43 |
46,069 |
1 0,43 18,015 |
При испарении не происходит изменения массовых и молярных долей вследствие закона сохранения массы. Кроме того, для паров молярные доли являются также и объёмными, поскольку молярный объём примерно одинаков для любого газообразного вещества и зависит только от температуры и давления.
Следовательно, объёмная доля спирта в паровой фазе: Молярная масса паровой смеси:
Mсм MНК x MВК 1 x
46,069кг кмоль 0,2278 18,015кг
кмоль 0,2278 18,015кг кмоль 1 0,2278 24,41кг
кмоль 1 0,2278 24,41кг кмоль.
кмоль.
Плотность паров:
|
|
|
Мсм Т0 |
р |
|
24,41кг кмоль 273К 760 |
мм рт.ст. |
0,7976 |
кг . |
||||
см |
|
|
|
|
|
||||||||
V0 |
Т |
р |
22,4м3 кмоль (273 100) К 760 |
ммрт.ст. |
|||||||||
|
|
|
|
м3 |
|||||||||
|
|
|
m |
|
0 |
|
|
|
|
|
|
|
|
Вязкость паров органических веществ при нормальном атмосферном давлении и температуре 100 °С [2, с. 22]: НК 10,83мкПа с.
Вязкость водяного пара при нормальном атмосферном давлении и температуре 100 °С:
либо находим по справочнику [3, с. 1001] ВК 124мкПз 12,4мкПа с, либо рассчитываем через константу Сазерленда
|
273 945 |
|
273 100 |
1,5 |
|
|||
ВК 8,24 10мкПа с |
|
|
|
|
|
|
12,16мкПа с |
|
273 |
100 |
945 |
273 |
|||||
|
|
|
|
|||||
8

Вязкость паровой смеси: |
|
|
|
Мсм |
|
|
|
|
|
||||||
см |
|
xi Mi |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
i |
|
i |
|
|
|
|
|
|
|
24,41кг кмоль |
|
|
|
|
|
|
|
11,45мкПа с. |
||||||
|
|
|
|
|
|
|
|||||||||
0,2278 46,069 |
кг |
|
1 0,2278 18,015 |
кг |
|
|
|||||||||
|
кмоль |
|
|
|
|||||||||||
|
кмоль |
|
|
|
|||||||||||
|
10,83мкПа с |
|
|
12,4мкПа с |
|
|
|
||||||||
Задача 6
Определить плотность и вязкость дымовых газов, полученных при сжигании углерода. Температура дымовых газов 300 °С, давление 745 мм рт. ст. Коэффициент избытка воздуха 1,2.
Решение
Уравнение реакции сгорания: С + О2 → СО2 Задаваясь количеством углерода равным 1 моль, получаем: nCO2 nC 1моль.
Исходное количество кислорода с учётом коэффициента избытка: nO2 исх nCO2 1,2 1моль 1,2моль.
Конечное количество кислорода (за вычетом прореагировавшего): nO2 кон nO2 исх nCO2 1,2моль 1моль 0,2моль.
Количество азота не меняется в процессе реакции и определяется соотношением азота и кислорода в исходном воздухе:
n |
n исх |
yN |
2 |
|
1,2моль |
0,79 |
4,514моль. |
|
|
|
|
|
|||||
N2 |
O2 |
|
yO2 |
|
0,21 |
|
||
Суммарное количество вещества дымовых газов: |
||||||||
ni nCO2 |
nO2 |
кон nN2 1моль 0,2моль 4,514моль 5,714моль. |
||||||
i |
|
|
|
|
|
|
|
|
Рассчитаем молярные (объёмные) доли компонентов дымовых газов:
xCO2 |
|
nCO2 |
|
|
1моль |
0,175; |
xO2 |
nO2 |
кон |
|
0,2моль |
0,035; |
||||
ni |
|
5,714моль |
ni |
5,714моль |
||||||||||||
|
|
|
i |
|
|
|
|
|
|
|
i |
|
|
|
|
|
xN2 |
|
nN2 |
|
4,514 |
моль |
0,790. |
|
|
|
|
|
|
||||
ni |
|
5,714 |
моль |
|
|
|
|
|
|
|||||||
i
9

Рассчитаем молярную массу дымовых газов: Mсм Mi xi
i
44,01 |
кг |
|
0175, |
32,0 |
кг |
0,035 28,01 |
кг |
0,790 30,95 |
кг |
. |
|
|||||||||
кмоль |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
кмоль |
|
кмоль |
|
|
кмоль |
|
||||||
Рассчитаем плотность дымовых газов: |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
Мсм Т0 |
р |
30,95кг кмоль |
273К |
745 |
мм рт.ст. |
0,645 |
кг . |
||||||||||
см |
V0 Т |
|
|
|
|
|
|
мм рт.ст. |
||||||||||||
|
|
|
р |
22,4м3 кмоль (273 300) К 760 |
|
|
|
м3 |
||||||||||||
|
|
|
m |
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Рассчитаем вязкость компонентов, взяв начения вязкости при нормальных |
|||||||
условиях μ0 и константы Сазерленда из [2, c. 12]: |
|||||||
CO2 0 CO2 |
273 СCO2 |
|
Т |
1,5 |
|
||
|
|
|
|
|
|||
Т СCO2 |
273 |
||||||
|
|
|
|
||||
13,75мкПа с |
273 254 |
|
573 |
1,5 |
25,13мкПа с; |
|
573 |
254 |
|
273 |
|
||
|
|
|
|
|||
O2 |
|
273 127 |
|
573 |
1,5 |
|
|
19,24 10мкПа с |
573 |
127 |
|
273 |
|
33,43мкПа с; |
|
|
|
|
|
|
|||
N2 16,52мкПа с |
273 103,9 |
|
573 |
1,5 |
|
|
|
|
|
||||||||
573 |
103,9 |
|
273 |
|
28,71мкПа с. |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Рассчитаем вязкость дымовых газов, воспользовавшись двумя различными |
|
||||||||||||||||
формулами и сравнив полученные результаты (значения |
|
см. [1, |
|
||||||||||||||
MiTкр i |
|
||||||||||||||||
табл. XI]): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
i xi |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
см |
|
Mi Tкр i |
|
|
|
|
|
|
|
|
|
||||||
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
xi |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Mi Tкр i |
|
|
|
|
|
|
|
|
|||||||||
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
25,13мкПа с 0,175 115,5 33,43мкПа с 0,035 70,2 28,71мкПа с 0,79 59,5 |
|
|
||||||||||||||
|
|
|
|
|
|
0,175 115,5 0,035 70,2 0,79 59,5 |
|
|
|||||||||
28,59мкПа с;
см Мxi смMi i i
|
|
|
30,95кг/кмоль |
|
|
|
|
|
|
|
|
||
0,175 44,01кг/кмоль |
|
0,035 32,0кг/кмоль |
|
0,79 28,01кг/кмоль |
||
|
25,13мкПа с |
|
33,43мкПа с |
|
28,71мкПа с |
|
28,62мкПа с.
10
