
- •ФГБОУ ВО УГМУ Минздрава РФ Кафедра биохимии
- •Определение понятия
- •Классификация по хим структуре и функции
- •др. классификации углеводов
- •1. Моносахариды – углеводы, которые не гидролизуются с образованием
- •по количеству атомов
- •Дисахариды – углеводы, которые гидролизуются до 2 моносахаридов.
- •Олигосахариды – углеводы, которые гидролизуются с образованием 2 10 моносахаридов.
- •Полисахариды – углеводы, при гидролизе образуется более 10
- •Полисахариды - по продуктам
- •Гетерополисахариды полимеры, состоящие из биозных (2-компанантных) фрагментов, которые гидролизуются с образованием несколько видов
- •Альфа-глюкоза и бета-глюкоза
- •Глюкоза циклич. форма
- •Глюкоза линейная ф-ла
- •Фрагмент молекулы гликогена
- •пищевой рацион человека
- ••Переваривание – это процесс расщепления веществ до их ассимилируемых форм, заключается в ферментативном
- •Ротовая полость
- •в тонком кишечнике
- ••Лактоза --- галактоза и глюкоза
- •Стадии переваривания углеводов
- •Всасывание
- ••ГЛЮТ-4 (мышечно-жировой тип) в мышцах, адипоцитах. Молекула - из 509 аминокислотных остатков. Ген
- •Всасывание разных моносахаридов
- •Гипотеза Na-градиента транспорта сахара
- •Поступление глюкозы в клетку
- •Пути обмена глюкозы
- •Гликоген
- •Фрагмент молекулы гликогена
- •Инсулин,
- •Уровень глюкозы как фактор гомеостаза
- •Регуляция уровня глюкозы в крови
- •Глюкоза крови у детей
- •Изменения уровня глюкозы в крови
- •Пути обмена глюкозы
- •ВИДЫ ГЛИКОЛИЗА
- •Гликолиз
- •1гексокиназа
- •Гликолиз (схема)
- •Биологическая роль гликолиза
- •НАД (никотинамиддинуклеотид)
- •Глицерофосфатный челночный механизм
- •Глицерофосфатный челночный механизм
- •Глицерофосфатный челночный механизм.
- •Малат-аспартатный челночный механизм
- •Малат-аспартатный челночный механизм
- •Окисление пирувата до ацетил-КоА (окислительное декарбоксилирование
- •Тиаминдифосфат (ТДФ) или Е1-ТПФ
- •В любом гликолизе можно выделить 2 этапа
- •Энергетический баланс гликолиза
- •Регуляция гликолиза анаэробного
- •Регуляция гликолиза
- •COOH
- •Обмен галактозы
- •Обмен галактозы
- •Уридиндифосфат
- •Обмен фруктозы
- •Пентозофосфатный шунт –
- •Синонимы названия ПФП
- •Органные особенности ПФП
- •Валовое уравнение р – и (брутто р - я)
- •окислительнаячасть
- •Структура НАДФ
- •CONH2
- •Регуляторные ферменты окислительного сегмента:
- •Биологическая роль окислительного сегмента
- ••3) в обезвреживании веществ: гидроксилирование ксенобиотиков
- •Функция энергообеспечения
- •Реакции окислительного этапа активно протекают в клетках
- •неокислительнаячасть
- •ферменты неокислительного этапа
- •• Витамин В1 входит в состав
- •Витамин В1 (тиамин)
- •Фосфорилирование витамина В1
- •COOH C O CH3
- •Биороль неокислительного этапа:
- •Регуляция пентозофосфатного пути
- •• Благодарю за внимание !

окислительнаячасть |
|||
Н ОН |
|
О |
|
С |
|
С |
|
Н-С-ОН |
|
Н-С-ОН |
|
НО-С-Н Онадф+ надфн2 НО-С-Н |
О |
||
Н-С-ОН |
гл-6-фосфатДГ |
Н-С-ОН |
|
Н-С |
|
Н-С |
|
Н2С-ОРО3Н2 |
Н2С-ОРО3Н2 |
||
гл-6-ф |
|
6-ф-глюконолактон |
|
|
+ инсулин, НАДФ+ |
|
|
|
- НАДФН2 |
|
|
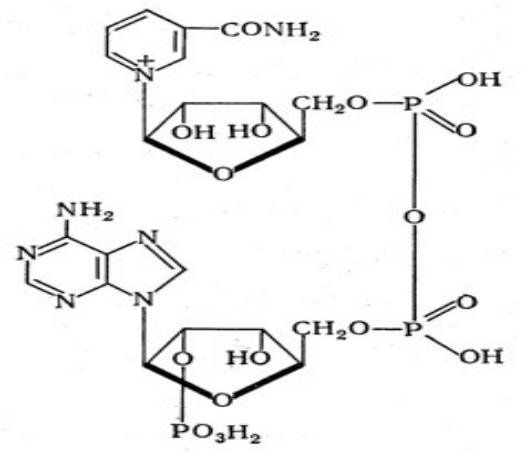
Структура НАДФ

CONH2
+ |
|
+ 2H (2H+/2e-) |
|
N |
|
||
|
|
|
|
R |
|
||
НАД+ |
|
||
HH
CONH2
+ H+
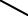 N
N
R
НАДН
О |
|
|
О |
С |
|
|
С-ОН |
Н-С-ОН |
|
|
Н-С-ОН |
НО-С-Н О н2о |
|
НО-С-Н |
|
Н-С-ОН |
глюконолактон- |
Н-С-ОН |
|
Н-С |
гидратаза |
|
Н-С-ОН |
Н2С-ОРО3Н2 |
|
|
Н2С-ОРО3Н2 |
6-ф-глюконолактон |
6-фосфоглюконат |
||

О |
|
|
|
|
|
С-ОН |
|
|
СН2ОН |
|
|
Н-С-ОН |
надф+ |
надфн |
С=О |
|
|
НО-С-Н |
|
2 |
Н-С-ОН |
|
|
|
|
|
|
||
Н-С-ОН |
|
со2 |
Н-С-ОН |
|
|
Н-С-ОН |
6-фосфоглюконатДГ |
Н С-ОРО Н |
|||
Н2С-ОРО3Н2 |
|
2 |
3 |
2 |
|
|
|
|
|
||
6-фосфоглюконат |
|
рибулозо-5-ф |
|||
+ инсулин
Регуляторные ферменты окислительного сегмента:
•1) глюкозо-6-фосфатдегидрогеназа — пусковой фермент;
•2) 6-фосфоглюконатдегидрогеназа.
Биологическая роль окислительного сегмента
•1. Поставщик рибозо-5-фосфата для биосинтезов:
•− мононуклеотидов (АМФ, ГМФ.);
•− нуклеиновых кислот (ДНК, РНК);
•− коферментов (НАД+, НАДФ+, ФАД, КоА- SН).
•2.Основной источник НАДФН.Н+ в клетках.
НАДФН.Н+
вклетках используется:
1)в реакциях биосинтеза как восстановитель:
•жирных кислот;
•холестерина, стероидных гормонов, желчных кислот;
•заменимых аминокислот
2) как кофермент глутаматдегидрогеназы в реакциях восстановительного аминирования α- кетоглутаровой кислот
•3) в обезвреживании веществ: гидроксилирование ксенобиотиков
•4) как антиоксидант: для восстановления окисленного глутатиона
— антиоксиданта клеток;

Hb ( Fe 2+) |
аскорбиновая |
GSSG |
Н2О2 |
к - та |
|
|
|
|
Hb ( Fe 2+) |
дегидроаскорбиновая |
GSH |
|
к – та |
|
глутатионпероксидаза Н2О2 + 2 GSH --------------→ 2 Н2О + G-S-S-G
глутатионредуктаза
GS-SG + НАДФН2 ---------→ 2 GSH + НАДФ+
• Глутатион = глутамил- цистеил –
аланин
• GSH – глутатион восстановленный
• G-S-S-G - глутатион окисленный
5) в фагоцитозе: генерирование активных форм кислорода. Фагоциты с использованием НАДФН.Н+
генерируют супероксидные анион- радикалы для в разрушения поглощённых бактериальных клеток
