
- •Российский химико-технологиченский университет имени д.И.Менделеева кафедра процессов и аппаратов химической технологии
- •1.Цель работы.
- •2. Схема установки.
- •Методика выполнения работы
- •3. Выполнение работы.
- •1.Таблицы опытных данных
- •2. Результаты расчётов
- •4. Графики
- •5. Выводы
- •Список используемой литературы
- •6. Ответы на контрольные вопросы
- •7. Ответы на вопросы преподавателя.
3. Выполнение работы.
1.Таблицы опытных данных
Исходная смесь |
|||||
VF , л |
TF , °C |
xF , мол. доли |
|
nF , кмоль |
mпF , кг |
10 |
118 |
0,315 |
0,1178 |
0,2301 |
11,077 |
Кубовый остаток |
||
TW , °C |
xW , мол. доли |
|
126,5 |
0,20 |
0,0677 |
Дистиллят (средний состав) |
|||||
ρP , кг/м3 |
|
|
|
|
|
1003 |
н/д |
0,992 |
0,972 |
0,971 |
0,907 |
2. Результаты расчётов
Исходная смесь |
Дистиллят |
||||||
mF , кг |
, кг H2О/кг смеси |
cF , кДж/(кг*К) |
HF , кДж |
mp , кг |
|
Hp , кДж |
|
11,077 |
0,315 |
2,729 |
3566,7 |
0,783 |
0,972 |
2088,9 |
|
-
Кубовый остаток
Тепловые потери
Количество подведённой теплоты
mW , кг
, кг H2О/кг смеси
HW , кДж
Qпот , кДж
QT , кДж
10,294
0,068
3471,3
150,0
2143,5
Определение численного значения интеграла |
||||
№ |
x |
y* |
y*-x |
f |
1 |
0,2 |
0,96 |
0,76 |
1,315789 |
2 |
0,22 |
0,965 |
0,745 |
1,342282 |
3 |
0,24 |
0,97 |
0,73 |
1,369863 |
4 |
0,28 |
0,975 |
0,695 |
1,438849 |
5 |
0,315 |
0,98 |
0,665 |
1,503759 |
 (использована
формула прямоугольников)
(использована
формула прямоугольников)
Масса исходной смеси:
mF = VF*ρF = 10*1,1067=11,067 кг (плотность смеси получена интерполяцией значений из приложения 1.)
Мольное количество кубовой жидкости:
nw=
 = 0,1958 кмоль
= 0,1958 кмоль
Масса кубовой жидкости:
mW = nw*MW = nw*( MH2O*xW+MC2H6O2*(1-xW)) = 10,417 кг
Средний мольный состав дистиллята:
 =
=
 = 0,971
= 0,971
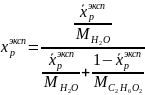 =
= = 0,992
= 0,992
Погрешность определения состава дистиллята:
Δ%=
 =
=
 * 100% = 2,12 %
* 100% = 2,12 %
Количество теплоты QT, необходимой для разделения смеси вода-этиленгликоль (используются значения при Ti ср)

 =
4,1840*0,118 + 2,5344*(1-0,118) = 2,7287
=
4,1840*0,118 + 2,5344*(1-0,118) = 2,7287

 =
4,1861*0,0677+2,5553*(1-0,0677) = 2,6657
=
4,1861*0,0677+2,5553*(1-0,0677) = 2,6657
 =
4,1850*0,972 + 2,5446*(1-0,972) = 4,1391
=
4,1850*0,972 + 2,5446*(1-0,972) = 4,1391
( и
и
 при
,
,
при
при
,
,
при
 ,
,

 получены интерполяцией значений из
приложения 4.)
получены интерполяцией значений из
приложения 4.)
Теплоёмкости воды и этиленгликоля находят при средних температурах:
 ,
,
 ,
,
 ,
,
 =
=

Расчёт величин удельных энтальпий исходной смеси и кубового остатка:
 =
2,7287
*
(118+0) = 322,2226
кДж/кг
=
2,7287
*
(118+0) = 322,2226
кДж/кг
 =
2,6657
* (126,5+0) = 337,1858
кДж/кг
=
2,6657
* (126,5+0) = 337,1858
кДж/кг
– средняя температура дистиллята.

=
2196,38 * 0,9722 + 985,54 * (1-0,972) = 2162,47

 =
4,1391
*122,25
+ 2162,47 = 3850,6406 кДж/кг (при
средней температуре дистиллята TР
ср)
=
4,1391
*122,25
+ 2162,47 = 3850,6406 кДж/кг (при
средней температуре дистиллята TР
ср)
Удельные теплоты парообразования (используются значения при Ti ср)
 =
11,067 * 321,990 = 3566,7 кДж
=
11,067 * 321,990 = 3566,7 кДж
 =
10,417 * 337,206 = 3471,3 кДж
=
10,417 * 337,206 = 3471,3 кДж
 =
0,783 * 2668,473 = 2088,9 кДж
=
0,783 * 2668,473 = 2088,9 кДж



QT = (HP + HW – HF)/0.93 = 2143,5 кДж
 =
=
 =
0,07 * 2143,5 = 150,0 кДж
=
0,07 * 2143,5 = 150,0 кДж

 ,
масс. доли
,
масс. доли ,
масс. доли
,
масс. доли
 ,
мол. доли
,
мол. доли ,
масс. доли
,
масс. доли ,
мол. доли
,
мол. доли ,
масс. доли
,
масс. доли ,
кг H2О/кг
смеси
,
кг H2О/кг
смеси