
- •Лекция 2
- •Карбоновые кислоты – большая группа органических соединений, содержащие в молекулах не менее 1
- •ФИЗИЧЕСКИЕ СВОЙСТВА
- •ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ КАРБОНОВЫХ КИСЛОТ:
- •Дикарбоновые насыщенные:
- •Дикарбоновые ненасыщенные:
- •СТРОЕНИЕ КАРБОКСИЛЬНОЙ ГРУППЫ
- •ОБЩИЕ ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ
- •КАЧЕСТВЕННЫЕ РЕАКЦИИ КАРБОНОВЫХ КИСЛОТ
- •Кето-енольная таутомерия оксокислот
- •Оптическая изомерия гидроксикислот
- •РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ (SN) ПРИ КАРБОНИЛЬНОЙ ГРУППЕ
- •Этерификация/гидролиз сложных эфиров:

Лекция 2
КАРБОНОВЫЕ КИСЛОТЫ.
ГИДРОКСИ-, ОКСОКИСЛОТЫ

Карбоновые кислоты – большая группа органических соединений, содержащие в молекулах не менее 1 карбоксильной группы –СООН.
Карбоновые кислоты классифицируют: 1. По количеству групп СООН:
монокарбоновыедикарбоновыетрикарбоновые
2. По строению углеродного скелета и наличию двойных связей:
ациклические насыщенныеациклические ненасыщенныеароматические
3. По природе дополнительной функциональной группы выделяют:
гидроксикислотыоксокислотыаминокислотыпрочие

ФИЗИЧЕСКИЕ СВОЙСТВА
•Карбоновые кислоты – бесцветные жидкие или твердые вещества, растворимые в органических растворителях.
•Низшие насыщенные карбоновые кислоты (С1 – С9) – жидкости со специфическим резким запахом, обжигают слизистые оболочки. Первые 3 кислоты во всех отношениях смешиваются с водой. При удлинении углеводородного скелета уменьшается растворимость в воде и увеличивается растворимость в малополярных растворителях.
•Высшие жирные кислоты (С10 и более) – твердые вещества, малорастворимые в воде, хорошо растворимы в органических растворителях.
•Низшие ненасыщенные карбоновые кислоты – жидкие, введение двойных связей снижает т. пл. и растворимость в воде.
•Дикарбоновые кислоты - твердые кристаллические вещества, умеренно и хорошо растворимые в воде, при нагревании разлагаются.
•Гидрокси- и оксокислоты – жидкие или твердые кристал- лические вещества, умеренно и хорошо растворимые в воде, при нагревании разлагаются.

ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ КАРБОНОВЫХ КИСЛОТ:
Монокарбоновые насыщенные:
•НСООН – C1, муравьиная, формиат
•СН3СООН – C2, уксусная, ацетат
•СН3СН2СООН - C3, пропионовая, пропионат
•СН3(СН2)2СООН – C4, масляная, бутират
•СН3(СН2)3СООН – C5, валериановая, валерат
•(CH3)2CHCH2COOH – C5,изовалериановая, изовалерат

Дикарбоновые насыщенные:
НООС-СООН - C2, щавелевая, оксалат НООС-СН2-СООН - C3, малоновая, малонат НООС-(СН2)2-СООН - C4, янтарная, сукцинат НООС-(СН2)3-СООН - C5, глутаровая, глутарат
Монокарбоновые ненасыщенные:
CН2=СН-СООН - акриловая, акрилат СН3-СН=СН-СООН - кротоновая, кротонат
H2C C COOH
CH3
- метакриловая, метакрилат

Дикарбоновые ненасыщенные:
|
|
HOOC |
|
|
|
|
|
COOH |
|
|
|
|
H |
|
|
|
|
|
COOH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
C |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
H |
|
|
|
|
|
H |
|
|
HOOC |
|
|
|
|
|
H |
||||||||||||||||||||
малеиновая (цис-), малеат |
фумаровая (транс-), фумарат |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
Гидроксикислоты: |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
|
|
|
|
|
COOH |
H3C |
|
|
CH |
|
|
|
|
|
COOH |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
гликолевая, гликолят |
молочная, лактат |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
HOOC |
|
|
|
|
C |
|
|
|
|
|
|
CH |
|
COOH |
H3C |
|
|
|
CH |
|
|
|
|
|
C2 |
|
COOH |
||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
L-яблочная, L-малат |
3-гидроксимасляная, β-оксибутират |
||||||||||||||||||||||||||||||||||||||
|
|
|
H2C |
|
|
COOH |
|
|
|
H2C |
|
COOH |
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
HO |
|
|
|
C |
|
|
COOH |
|
|
|
|
|
HC |
|
COOH |
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
H2C |
|
|
COOH |
|
HO |
|
CH |
|
COOH |
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
лимонная, цитрат |
изолимонная, изоцитрат |
O |
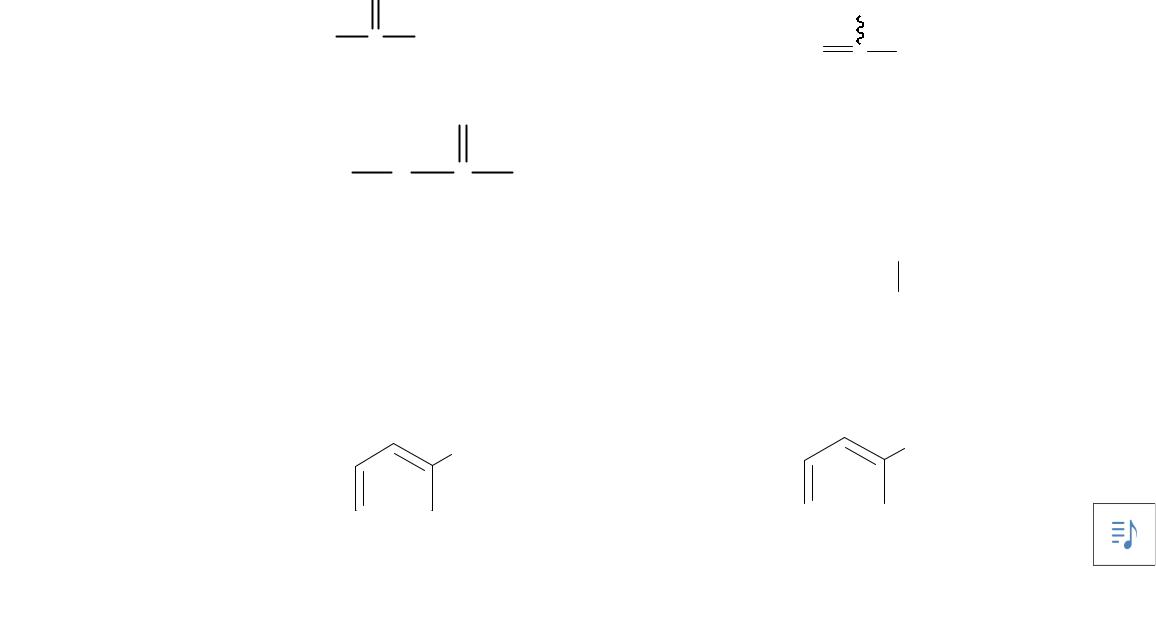
Оксокислоты: |
OPO3H2 |
|
||
|
|
|
H3C C COOH |
|
H2C C COOH |
|
|
|
пировиноградная (ПВК), пируват |
фосфоенолпируват (ФЕП) |
|
O
H2
HOOC C C COOH
|
|
|
|
|
|
O |
|
|
||
|
|
H2 |
H2 |
|
|
|
|
|
||
HOOC |
|
C |
|
C |
|
C |
|
COOH |
||
|
|
|
|
|||||||
щавелевоуксусная (ЩУК), оксалоацетат α-кетоглутаровая (α -КГ), α-кетоглутарат
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
H2 |
|
|
C |
|
O |
||||
|
|
|
|
|
|
|
|
|
|||||||
H3C |
|
C |
|
COOH |
|
||||||||||
|
|
C |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|||||||||||
β-оксомасляная (ацетоуксусная), ацетоацетат |
глиоксиловая, глиоксилат |
||||||||||||||
Ароматические кислоты:
CO |
C |
бензойная, бензоат |
никотиновая, никотинат |

СТРОЕНИЕ КАРБОКСИЛЬНОЙ ГРУППЫ
Карбоксильная (-СООН) и карбоксилатная (-СОО-) группы полярные, электроноакцепторные (- I, - M) сопряженные функциональные группы.
|
1/2 - |
C |
O |
|
C |
O |
+ |
|
+ H |
||||
|
|
|
|
|
|
|
|
|
1/2 - |
|
|
|
|
|
O |
|
|
|
O H |
состояниях |
|
||
В жидком и твердом |
молекулы RCOOH |
||||
ассоциированы |
димеризацией |
– |
образованием |
||
межмолекулярных водородных связей между двумя группами –СООН.
Наличие ОН в структуре –СООН уменьшает склонность карбоновых кислот к реакциям AN (характерным для
карбонильных соединений) и SN (они протекают in vitro только в сильнокислой среде).
Наличие карбонильной группы в структуре –СООН усиливает ОН-кислотность:
RCOOH – более сильные кислоты, чем вода, спирты ROH и угольная кислота H2CO3
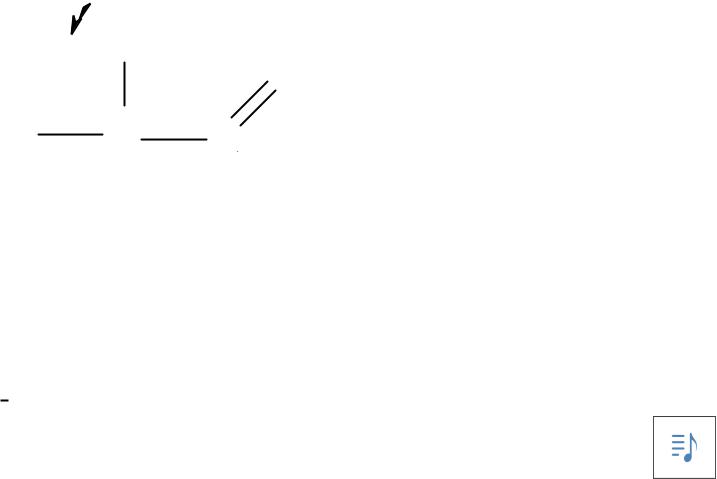
ОБЩИЕ ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ
В молекуле имеется 4 типа реакционных центров:
|
|
|
|
|
|
C |
CH |
|
|
|
|
|
|
|
OH-группа обладает заметной кислотностью (образует соли с различными основаниями и активными металлами)
карбонильная группа (реакции SN, образование и взаимопревращения производных)
α-С-Н группа обладает слабой кислотностью (галогенирование, окисление, конденсации, карбокси- лирование in vivo)
карбоксильная группа как целое (декарбоксилирование дикарбоновых и некоторых оксокислот)

КАЧЕСТВЕННЫЕ РЕАКЦИИ КАРБОНОВЫХ КИСЛОТ
-все растворимые кислоты реагируют с водным NaHCO3: RCOOH + NaHCO3 → RCOO-Na+ + CO2 ↑ + H2O
-щавелевая кислота осаждается ионами кальция, оксалат кальция СаС2О4 растворяется в сильных кислотах
-ряд гидрокси- и оксокислот (молочная, пировиноградная)
образуют окрашенные комплексы с солями железа (III)
