
Лекция 14 гидроксикислоты
Схема лекции.
1. Классификация, номенклатура, изомерия.
2. Способы получения
3. Химические свойства
4. Оптическая изомерия
Гидроксикислотами называются карбоновые кислоты, содержащие наряду с карбоксильной группой одну или несколько гидроксильных групп. По числу гидроксильных групп, включая входящую в карбоксильную группу, определяют атомность гидроксикислот. По числу карбоксильных групп определяют основность гидроксикислоты.
1.Классификация, номенклатура, изомерия.
Большинство гидроксикислот имеют тривиальные названия, сложившиеся исторически по их природному источнику. Например: молочная кислота, яблочная, виноградная, лимонная и т.д. Рациональная номенклатура строится по тривиальному названию карбоновой кислоты в префиксе ставится «гидрокси» и буквой греческого алфавита обозначается положение гидроксигруппы. По систематической номенклатуре локантом обозначается положение гидроксигруппы. Карбоксильная группа всегда занимает первое положение. Название строится по углеводороду с добавкой суффиксов «овая» или «диовая».
Гомологический ряд одноосновных гидроксикислот начинается с гидроксимуравьиной или угольной кислоты. Затем идет гликолевая или гидроксиуксусная, Эти две кислоты не имеют структурных изомеров. Следующий гомолог может существовать в виде двух изомеров, различающихся положением гидроксильной группы: это молочная или α-гидроксипропионовая и β-гидроксипропионовая кислота. Кислота с четерьмя углеродными атомами может существовать в виде пяти изомеров. Три соответствуют н-масляной кислоте и два изомасляной кислоте.
Однако наиболее распространенной формой изомерии для гидроксикислот является оптическая изомерия, что и рассматривается на примере гидроксикислот.

2. Способы получения
Гидроксикислоты получают либо из карбоновых кислот введением гидроксильной группы, либо из спиртов введением карбоксильной группы.
2.1. Получение α-гидроксикислот
α-хлор или бром карбоновые кислоты, получаемые по реакции Гелля-Форльгарда-Зелинского, легко превращаются в α-гидроксикислоты при нагревании в воде:
![]()
Другим распространенным путем получения является омыление циангидринов или гидроксинитрилов:
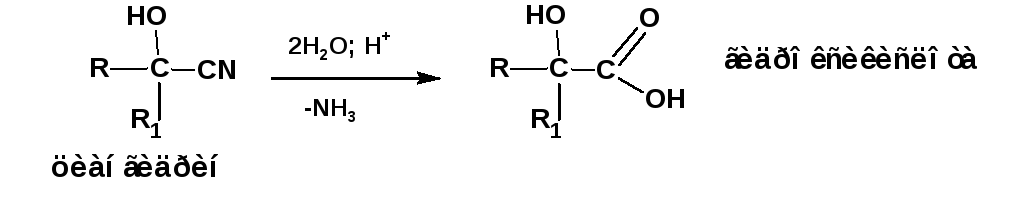
2.2. Получение β-гидроксикислот
Присоединением воды к α,β-ненасыщенным кислотам получают β-гидроксикислоты:

Общим способом получения β-гидроксикислот является реакция Реформатского:

2.3. Получение γ-гидроксикислот
γ-Гидроксикислоты получаются при гидролизе циклических сложных эфиров так называемых лактонов. Сами лактоны получаются при восстановлении циклических ангидридов:

3. Химические свойства
Гидроксикислоты – жидкости или большей частью кристаллические вещества. В воде растворимы лучше, чем соотвествующие карбоновые кислоты. Низшие гидроксикислоты смешиваются с водой в любых отношениях.
3.1. Общие свойства гидрокислот
Гидроксикислоты проявляют свойства спиртов и кислот. Как кислоты они образуют соли, сложные эфиры, амиды:

Как спирты гидроксикислоты образуют алкоголяты, простые эфиры, могут замещать гидроксил на галоген:

По сравнению с карбоновыми кислотами, гидроксикислоты являются более сильными кислотами, осообенно если гидроксигруппа расположена в α-положении.
3.2 Специфические свойства α-гидрокислот
α-Гидрокислоты легко восстанавливаются в карбоновые кислоты йодистым водородом:

При кипячении с разбавленными минеральными кислотами происходит расщепление с выделением муравьиной кислоты:

При нагревании α-гидрокислот происходит отщепление двух молекул воды от двух молекул гидроксикислоты с образованием сложного эфира циклического строения, так называемого лактида:

3.3. Специфические свойства β-гидрокислот
При нагревании β--гидрокислот происходит отщепление одной молекулы воды от одной молекулы гидроксикислоты с образованием α,β-ненасыщенной карбоновой кислоты:

3.4. Специфические свойства γ- и δ -гидрокислот
При нагревании γ- и δ-гидрокислот происходит внутримолекулярная реакция этерификации, сопровождающаяся отщеплением одной молекулы воды и образованием циклического эфира - лактона:

