
Т06-раздаточный материал тема 6 (углеводы)
.doc

МОНОСАХАРИДЫ
Строение
Моносахариды представляют собой полигидроксиальдегиды и полигидроксикетоны, которые называются соответственно альдозами и кетозами.
Все альдозы дают характерные реакции на альдегиды.
По числу атомов углерода в молекуле (обычно оно равно числу атомов кислорода), среди моносахаридов различают триозы, тетрозы, пентозы, гексозы, гептозы и т. д. К этим названиям при построении названий моносахаридов присоединяют функциональную приставку (альдо- или кето-), например:

Все моносахариды оптически активны, поскольку в их молекулах имеются асимметрические атомы углерода. Число асимметричных атомов углерода в моносахариде растет по мере удлинения цепи. В зависимости от того, где расположена группа —ОН y предпоследнего атома С в углеродной цепи, изомерные углеводы будут D -в L-соединениями:
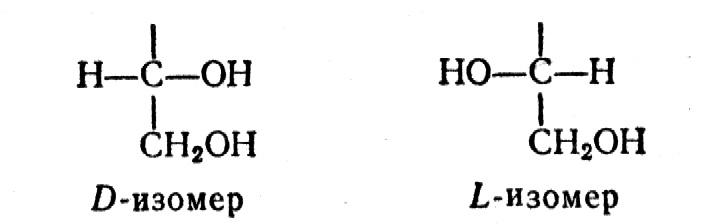
Моносахариды существуют в открытой (ациклической) и закрытой (циклической) таутомерных формах. Поэтому структурные формулы сахаридов изображают двояко:

Углеводы с шестичленными циклами называются пиранозами, а углеводы с пятичленными циклами — фуранозами (от наименования соответствующих гетероциклических систем — пиран и фуран).
Примеры циклических пространственных формул моносахаридов:

Гидроксил, образующийся в результате циклизации, называется полуацетальным. Полуацетальный гидроксил резко отличается по свойствам от других гидроксильных групп молекулы. Он легко может замещаться на другие нуклеофильные группировки, в результате чего образуются различные производные сахаров.

Расположение группы ОН выше или ниже плоскости цикла у атома С в положении (1) влияет на физические свойства изомеров (растворимость, температура плавления, оптическое вращение).

Следует обратить внимание на то, что - и - глюкозы – это не оптические антиподы, а диастереоизомеры, т, е. пространственные изомеры, отличающиеся конфигурационным окружением хирального атома углерода (в данном случае — пространственным расположением группы ОН и атома Н).
Наиболее важными моносахаридами являются пентозы и гексозы.
Пентозы
Моносахариды с пятью атомами углерода и пятью атомами кислорода не встречаются в природе в свободном виде, но являются важными составными частями олиго- и полисахаридов, содержащихся, например, в древесине. Примеры известных альдопентоз:

L-Арабиноза входит в состав вишневого клея и свеклы, а D-арабиноза является компонентом сока алоэ. D-Ксилоза может быть выделена из отрубей, древесины, соломы, шелухи подсолнечниковых семечек; D-рибоза входит в состав природных нуклеиновых кислот.
Гексозы
Моносахариды с шестью атомами углерода, несущими атомы кислорода, встречаются в природе в свободном виде и входят в состав природных олиго- и полисахаридов. Кроме того, они образуют гликозиды — продукты конденсации со спиртами, тиолами и аминами.
Примеры распространенных альдо- и кетогексоз:

D-Глюкоза (виноградный сахар, декстроза) — наиболее известная из альдогексоз. В свободном виде этот моносахарид содержится во многих сладких фруктах (виноград и др.) и в меде, а также в крови животных и человека; в связанном виде глюкоза имеется в сахарозе, мальтозе, лактозе, целлюлозе, крахмале и других ди- и полисахаридах. Представляет собой белое кристаллическое вещество, хорошо растворимое в воде и легко образующее пересыщенный раствор. D -Глюкоза—главный источник энергии для большинства живых организмов.
D-Маиноза содержится в скорлупе некоторых орехов и в кожуре апельсинов, является структурным фрагментом определенных полисахаридов — маннанов.
D-Галактоза в связанном виде находится в молочном сахаре (лактозе), гидролизом которого ее можно получить.
D-Фруктоза (плодовый, или фруктовый, сахар, левулоза) является кетогексозой. В свободном виде она содержится во многих спелых фруктах и в меде, а в связанном виде — в дисахаридах и полисахаридах, например соответственно в сахарозе, и инулине. Инулин включает только остатки фруктозы, обладает крахмалоподобными свойствами и содержится в клубнях георгина и цикория, а также в некоторых водорослях. Инулин используется для получения фруктозы.
D-Фруктоза представляет собой белые кристаллы, очень сладкие на вкус (в 1,5 раза слаще сахарозы). Фруктоза проявляет восстановительные свойства по отношению к фелинговой жидкости, хотя содержит только кетонную функциональную группу, это объясняется явлением кето-енольной таутомерии.
ДИСАХАРИДЫ
Дисахариды (простейшие олигосахарнды) образуются при конденсации двух молекул моносахаридов с отщеплением воды, например:
С6Н12О6 + С6Н12О6 —> C12H22O12+Н2О
Связывание молекул моносахаридов происходит через полуацетальный гидроксил одной молекулы и любой (в том числе и полуацетальный) гидроксил другой молекулы. Образующуюся связь называют гликозидной. Если в образовании связи принимают участие два полуацетальных гидроксила, образуются такие дисахариды, как тростниковый сахар, лишенные восстановительных свойств (невосстанавливающие дисахариды), в другом случае случае — такие дисахариды, как молочный сахар, проявляющие восстановительные свойства по отношению к фелинговой жидкости и др. (восстанавливающие дисахариды).
Наиболее известными представителями дисахаридов являются сахароза, лактоза и мальтоза.
Сахароза (тростниковый сахар, свекловичный сахар) содержит остатки α-D-глюкозы и β-D-фруктозы:

Сахароза — невосстанавливающий дисахарид, поскольку в образовании ее гликозидной связи участвует карбонильная группа фруктозы. При гидролитическом расщеплении гликозидной связи под действием кислотной среды или ферментов (процесс инверсии) сахароза превращается в моносахариды, обладающие восстановительными свойствами.
Получающаяся смесь называется инвертным сахаром.
Лактоза (молочный сахар) включает остатки -D-галактозы и -D-глюкозы:

В положении (1) остатка D-глюкозы имеется свободная полуацетальная группа ОН, поэтому лактоза может переходить в альдегидную форму:

Следовательно, лактоза, как и всякий другой альдегид, способна восстанавливать фелингову жидкость, т. е. она является восстанавливающим дисахаридом. Поэтому же атом С в положении (1) остатка глюкозы в молочном сахаре не присоединяет других молекул моносахаридов.
Лактоза значительно (в 4—5 раз) менее сладкая, чем сахароза. В коровьем молоке содержится 4—5 % лактозы, а в женском молоке — 5,5—7,5 %. При скисании молока весь молочный сахар под действием бактерий переходит в молочную кислоту.
Мальтоза (солодовый сахар) представляет собой соединение двух остатков -D-глюкозы:

Мальтоза получается при неполном ферментативном гидролизе крахмала, содержащегося в солоде, т. е. в проросших ячменных зернах. Как и лактоза, мальтоза восстанавливает фелингову жидкость.
ПОЛИСАХАРИДЫ
К важнейшим полисахаридам относятся крахмал, гликоген и целлюлоза, состоящие из остатков глюкозы, инулин, состоящий из остатков фруктозы, и гемицеллюлозы, включающие остатки различных моносахаридов.
Крахмал — белый аморфный продукт конденсации -D-глюкозы. Он представляет собой не однородное вещество, а смесь, состоящую из амилопектина (80 %) и амилозы (20 %).


Амилопектин — это полисахарид, имеющий многократно разветвленные цепи глюкозных остатков; степень полимеризации составляет 1000—6000. Он не растворим в воде, но сильно набухает в ней. Амилоза состоит из неразветвленных (линейных) цепей глюкозных остатков; степень полимеризации находится в пределах 100—1400. Амилоза растворима в воде, но образующиеся растворы нестойки, и через непродолжительное время амилоза выпадает в виде кристаллического осадка.
Гликоген (животный крахмал) имеет тот же состав, что и крахмал растений; по строению подобен амилопектину (25000 — 90000 глюкозных остатков). Гидролизуется аналогично крахмалу. Гликоген содержится во всех клетках живого организма, наиболее богаты им печень и мышцы.
Целлюлоза (клетчатка) — наиболее распространенный в природе полисахарид и вообще органическое вещество. Молекулы целлюлозы построены из остатков -D-глюкозы; степень полимеризации достигает 10000 — 14000. Целлюлоза относительно трудно подвергается гидролизу, и только в жестких условиях (40 %-ая хлороводородная кислота, 105 — 180 °С) происходит ее расщепление через стадию образования дисахарида — целлобиозы — до глюкозы:
Целлюлоза — > Целлобиоза — > Глюкоза
Целлюлозе, как всякому спирту, свойственны реакции этерификации. В промышленном масштабе проводится нитрование (с азотной кислотой) и ацетилирование (с уксусной кислотой) целлюлозы.
Древесина состоит из целлюлозы (около 45%), гемицеллюлоз (около 30%) и лигнина (около 20%), а также примесей смол и неорганических веществ. Лигнин— это сложное макромолекулярное ароматическое вещество, образуется как побочный продукт в производстве целлюлозы. После сложной химической обработки древесины все спутники целлюлозы становятся водорастворимыми, а сама целлюлоза как химически стойкое вещество остается в виде очищенного технического продукта, в котором содержание целлюлозы может достигать 99 % и выше.
