
- •Органическая химия
- •Состав органических веществ, их многообразие. Место органической химии в системе естественных наук. Источники органических соединений.
- •Формирование и основные положения теории строения органических соединений (а.М. Бутлеров, а. Кекуле, а. Купер).
- •Основные признаки классификации органических веществ. Основные классы органических веществ.
- •Номенклатура органических соединений. Основные принципы построения названий органических соединений.
- •Типы связей в молекулах органических соединений. Σ- и π-связи. Гибридизация, понятие о молекулярных орбиталях.
- •Представление о механизмах реакций. Представление о промежуточных частицах: радикалы, карбокатионы, карбанионы. Классификация реагентов: радикалы, нуклеофилы, электрофилы.
- •Энергетический профиль реакции; энергетический барьер реакции, энергия активации, энергия переходного состояния, тепловой эффект реакции. Кинетический и термодинамический контроль.
- •Кислоты и основания (Бренстед, Льюис). Сопряженные кислоты и основания. Кислотно-основые равновесия. Константа кислотной ионизации и ее показатель (рКа).
- •Взаимное влияние атомов в молекулах, ионах, радикалах. Электронные и пространственные эффекты в органических реакциях (индуктивный эффект, эффект поля, мезомерный эффект, гиперконьюгация).
- •Гомологический ряд, номенклатура, электронное строение, sp3-гибридизация и физические свойства алканов.
- •Химические свойства алканов. Общие представления о механизме цепных радикальных реакций замещения в алканах (на примере реакции галогенирования).
- •Номенклатура, структурная и пространственная изомерия, электронное строение, sp2-гибридизация и физические свойства алкенов.
- •Химические свойства алкенов: каталитическое гидрирование, реакции электрофильного присоединения к двойной связи алкенов, их механизмы.
- •Химические свойства алкенов: реакции присоединения галогенов, галогеноводородов, воды. Правило Марковникова и его объяснение.
- •Представление о стереохимии присоединения галогенов у алкенов. Перегруппировки карбокатионов. Реакции радикального присоединения (по Харашу).
- •Окислительное расщепление алкенов (восстановительный и окислительный озонолиз). Гидроборирование алкенов и использование в синтезе спиртов.
- •Полимеризация алкенов как важнейший метод получения высокомолекулярных соединений. Полиэтилен, полипропилен. Понятие о стереорегулярных полимерах.
- •Аллильное хлорирование алкенов, механизм. Аллильный радикал. Окисление алкенов кислородом воздуха (пероксидное окисление).
- •Номенклатура, классификация, изомерия диеновых углеводородов.
- •Классификация диенов:
- •Изопреновое звено в природных соединениях. Понятие об изопреноидах. Каучук. Синтетические каучуки.
- •Номенклатура, электронное строение, sp-гибридизация и физические свойства алкинов.
- •Химические свойства алкинов: каталитическое гидрирование и восстановление натрием в жидком аммиаке, использование в синтезе (z)- и (e)-алкенов.
- •Химические свойства алкинов: реакции электрофильного присоединения к тройной связи – галогенирование, гидрогалогенирование, гидратация (реакция Кучерова).
- •Кислотность ацетилена и терминальных алкинов. Димеризация, тримеризация ацетилена. Полиацетилен.
- •Классификация, номенклатура, структурная изомерия и пространственное строение циклоалканов.
- •Классификация и номенклатура аренов. Природа связей в молекуле бензола. Конденсированные ароматические углеводороды: нафталин, антрацен, фенантрен, бензпирен.
- •Ароматичность, критерии ароматичности. Правило Хюккеля.
- •Влияние заместителей в бензольном кольце на изомерный состав продуктов и скорость реакции. Активирующие и дезактивирующие заместители. Орто-, пара- и мета-ориентанты.
- •Классификация, номенклатура, изомерия галогенуглеводородов.
- •Литий- и магнийорганические соединения и их использование в органическом синтезе.
- •Биологическое действие галогенпроизводных, их применение в народном хозяйстве. Хлороформ, иодоформ, перфторуглеводороды, перфторполиэтилен (тефлон). Инсектициды.
- •Одноатомные спирты. Номенклатура, изомерия. Электронное строение. Физические свойства спиртов, роль водородной связи.
- •Химические свойства спиртов: кислотно-основные свойства. Алкоголяты металлов, их основные и нуклеофильные свойства.
- •Реакции нуклеофильного замещения с участием спиртов. Биологически важные реакции нуклеофильного замещения с участием эфиров фосфорных кислот.
- •Внутри- и межмолекулярная дегидратация спиртов (образование алкенов и простых эфиров). Окисление первичных и вторичных спиртов.
- •Фенолы. Номенклатура и изомерия. Простейшие представители: фенол, крезолы, пирокатехин, резорцин, гидрохинон, флороглюцин, пирогаллол. Электронное строение фенола. Кислотность фенолов.
- •Образование простых и сложных эфиров фенолов. Реакции электрофильного замещения в ряду фенолов (галогенирование, сульфирование, нитрование, алкилирование).
- •Карбоксилирование фенолятов щелочных металлов (реакция Кольбе). Окисление фенолов.
- •Хиноны и их биологическая роль. Фенольные соединения в природе. Витамин е. Флавоноиды.
- •Простые эфиры. Номенклатура, классификация. Расщепление кислотами. Образование гидропероксидов, их обнаружение и разложение. Циклические простые эфиры. Тетрагидрофуран. 1,4-Диоксан.
Химические свойства алкинов: каталитическое гидрирование и восстановление натрием в жидком аммиаке, использование в синтезе (z)- и (e)-алкенов.
Восстановление алкинов. Алкины в присутствии катализаторов Pd, Pt или Ni восстанавливаются с образованием алканов. Процесс гидрирования осуществляется ступенчато:
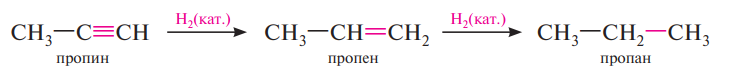
Сначала образуется цис-изомер:
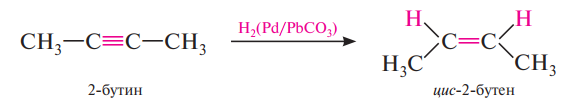
При восстановлении алкинов с помощью натрия в жидком аммиаке водород также присоединяется селективно, но с образованием транс-изомера:

Химические свойства алкинов: реакции электрофильного присоединения к тройной связи – галогенирование, гидрогалогенирование, гидратация (реакция Кучерова).
В реакцию галогенирования может вступать одна или две молекулы галогена. В результате присоединения одной молекулы галогена образуется преимущественно транс-дигалогеналкен. Присоединение второй молекулы галогена идет труднее. При этом образуется тетразамещенный алкан и наблюдается обесцвечивание характерной окраски брома (качественная реакция на кратную связь).

Гидрогалогенирование
Алкины могут присоединять одну или две молекулы галогеноводорода (НСl, НВr) с образованием моногалогенозамещенных алкенов или геминальных дигалогеналканов (оба атома галогена находятся при одном атоме углерода). Присоединение протекает в соответствии с правилом Марковникова:
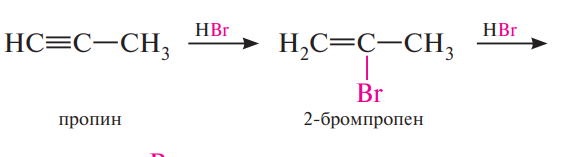
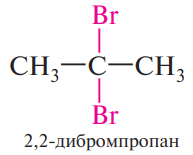
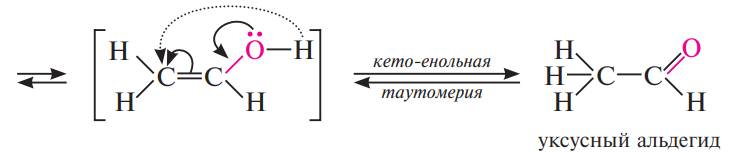
Гидратация (реакция Кучерова). Алкины в присутствии катализатора — солей ртути (II) взаимодействуют с водой. Присоединение происходит в соответствии с правилом Марковникова. В результате гидратации ацетилена образуется уксусный альдегид, гомологи образуют кетоны.
Гидратация алкинов протекает через стадию образования енолов — гидроксипроизводных углеводородов, содержащих гидроксильную группу у атома углерода с двойной связью. Такие соединения являются неустойчивыми. В процессе образования они изомеризуются в более стабильные карбонильные соединения — альдегиды или кетоны. Эта закономерность была установлена в 1877 году русским химиком А. П. Эльтековым и получила название «правило Эльтекова»
![]()
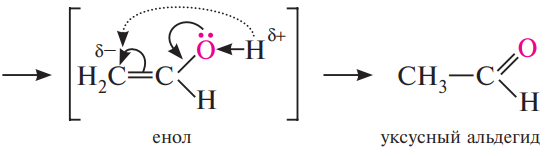
![]()

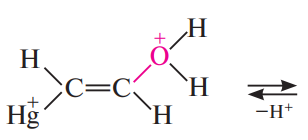
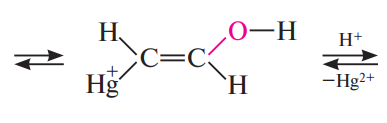
Механизм:
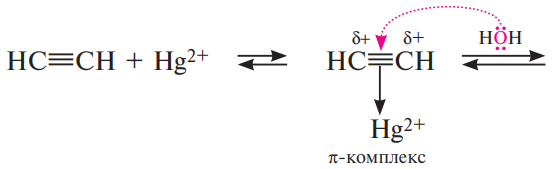
Кислотность ацетилена и терминальных алкинов. Димеризация, тримеризация ацетилена. Полиацетилен.
Терминальные алкины проявляют свойства очень слабых кислот: водород при концевой тройной связи может замещаться на металл. В результате реакции образуются соли алкинов: ацетилениды, т.е. реагируют с натрия амидом NаNН2 в жидком аммиаке, аммиачным раствором серебра оксида Аg2O и меди (I) хлорида СuCl.
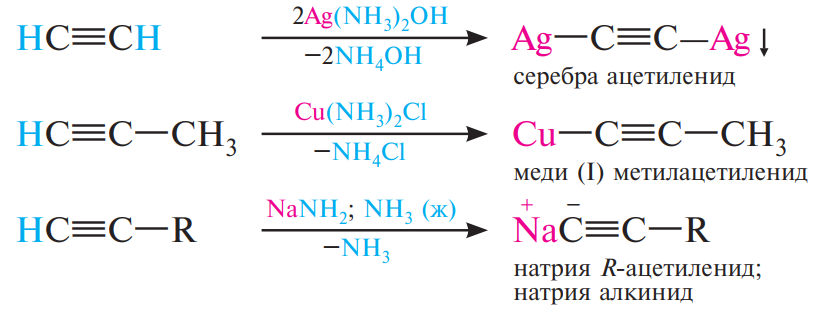
Алкиниды серебра представляют собой осадки белого цвета, а меди (I) — осадки красно-бурого цвета. Реакции терминальных алкинов с растворами аммиакатов серебра и меди (I) является качественной на концевую тройную связь.
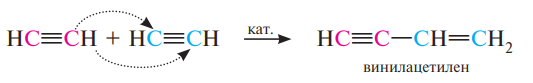
Ацетилен в присутствии меди (I) хлорида и аммония хлорида димеризуется с образованием винилацетилена (промежуточный элемент при производстве синтетических каучуков):
Ацетилен и его гомологи подвергаются циклотримеризации. При нагревании ацетилена в присутствии активированного угля образуется бензол.

Полиацетилен [–CH≡CH–] — органическое вещество, полимер ацетилена. Известны цис- и транс-формы полиацетилена. При нагревании цис-изомера до 100-150 °C, совершается переход в транс-форму. В зависимости от способа получения полиацетилен может представлять собой чёрный порошок, сероватый пористый материал, серебристые или золотистые плёнки. Не растворим ни в одном из известных органических растворителей.
