
ИДЗ / ИРС_2
.docxМИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
федеральное государственное автономное образовательное учреждение
высшего образования
«НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ
ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»

Инженерная школа новых производственных технологий
Обеспечивающее подразделение: Отделение материаловедения
Направление подготовки: 12.03.02 Оптотехника
ООП: Оптико-электронные приборы и системы
ИНДИВИДУАЛЬНАЯ РАБОТА СТУДЕНТА №2
дисциплина "Физические основы источников излучения"
Вариант 12
Выполнила:
студентка группы _________________
Проверил:
доктор ф-м.н., профессор ОМ ИШНПТ _________________ В.Ф. Штанько
Томск – 2023
Вариант 12 - As+3
Задание 1. Рассмотреть и построить качественную схему термов атома (иона) с двумя валентными электронами при возбуждении одного электрона (для трёх возбуждённых состояний)
Порядковый номер N в периодической системе равен 33. Т.к он ионизован трижды, то сумма электронов равна 30.
Заполнение
электронных состояний происходит в
следующем порядке, в соответствии с
правилом Клечковского:
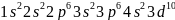 .
.
Возбуждать будем один электрон.
Для основного состояния (s- состояние):
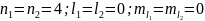 .
.
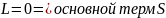 ;
;
Спин-орбитальное взаимодействие отсутствует и терм не расщеплён.
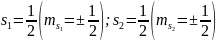 ;
;
По принципу запрета
Паули, в атоме не может быть электронов
с одинаковым набором квантовых чисел
=>
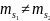
Значит
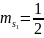 и
и
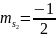
Соответственно
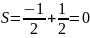 ;
;
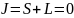 ;
;
Мультиплетность:
 ;
;
Терм основного состояния: 1S0.
Для первого возбуждённого состояния (p-состояние):
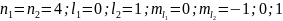 .
.
 ;
;
 ;
;
В данном случае,
электроны имеют различные орбитальные
числа, соответственно, возможно,

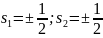 ;
;
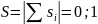 ;
;
При S=0:
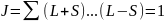 ;
;
Мультиплетность: 2S+1=1.
При S=1:
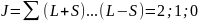 ;
;
Мультиплетность: 2S+1=3.
Термы первого возбуждённого состояния: 1P1; 3P0; 3P1; 3P2.
Для второго возбуждённого состояния (d-состояния):
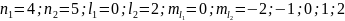 .
.
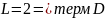 ;
;
;
В данном случае, электроны имеют различные орбитальные числа, соответственно, возможно,
;
.
При S=0:
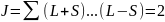 ;
;
Мультиплетность: 2S+1=1.
При S=1:
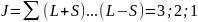 ;
;
Мультиплетность: 2S+1=3.
Термы второго возбуждённого состояния: 1D2; 3D1; 3D2; 3D3.
Для третьего возбуждённого состояния (f-состояния):
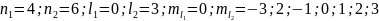 .
.
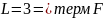 ;
;
;
В данном случае, электроны имеют различные орбитальные числа, соответственно, возможно,
;
.
При S=0:
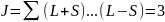 ;
;
Мультиплетность: 2S+1=1.
При S=1:
 2;
2;
Мультиплетность: 2S+1=3.
Термы третьего возбуждённого состояния: 1F3; 3F2; 3F3; 3F4.
Задание 2. Определить величины орбитальных, собственных и полных механических и магнитных моментов для основного и двух возбуждённых состояний.
Возможные численные
значения механических моментов
 ,
, и
и
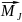 определяются через квантовые числа
L, S и J следующим образом:
определяются через квантовые числа
L, S и J следующим образом:
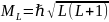 ;
;
 ;
;
 .
.
Магнитные моменты связаны с механическими следующими соотношениями:
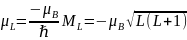 ;
;
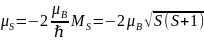 ;
;
 .
.
где
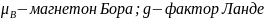 .
.
Для основного состояния:
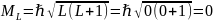 ;
;
 ;
;
 .
.
Соответственно
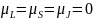 .
.
Для первого возбуждённого состояния:
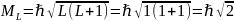 ;
;
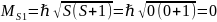 ;
;
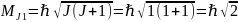 .
.
В отсутствии
собственного момента, полный механический
момент будет равен орбитальному, для
каждой ориентации орбитального момента
(кроме состояния с ℓ = 0) будет одна
ориентация полного механического
момента величиной
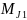 :
:
 ;
;
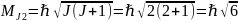 ;
;
 ;
;
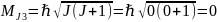 .
.
Найдём величины магнитных моментов:
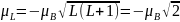 ;
;
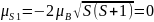 ;
;
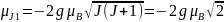 ;
;
 ;
;
 ;
;
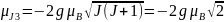 ;
;
 .
.
Величины механических моментов для второго возбуждённого состояния:
 ;
;
;
 ;
;
;
 ;
;
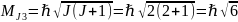 ;
;
 .
.
Найдём величины магнитных моментов:
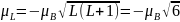 ;
;
;
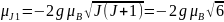 ;
;
;
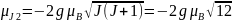 ;
;
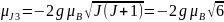 ;
;
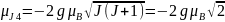 .
.
Задание 3. Определить и построить оптические переходы для основных серий спектра.

Рисунок 1. Схема термов и основные серии для иона As+3
О
- синглетная серия
(n = 4,5,6...)
сновные серии спектра: 4 1S0 - n
1P1
4 1S0 - n
1P1
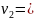 4 1P1
- n 1S0
4 1P1
- n 1S0

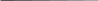 4 1P1
- n 1D2
4 1P1
- n 1D2
-главная серия
5 3S1 - n 3P05 3S1 - n 3P1
5 3S1 - n 3P2
- 2я побочная серия
5 3P0 - n 3S15 3P1 - n 3S1
5 3P2 - n 3S1
- 1я побочная серия
5 3P0 - n 3D15 3P1 - n 3D1
5 3P2 - n 3D1
 5 3P1
- n 3D2
5 3P1
- n 3D2
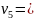 5 3P2
- n 3D2
5 3P2
- n 3D2
 5 3P2
- n 3D3
5 3P2
- n 3D3
Для главной серии 3S1 терм является постоянным, а 3Р012 переменным. Отношение интенсивностей компонентов триплета главной серии определяется как отношение статистических весов состояний. По мере увеличения n2 расщепление переменного 3Р012 терма уменьшается, а, следовательно, уменьшаются интервалы между линиями в каждой последующей тройке линий. [1]
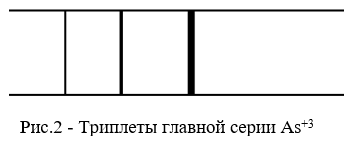
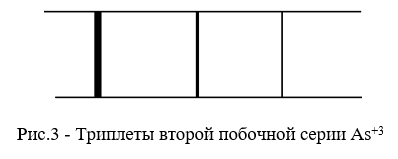
Во второй побочной серии частотные интервалы между линиями в триплетах одинаковы. Постоянным является 3Р012 терм, а 3S1 переменным. Серия состоит из повторяющихся троек линий, причём интервалы частот между линиями в каждой последующей тройке сохраняются.[1]
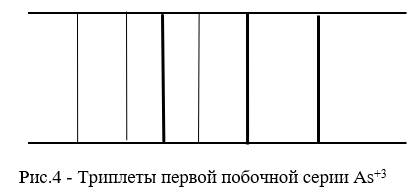
В 1й побочной серии наиболее яркими являются три линии: 33P2-n3D3, 33P1-n3D2 и 33P0-n3D1. Так как обычно разности между термами 3DJ много меньше, чем между термами 3PJ, то остальные линии выглядят слабыми около трех основных. Разности между частотами линий, стоящих в одном столбце в группах, совпадают с разностями между термами 33P1-33P2 и 33P0-33P1. Также разности частот линий, стоящих в одной строке, совпадают с разностями n3D2-n3D3 и n3D1-n3D2. [1]
СПИСОК ЛИТЕРАТУРЫ
Штанько В.Ф. Введение в атомную и молекулярную спектроскопию. - Томск: Изд-во Томского Политехнического университета, 2008.-164 с. - ISBN 5-98298-357-8.
