
6 курс / Гастроэнтерология / Острый_панкреатит_Савельев_В_С_,_Буянов_В_М_,_Огнев_Ю_В_
.pdfсиндрома, который сопровождается поражением легких, сердца и сосудов, печени, почек и надпочечников, расстройствами психики
[Чаплинский В. В., Гнатышак А. И., 1972; Bernard, 1963].
Трипсинемия обусловливает развитие коллапса и шока при остром панкреатите [Маждраков Г. М., 1961; Weil, Schubin, 1967]. Мы указывали, что представления о «всепричинной» роли трипсина были поколеблены негативными результатами экспериментальных и клинических исследований. Таким образом, вопрос о сущности и причинной роли панкреатогенной токсемии при остром панкреатите еще не решен, что тормозит прогресс лечебной тактики.
РАЗВИТИЕ МЕТОДОВ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ОСТРОГО ПАНКРЕАТИТА
Труднодоступность поджелудочной железы для клинического исследования обусловливает трудности диагностики острого панкреатита. По данным Б. Л. Осповата и А. И. Копылкова, диагноз направления был правильным лишь у 36,9% больных острым панкреатитом, поступивших в приемное отделение Больницы им. С. П. Боткина. Сложность дифференциальной диагностики острого панкреатита отмечена многими авторами [Осипов Б. К. и др., 1970; Бунин К. В. и др., 1973; Маят В. С. и др., 1978, и др.]. Тем не менее накопленный опыт клинической [Шелагуров А. А., 1967; Глускина В.
М., 1972; Gulzow et al., 1972, и др.], общелабораторной [Мурашева 3. М., Новосельцев А. Е., 1978; Murphy et al., 1977] и отчасти рентгенологической [Акжигитов Г. Н., 1974; Stein et al., 1959] диагностики позволяет в типичных случаях (чаще легких по течению) своевременно распознать острый панкреатит. Тяжелые, или, как принято их называть, деструктивные, формы острого панкреатита представляют собой наиболее трудную диагностическую задачу. Лишь «плюривисцеральность» клиники [Carey, 1979] и тяжесть течения заболевания позволяют в ряде случаев заподозрить панкреонекроз. Так, по данным Peterson и Brooks (1979), только 57% больным, умершим от острого панкреатита, диагноз был поставлен прижизненно.
Многие годы разработка методов диагностики острого панкреатита шла преимущественно в направлении изучения диагностической ценности ферментных и других биохимических тестов [Durr et al., 1981].
Методы специфической ферментной диагностики острого панкреатита не разработаны. Внимание клиницистов издавна привлекают три наиболее изученных фермента: а-амилаза, липаза и трипсин.
Повышение их активности в крови и моче большинство авторов связывают с острым панкреатитом [Шабанов А. Н. и др., 1967; Левицкий А. П. и др., 1970; Шпектор В. А., Ша-терников В. А., 1972; Ammann, 1969; Gulzow et al., 1972; Tenhunen, 1972; Wettendorf, 1974, и др.].
Амилаземия и амилазурия с момента внедрения в клиническую практику метода Вольгемута [Wohlgemuth, 1907, 1908] считаются классическими ранними тестами, подтверждающими дяагноз острого панкреатита. В то же время повышение амило-литической активности крови и мочи было выявлено и при других заболевания» органов брюшной полости [Ammann, 1969; Shebel et al., 1970; Tenhunen, 1972; Lankisch et al., 1977], например при мезентериальном тромбозе.
В последние годы внимание привлекает липолитическая группа ферментов поджелудочной железы, среди которых основное значение в ранней диагностике острого панкреатита придают липазе [Левицкий А. П. и др., 1970; Ticktin et al., 1965; Song et al., 1970; Lifton, 1974].
По мнению Schwokowski и Poge (1979), липолитическая активность— наиболее специфический диагностический тест острого панкреатита. Роль определения активности протеолитических ферментов поджелудочной железы, в частности трипсина, в диагностике острого панкреатита не выяснена. Имеются чисто методологические трудности, мешающие широкому внедрению этих тестов в клиническую практику. Существует также мнение о том, что активное связывание этих ферментов ингибиторными системами крови, а также их участие в ряде физиологических механизмов (свертывание, кининообразование) не позволяют получить достаточно достоверные сведения о системе протеолиза [Веремеенко К. Н., 1964, 1971, 1975; Markwardt, 1967; Ammann, 1969].
Из неспецифических методов биохимической диагностики острого панкреатита наибольший интерес представляет определение в сыворотке крови трансамидиназы [Карелин А. А., Беляев А. А., 1978], метгемальбумина [Borda et al., 1980] и геминовых соединений [Глускина В. М., 1972; Постолов П. М., 1973]. Эти тесты неспецифичны, но позволяют судить о развитии некротической (трансамидиназа) и геморрагической (метгемальбумин, геминовые соединения) фаз острого панкреатита.
Предложены и другие тесты: определение уровня кальция в крови [Souza, Floch, 1973], различных показателей свертывающей системы крови [Крючок А. Г., 1970; Аскерханов Р. П., Абдуллаев М. А., 1973; Brunswig, 1975], органоспецифических ферментов [Хватова Е. А., 1973; Амбарцумян Р. Г. и др., 1977; Сувальская Л. А. и др., 1977],
кислотно-щелочного состояния [Зайцев В. Г., 1966] и др. Однако эти тесты не имеют самостоятельного диагностического значения и могут служить лишь показателями тяжести течения патологического процесса и развивающихся органных осложнений.
Последнее десятилетие характеризуется широким внедрением инструментальных биофизических и автоматизированных методов диагностики и исследования в клиническую практику. Появление оптических приборов с волоконной оптикой, в частности лапароскопов более совершенной конструкции, привело к возрождению почти забытого метода и использованию его возможностей в экстренной хирургической диагностике острого панкреатита [Горохов Л. И., 1968, 1971; Березов Ю. Е. и др., 1970;
Буянов В. М. и др., 1972, 1974, 1975; Popovici, 1965].
Перспективным методом, с нашей точки зрения, является селективная целиакография, которая в экстренной хирургической диагностике острого панкреатита впервые была применена в факультетской хирургической клинике II МОЛГМИ [Прокубовский В. И. и сотр., 1976, 1982].
В последние годы в биологии и медицине получил распространение биофизический метод определения сверхслабого свечения (хемилюминесценция) биологических объектов, в частности сыворотки крови [Владимиров Ю. А., 1966]. Была показана перспективность и диагностическая ценность феномена хемилюминесценции сыворотки крови больных острым панкреатитом [Молоденков М. Н. и др., 1974; Савельев В. С. и др., 1975; Федоров Ю. Л. и др., 1977].
Лечебная тактика и методы лечения острого панкреатита остаются предметом широкого обсуждения в периодической печати и на форумах хирургов. Определились три принципиально различных подхода к лечению этого заболевания, которые можно охарактеризовать как строго консервативный активно-выжидательный и активный хирургический. В ходе дискуссии прежде всего выявились патогенетическая необоснованность операции тампонады сальниковой сумки и сугубо симптоматический характер консервативного лечения.
Конец 60-х — начало 70-х годов характеризуется разработкой главным образом патогенетического подхода к решению лечебнотактических вопросов. С этого времени начинается углубленное изучение патогенетических особенностей заболевания и внедрение новых патогенетически обоснованных методов лечения, к которым относятся специфическое антиферментное лечение [Огнев Ю. В.,
Колодий С. М., 1973; Савельев В. С. и др., 1977; Сыновец А. С,
Левицкий А. И., 1979; Frey, 1953; Haber-land, 1968], регионарная внутриартериальная ингибиторотерапия [Огнев Ю. В., и др., 1974;
Сологуб В. К. и др., 1969; Grozinger, Wanke, 1966; Vestad, Auknus, 1970], перитонеальный диализ [Савельев В. С. и др., 1973, 1977; Wall, 1965; Gjessing, 1967; Bolooki, Gliedman, 1968], дренирование грудного протока [Алексеев А. А., Огнев Ю. В., 1975; Пиковский Д. Л., Алексеев Б. В., 1976; Огнев Ю. В., Филимонов М. И., Алексеев А. А., 1976;
Савельев В. С. и др., 1977; Brzek, Bartos, 1969; Dumont, Witt 1969],
различные виды региональных новокаиновых блокад [Вишневский А. В., 1948; Бакулев А. Н., Виноградов В. В., 1951; Благовидов Д. Ф., Чорбинская Т. И., 1967; Николаев Г. М., 1968; Роман Л. И., 1968; Буянов В. М., 1980; Bockus, 1965], гипотермия желудка [Виноградов В. В. и др., 1965; Петров Б. А. и др., 1966; Котельников В. П. и др., 1977; Loygue, 1964] и прямой кишки [Романов А. И., 1970],
применение препаратов, обладающих антиферментным и секретоблокирующим действием: пент-оксила [Камаев М. Ф., 1964], фторафура [Далгат Д. М. и др. 1978; Маят В. С. и др., 1980], рибонуклеазы [Владимиров В. Г. и др., 1978].
Были разработаны новые принципы хирургической тактики [Тоскин К. Д., 1970; Савельев В. С, Огнев Ю. В., 1976; Козлов В. А., 1978], предложена резекция поджелудочной железы в острый период заболевания [Серга В. И., 1960, 1971; Королев Б. А. и др., 1972;
Шалимов А. А. и др., 1977, 1981; Семенов В. С, 1978; Hollender et al., 1971; Gall et al., 1980].
Разработка и усовершенствование основ неспецифической фармакотерапии и принципов интенсивной терапии [Савельев В. С, 1981; Weil, Schubin, 1967; Zimberg, 1968; Crian, 1980] позволили сформулировать основные положения и определить перспективы консервативной лечебной тактики, а также установить показания к активному хирургическому вмешательству как необходимому этапу патогенетического лечения.
Представленные данные подчеркивают сложность, многопрофильность и практическую значимость рассматриваемой проблемы. Дискутабельность ряда затронутых вопросов предопределяет необходимость их дальнейшего углубленного изучения.
Г л а в а II
КЛИНИЧЕСКАЯ АНАТОМИЯ И ФИЗИОЛОГИЯ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Поджелудочная железа, впервые описанная Клавдием Галеном (130— 200 гг.) —непарный орган, эмбриологически относящийся к брюшной полости. Развиваясь из трех зачатков энтодермы кишечной трубки, она сохраняет некоторую разобщенность анатомически различимых частей: головки, тела и хвоста. Это значительно влияет на механизмы возникновения, характер течения и распространение патологического процесса и обусловливает специфические закономерности развития осложнений. Физиологические особенности поджелудочной железы предопределяют особенности клинических проявлений болезни, а также обусловливают выбор лечебной тактики. В данной монографии мы рассмотрим лишь те вопросы анатомии и физиологии поджелудочной железы, которые имеют прикладной характер и отражают результаты новых исследований.
ФОРМА. ПОЛОЖЕНИЕ И ОРИЕНТИРЫ. КАПСУЛА, БРЮШИНА И ФАСЦИИ
Поджелудочная железа представляет собой образование треугольнопризматической формы. Тело ее обычно имеет три отчетливо выраженные поверхности: переднюю, заднюю и нижнюю, головка и хвост — только две: переднюю и заднюю. На нижней поверхности головки по верхнему краю нижней горизонтальной части двенадцатиперстной кишки располагается крючковидный отросток. Длина поджелудочной железы составляет в среднем 16—17 см, ширина в области головки — 5 см, в области тела — 3,5 см и в области хвоста — 0,3—3,4 см, толщина головки от 1,3 до 3,4 см, тела
— 1,0—2,8 см, хвоста —0,6— 2 см. Масса поджелудочной железы 70—90 г [Воробьев В. П. 1939; Кульчицкий К. И., 1952; Тонков В. Н., 1953; Пронин О. В. 1957; Sobbota, 1953, и др.].
Поджелудочная железа расположена на уровне L1. Продольная ось ее направлена косо: справа налево, снизу вверх. Головка и хвост отклоняются от этой оси кзади. Крайние варианты скелетотопии головки, тела и хвоста, по данным О. В. Пронина (1957), определяются соответственно на уровнях: L1 (реже D12); D12, нижнего края D11 и L4, L3, L2. При крайне правом по отношению к сагиттальной плоскости положении головка железы может находиться на 7 см кнаружи от правого контура позвоночника, а хвост — в пределах до 2 см от его левого края. При крайне левом положении головка проецируется непосредственно на позвоночник, а тело и хвост находятся слева на расстоянии до 9 см от его левого контура. Таким образом, поджелудочная железа располагается в собственно надчревной области и левом подреберье. На переднюю брюшную
стенку тело поджелудочной железы проецируется в середине расстояния между пупком и мечевидным отростком. Головку ее определяют справа от белой линии в треугольнике Шоффара или точке Дежардина [Шелагуров А. А., 1967]. Следует подчеркнуть, что поджелудочная железа расположена на границе брюшной полости и забрюшинного пространства и топографоанатомически тесно связана с забрюшинными органами и сосудами: правыми почечными сосудами и началом воротной вены, верхними брыжеечными сосудами, аортой и началом грудного протока, селезеночной и нижней брыжеечной венами, солнечным сплетением, левыми почкой, надпочечником и почечными сосудами [Лубоцкий Д. Н., 1953]. Отсюда вполне объяснимы трудности разработки так называемых поясничных доступов к поджелудочной железе как к органу, расположенному в забрюшинном пространстве.
Принципиально важно рассмотреть наиболее спорные и важные в практическом смысле вопросы о капсуле поджелудочной железы и ее взаимоотношениях с брюшиной и собственной фасцией, а также о взаимоотношениях самой железы с фасциями и клетчаточными пространствами забрюшинной области.
По О. В. Пронину (1972), многочисленные дольки поджелудочной железы покрыты тонкой капсулой и отделены друг от друга прослойками соединительной ткани. Собственно капсула поджелудочной железы состоит из коллагеновых и эластических волокон, плотно прилегает к секретирующим клеткам долек и и без перерыва продолжается во внутриорганные соединительнотканные прослойки. Толщина ее составляет 42—63 мкм (рис. 1).

По В. В. Кованову и Т. И. Аникиной (1961), собственная фасция поджелудочной железы представляет собой плотную полупрозрачную пластинку, которая неодинаково окружает ее различные отделы. Головку эта фасция окружает со всех сторон и сращена с прилегающей стенкой двенадцатиперстной кишки. Между фасцией и паренхимой головки находится клетчаточная щель, заполненная мелкодольчатой жировой тканью и разделенная соединительнотканными тяжами, идущими от фасциального футляра в паренхиму. Тело и хвост покрыты собственной фасцией только сзади, сверху и снизу. К передней поверхности тела и хвоста прилежит брюшина, соединенная с капсулой и фасцией железы в неразделимую пластинку, за исключением участка у корня поперечной ободочной кишки и оснований связок. Таким образом, вследствие сращения между париетальной брюшиной и фасцией поджелудочной железы фасциальный футляр головки замкнут и изолирован от брюшинно-фасциального футляра тела и хвоста [Лебедев А. М., 1959].
Много исследований посвящено изучению клетчатки, лежащей позади поджелудочной железы. Установлено [Кочиашвили В. И., 1959;
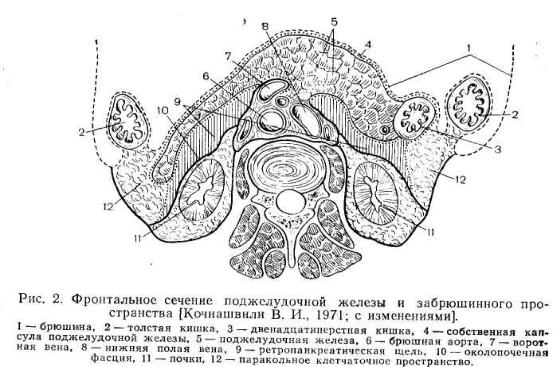
Лебедев А. М., 1959; Кованов В. В., Аникина Т. И., 1961], что поджелудочная железа тесно прилежит к массе рыхлой забрюшшшой клетчатки. Она отделена от нее узким щелевидным пространством («ретропанкреатическая щель», по В. И. Кочиа-швили, 1959), заключенным между фасциальным футляром поджелудочной железы, предпочечной фасцией и фиброзной пластинкой «средостения» живота (рис. 2).
Таким образом, распространению экссудата в клетчаточные пространства забрюшинной области при остром панкреатите препятствуют не только капсула и собственный фасциальный футляр поджелудочной железы, но и позади-брюшинная фасция. В то же время передненижняя поверхность поджелудочной железы, а также область ее хвоста практически ничем не отграничены от клетчатки, выполняющей щели в брыжейке поперечной ободочной кишки, а также от левого паракольного пространства. Именно в этом направлении, как показывают клинические наблюдения, и распространяется панкреатический экссудат в первоначальный период развития острого панкреатита (рис. 3).

Парапанкреатит, который клинически выявляется в виде инфильтрата, расположенного в эпигастрии и левом подреберье, представляет собой результат вовлечения в патологический процесс клетчатки брыжеек поперечной ободочной и тонких кишок, а также левого паракольного пространства.
АРТЕРИАЛЬНАЯ, ВЕНОЗНАЯ И ЛИМФАТИЧЕСКАЯ СИСТЕМА
Литература, посвященная изучению кровоснабжения поджелудочной железы, обширна. До сих пор сохраняются разногласия в трактовке тех или иных типов кровоснабжения и даже в
наименовании одних и тех же отходящих вариантно артериальных стволов. Описано более 20 вариантов ангиоархитектоники поджелудочной железы. Внедрение ангиографических диагностических методов, в частности селективной целиакографии, сделало возможным прижизненное изучение ангиоархитектоники поджелудочной железы.
Для характеристики артериального кровоснабжения поджелудочной железы мы использовали данные анатомических исследований К. И. Кульчицкого (1970), О. И. Елецкой (1971), В. Ф. Парфентьевой и
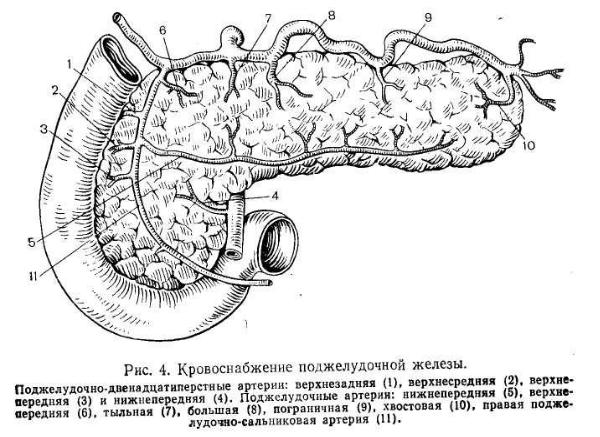
соавт. (1972), В. В. Кованова и Т. И. Аникиной (1974). а также результаты наших ангиографических исследований. Принципиально важно, что поджелудочная железа, не имея собственных крупных артерий, получает многочисленные ветви от артерий других органов. Второй важной особенностью кровоснабжения поджелудочной железы является то, что источники кровоснабжения головки, тела и хвоста вследствие их различного эмбриогенеза разные (рис. 4).
Головку поджелудочной железы снабжают кровью постоянные верхние передняя и задняя поджелудочно-двенадцатиперстные артерии, которые могут отходить раздельно или общим стволом от желудочно-двенадцатиперстнои артерии [Кульчицкий К. И., 1970; Елецкая О. И., 1971; Парфентьева В. Ф. и др., 1972; Кованов В. В., Аникина Т. И., 1974]. В 66,4% случаев встречается и верхняя средняя артерия, которая может быть ветвью желудочно-двенадцатиперстнои либо верхней задней поджелудочно-двенадцатиперстной артерии [Парфентьева В. Ф. и др., 1972]. От верхней брыжеечной артерии или от ее ветвей к головке отходят нижние передняя и задняя поджелудочно-двенадцатиперстные артерии: общим стволом в 43,8% и раздельно в 41,9% случаев [Кульчицкий К. И., 1970]. В. Ф. Парфентьева и соавт. (1972) в 17,85% случаев обнаруживали и так
