
Lab__13_Gidroliz_soley
.docxМинистерство образования и науки Российской Федерации
Владимирский государственный университет
Кафедра химии
Отчет по лабораторной работе
«Гидролиз солей»
Работу выполнил:
Студент группы С-211
Антропов А.С.
Работу принял: Федоров Н.В.
Владимир 2011г.
Краткая теория к работе:
При растворении многих солей в воде образующиеся при диссоциации ионы способны вступать во взаимодействие с молекулами воды. При этом происходит смещение равновесия при диссоциации воды, связывание ионов Н+ или ОH-, в результате чего изменяется рН раствора.
В общем случае процесс обмена ионами между водой и растворёнными в ней солями называется гидролизом.
Существует несколько видов гидролиза солей.
1. Гидролиз солей, образованных сильным основанием и слабой кислотой (например: CH3COONa, K2S03, Na2C03, Na2S).
Гидролиз этих солей обусловлен связыванием ионов водорода в слабый электролит. Так, гидролиз ацетата натрия может быть представлен уравнениями:
CH3COONa
+ H2O
 CH3COOH
+ NaOH
CH3COOH
+ NaOH
CH3COO-
+ Na+ H2O
 CH3COOH
+ Na+
+ OH-
CH3COOH
+ Na+
+ OH-
CH3COO-
+ H2O
 CH3COOH
+ OH-
CH3COOH
+ OH-
(pH > 7).
Соли, образованные слабой многоосновной кислотой, гидролизуются ступенчато. Гидролиз протекает в значительно большей мере по первой ступени. Это приводит к образованию кислых солей.
Na2S
+ H2O
 NaHS + NaOH
NaHS + NaOH
2Na+
S2-
+ H2O
 Na+
+ HS-
+ Na+
+ OH-
Na+
+ HS-
+ Na+
+ OH-
S2-
+ H2O
 HS-
+ OH-
HS-
+ OH-
(pH > 7).
Растворы солей, образованных сильным основанием и слабой кислотой, имеют щелочную реакцию среды.
2. Гидролиз солей, образованных слабым основанием и сильной кислотой (например: NH4C1, CuSO4, Zn(NO3)2, A1C13).
Гидролиз этих солей обусловлен связыванием гидроксид-ионов в слабый электролит. Так, гидролиз хлорида аммония может быть представлен уравнениями:
NH4Cl
+ H2O
 NH4OH
+ HCl
NH4OH
+ HCl
 +
Cl-
+ H2O
+
Cl-
+ H2O
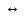 NH4OH
+ H+
+ Cl-
NH4OH
+ H+
+ Cl-
 +
H2O
+
H2O
 NH4OH
+ H+
NH4OH
+ H+
(pH < 7).
Соли, образованные слабым многокислотным основанием, гидролизуются ступенчато. Процесс гидролиза протекает в большей мере по первой ступени, что приводит к образованию основных солей:
Zn(NO3)2
+ H2O
 Zn(OH)NO3
+ HNO3
Zn(OH)NO3
+ HNO3
Zn2+
+
 + H2O
+ H2O
 Zn(OH)+
+
Zn(OH)+
+
 + H+
+
+ H+
+

Zn2+
+ H2O
 Zn(OH)+
+ H+
Zn(OH)+
+ H+
(pH < 7).
Растворы солей, образованных слабым основанием и сильной кислотой, имеют кислую реакцию среды.
3. Гидролиз солей, образованных слабым основанием и слабой кислотой.
Соли этого типа гидролизуются наиболее сильно, так как их ионы одновременно связывают ионы водорода и гидроксид-ионы воды. Например, гидролиз ацетата аммония может быть выражен уравнением:
CH3COONH4
+ H2O
 CH3COOH
+ NH4OH.
CH3COOH
+ NH4OH.
Соли, образованные слабыми многокислотными основаниями и слабыми многоосновными кислотами, гидролизуются необратимо:
A12S3
+ 6Н20
 2Аl(ОН)3
2Аl(ОН)3 + 3H2S
+ 3H2S ,
,
поэтому не могут быть получены водные растворы таких солей, как Al(CO3)3, Cr2S3, Fe2S3 и др.
В
зависимости от соотношения констант
диссоциации образующихся при гидролизе
кислоты и основания растворы солей
этого типа могут иметь слабокислую или
слабощелочную среду реакции, т.е. pH
 7.
7.
4. Соли, образованные сильным основанием и сильной кислотой (например: NaCl, K2SO4, KNO3 и др.), гидролизу не подвергаются, так как при их растворении взаимодействия ионов этих солей с водой не происходит. Поэтому в растворах этих солей рН = 7, т. е. реакция среды остаётся нейтральной.
Экспериментальная часть:
Приборы и реактивы: спиртовка; микрошпатель. Растворы: карбоната натрия 0,2 н.; хлорида цинка 0,1 н.; нитрата натрия 0,2 н.; гидрокарбоната натрия 0,2 н; сульфата алюминия 0,1 н.; сульфата меди (II) 0,2 н.; соляной кислоты (концентрированная). Ацетат натрия кристаллический; вода дистиллированная; фенолфталеин; лакмус.
Выполнение работы:
Опыт 1: Изучение различных видов гидролиза
2-ая
пробирка:
1.Na2CO3
+ H2O
 NaOH + NaHCO3
NaOH + NaHCO3
2Na+
+
 + H2O
+ H2O
 Na+OH-
+ Na+
+
Na+OH-
+ Na+
+

 +
H2O
+
H2O

 + OH-
+ OH-
2.
NaHCO3
+ H2O
 NaOH + H2CO3
NaOH + H2CO3
Na+
+
 + H2O
+ H2O
 Na+
+ OH-
+
Na+
+ OH-
+

HCO3
+ H2O
 OH-
+ H2CO3
OH-
+ H2CO3
3-яя
пробирка:
1.ZnCl2
+ H2O
 HCl + ZnOHCl
HCl + ZnOHCl
Zn2+
+ 2Cl-
+ H2O
 H+
+ Cl-
+ ZnOH+
+ Cl-
H+
+ Cl-
+ ZnOH+
+ Cl-
Zn2+
+ Cl-
+ HOH
 ZnOH+
+ H+
ZnOH+
+ H+
2.ZnOH
+ H2O
 HCl + Zn(OH)2
HCl + Zn(OH)2
ZnOH+
+ Cl-
+ H2O
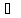 H+
+ Cl-
+ Zn(OH)2
H+
+ Cl-
+ Zn(OH)2
ZnOH+
+ HOH-
 H+
+ Zn(OH)2
H+
+ Zn(OH)2
pH < 7 т.к. кислая среда.
4-ая
пробирка: NaNO3
+ H2O
 NaOH
+ HNO3
NaOH
+ HNO3
Na+
+
 + H2O
+ H2O
 Na+
+ OH-
+ HNO3
Na+
+ OH-
+ HNO3
 +
H2O
+
H2O
 HNO3
+ OH-
HNO3
+ OH-
|
|
H2O |
Na2CO3 |
ZnCl2 |
NaNO3 |
|
Окраска |
Фиолетовая |
Синяя |
Розовая |
Фиолетовая |
|
Реакция |
Нейтральная |
Щелочная |
Кислотная |
Нейтральная |
|
Вывод |
H+ = OH- |
Соль, образованная сильным основанием и слабой кислотой, имеет щелочную реакцию, т.к. в растворе избыток гидроксид-ионо |
Соль, образованная слабым основанием и сильной кислотой, имеет кислую реакцию, т.к. в растворе избыток ионов водорода. |
H+ = OH- |
Опыт 2: Сравнение гидролиза кислых и средних солей
1-ая
пробирка:
Na2CO3
+ H2O
 NaOH + NaHCO3
NaOH + NaHCO3
2Na+
+
 + H2O
+ H2O
 Na+
+ OH-
+ H+
+
Na+
+ OH-
+ H+
+

2-ая
пробирка:
NaHCO3
+ H2O
 H2CO3
+ NaOH
H2CO3
+ NaOH
Na+
+ H+
+
 + H2O
+ H2O
 2H+
+
2H+
+
 + Na+
+ OH-
+ Na+
+ OH-
В ходе опыта, удостоверились в получение окраски веществ:
|
Раствор |
Na2CO3 |
NaHCO3 |
|
Окраска |
малиновая |
бесцветная |
Выводом следует возможность образования кислых солей при гидролизе, т.к. соли, образуются путем слабой многоосновной кислотой и гидролизируются ступенчато, но гидролиз протекает в значительной мере по первой ступени, что и приводит к образованию кислых солей.
Опыт 3: Получение и гидролиз соли слабого основания и слабой кислоты
1-ая
пробирка: Al2(SO4)3
+ 6H2O
 2Al(OH)3
+ 3H2SO4
2Al(OH)3
+ 3H2SO4
2Al3+
+ 3(SO4)2-
+ 6H2O
 2Al3+
+ 3OH-
+ 6H+
+
2Al3+
+ 3OH-
+ 6H+
+

2-ая
пробирка:
Na2CO3
+ H2O
 NaOH + NaHCO3
NaOH + NaHCO3
2Na+
+
 + H2O
+ H2O
 Na+
+ OH-
+ H+
+
Na+
+ OH-
+ H+
+

В ходе опыта, в пробирке наблюдается осадок алюминия, после добавления кислоты – вещество обесцыечивается. Полный и необратимый гидролиз солей. Некоторые соли, образованные слабыми летучими кислотами и многокислотными гидроксидами не могут находиться в виде водных растворов из-за полного необратимого взаимодействия с водой, сопровождающегося одновременным выделением газа и выпадением осадка.
