
Ароматичность
Это понятие, включающее различные свойства ароматических соединений ввёл немецкий физик Э. Хюккель (1931).
Условия ароматичности:
плоский замкнутый цикл
все атомы С находятся в sp2 – гибридизации
образуется единая сопряженная система всех атомов цикла
выполняется правило Хюккеля: “В сопряжении участвуют 4n+2 -электронов, где n = 1, 2, 3... ”
Простейший представитель ароматических углеводородов – бензол. Он удовлетворяет всем четырем условиям ароматичности.
Правило Хюккеля: 4n+2 = 6, n = 1.
|
Нафталин |
Нафталин – ароматическое соединение Правило Хюккеля: 4n+2 = 10, n = 2. |
|
Пиридин |
Пиридин – ароматическое гетероциклическое соединение. |
Мезомерный эффект
В отличие от несопряженных в которых электронное влияние заместителей передается по ϭ-связям (индуктивный эффект), в сопряженных системах в передаче электронного влияния основную роль играют π-электроны делокализованных ковалентных связей. Эффект, проявляющийся в смещении электронной плотности делокализованной (сопряженной) π-системы, называют эффектом сопряжения или мезомерным эффектом.
Мезомерный эффект (+М, -М) – передача электронного влияния заместителя по сопряженной системе.
При
этом заместитель становится частью
сопряженной системы. Он может вносить
в систему сопряжения π-связь (карбонильная,
карбоксильная, нитро группа, сульфогруппа
и др.), неподелённую пару электронов
гетероатома (галогены, амино-, гидроксильную
группы), вакантную или заполненную одним
или двумя электронами р-орбиталей.
Обозначается буквой М и изогнутой
стрелкой
![]() Мезомерный
эффект может быть «+» или «–».
Мезомерный
эффект может быть «+» или «–».
З
 аместители,
повышающие электронную плотность в
сопряженной системе, проявляют
положительный мезомерный эффект. Они
содержат атомы с неподеленной электронной
парой или отрицательным зарядом и
способны к передаче своих электронов
в общую сопряженную систему, т. е.
являютсяэлектронодонорами.(ЭД).
Они направляют реакции SE
в
положения 2,4,6 и называются ориентантами
I
рода
аместители,
повышающие электронную плотность в
сопряженной системе, проявляют
положительный мезомерный эффект. Они
содержат атомы с неподеленной электронной
парой или отрицательным зарядом и
способны к передаче своих электронов
в общую сопряженную систему, т. е.
являютсяэлектронодонорами.(ЭД).
Они направляют реакции SE
в
положения 2,4,6 и называются ориентантами
I
рода
Примеры ЭД:
|
Фенол
|
р, -сопряжение Гидроксильная группа –ОН проявляет +М. |
З аместитель,
притягивающий электроны из сопряженной
системы, проявляет –М и наз-сяэлектроноакцептором
(ЭА).
Это заместители, имеющие двойную связь
аместитель,
притягивающий электроны из сопряженной
системы, проявляет –М и наз-сяэлектроноакцептором
(ЭА).
Это заместители, имеющие двойную связь
|
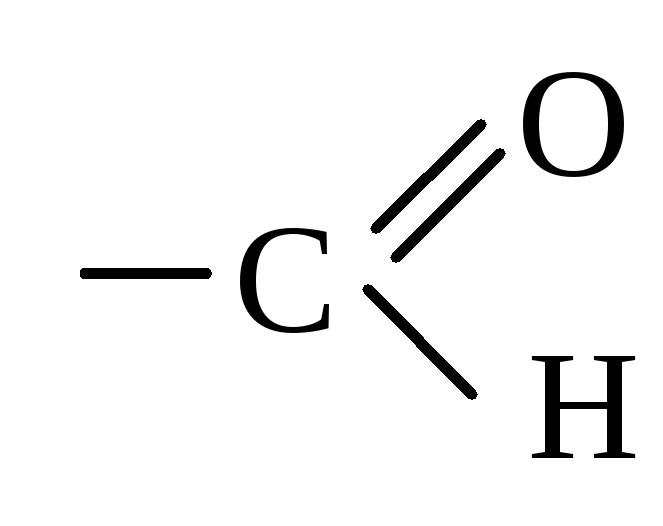
Акролеин |
Альдегидная группа проявляет – М. |
 бензальдегид
бензальдегид
Таблица 1 Электронные эффекты заместителей
|
Заместители |
Ориентанты в С6Н5-R |
I |
М |
|
|
Ориентанты I рода: направляют ЭД заместители в орто- и пара- положения |
+ |
|
|
– |
– |
+ | |
|
– |
– |
+ | |
|
–Н |
– |
+ | |
|
ЭА |
Ориентанты II рода: направляют заместители в мета- положения |
– |
– |
Рекомендуемая литература
Основная
1. Лузин А. П., Зурабян С. Э., Н. А. Тюкавкина, Органическая химия (учебник для учащихся средних фармацевтическх и медицинских заведений), 2002 г. С.42-46, 124-128.
Дополнительная
Егоров А. С., Шацкая К. П. Химия. Пособие – репититор для поступающих в вузы
Кузьменко Н. Е., Еремин В. В., Попков В. А. Начала химии М., 1998. С. 57-61.
Райл С. А., Смит К., Уорд Р. Основы органической химии для студентов биологических и медицинских специальностей М.: Мир, 1983.
4. Лекции преподавателей.




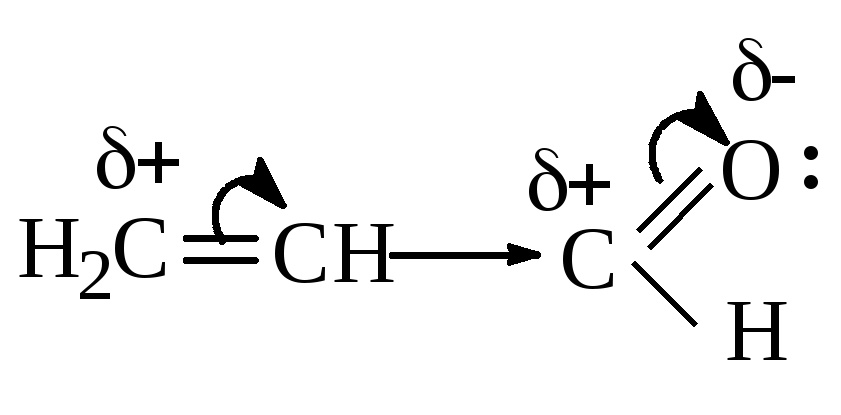
 ,
- сопряжение
,
- сопряжение Аlk
(R-):
СН3-,
С2Н5-...
Аlk
(R-):
СН3-,
С2Н5-...

