
- •Лекции 1,2 по курсам «Основы спектральных методов анализа» (нм2) и «Атомно-эмиссионный анализ» (сп)
- •1. Электромагнитное излучение
- •1.2. Спектр электромагнитного излучения
- •2. Строение вещества и происхождение спектров
- •2.1. Строение атома и происхождение атомных спектров
- •Происхождение атомных спектров
- •2.2. Строение молекул и происхождение молекулярных спектров
- •3. Атомная спектроскопия
- •3.1. Атомно-эмиссионная спектроскопия
- •Лекции 3,4 Экскурс в историю спектрального анализа
- •Спектральные приборы
- •Щель спектрального прибора
- •Лекции 5,6
- •Фотометрические понятия
- •Приемники света
- •Интенсивность спектральных линий
- •Зависимость интенсивности спектральной линии от энергии возбужденного состояния
- •Зависимость интенсивности спектральной линии от температуры газа
- •Ширина спектральных линий
- •Зависимость интенсивности спектральной линии от числа атомов в светящейся паре и от концентрации элемента в пробе
- •Самообращение спектральных линий
- •Интенсивность фона в спектре и его природа
- •Атомно-эмиссионный спектральный анализ с электротермическим возбуждением
- •6.2. Атомно-абсорбционная спектроскопия
- •6.2.1. Способы атомизации
- •6.2.2. Источники излучения
- •6.2.3. Приборы в аас
- •Онных измерений: 1—лампа с полым катодом; 2—модулятор; 3—пламя; 4—монохроматор; 5—детектор
- •6.2.4. Способы определения концентрации
- •6.3. Сравнение атомно-спектроскопических методов и их применение
Происхождение атомных спектров
При изменении хотя бы одного квантового числа (главное n, побочное – l; магнитное – m; спиновое - ms) атом получает или отдает энергию. Это может произойти при взаимодействии атома с электромагнитным полем, при непосредственном обмене энергией с другими атомами или молекулами, например при столкновениях или при химических реакциях. В отсутствии внешних воздействий атом находится в основном состоянии, т. е. обладает наименьшей энергией. При получении энергии извне скорость электронов увеличивается— атом возбуждается.
Рис.3.
Энергетические переходы в атоме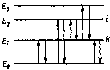
Один атом за один акт поглощает или испускает только один фотон с определенной энергией (частотой). Вещество состоит из множества одинаковых атомов, способных переходить на разные энергетические уровни, испуская или поглощая фотоны разных частот. Совокупность всех фотонов одной и той же частоты составляет спектральную линию, при поглощении ее называют абсорбционной, при испускании—эмиссионной. Совокупность всех абсорбционных или всех эмиссионных линий называют абсорбционным (поглощение) или эмиссионным (испускание) спектром вещества.
Спектр поглощения получают, помещая исследуемое вещество в поле электромагнитного излучения (например, на пути светового потока), а для получения спектра испускания предварительно переводят атомы вещества в возбужденное состояние, что достигается подведением какого-либо вида энергии (тепловой, химической, электроразряда, электромагнитного излучения и т. п.); после возбуждения атомы через 10–9–10–7 с возвращаются в основное состояние, испуская фотоны либо теплоту. В последнем случае переход будет безызлучательным; на рис. 3 он изображен волнистой стрелкой.
Частота испускаемого или поглощаемого излучения определяется разностью энергии между электронными орбиталями ∆Е:
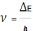
 , где
h
– постоянная Планка
, где
h
– постоянная Планка
Абсолютная энергия квантовых состояний неизвестна, поэтому ее отсчитывают от некоторого уровня, условно принятого за нулевой, а именно от энергии ионизации, т. е. полного отрыва электрона от атома.
Энергия атомных орбиталей сильно различается. Так, для возбуждения электрона с ближайшей к ядру орбитали (главное квантовое число n=1) требуется более 6∙104 кДж моль–1 (испускаемые фотоны имеют частоту рентгеновского излучения), а для возбуждения внешних электронов достаточно 150— 600 кДж моль-1 (излучение ультрафиолетовой и видимой областей). С увеличением главного квантового числа энергия возбуждения ∆Е и частота излучения уменьшаются (рис. 2.).
Наиболее вероятны переходы с первого возбужденного уровня на основной Е0; соответствующие им спектральные линии называют резонансными. Электрон может перейти и в более высокое энергетическое состояние (Е2, Е3 и т. д.). Возвращение его на уровень Е0 может проходить через ряд промежуточных ступеней.

Рис. 4. Относительное расположение энергетических уровней различных квантовых состояний и изменение энергии при электронных переходах
Внешние легко возбудимые электроны называют оптическими, переходы с их участием дают оптический спектр. Энергия возбуждения внешних электронов разных элементов неодинакова. Например, для получения резонансной линии щелочных металлов (переход Е1→Е0) требуется сравнительно невысокая энергия (~2эВ, длины волн лежат в видимой области), для неметаллов эта энергия существенно больше (~ 5 эВ, длины волн лежат в УФ-области). Чем больше внешних электронов, тем больше возможностей имеет атом для энергетических переходов, поэтому спектры металлов типа железа состоят из тысяч линий, а спектры щелочных элементов бедны ими.
Атомно-спектроскопические методы анализа.
Все многочисленные энергетические переходы электронов по орбиталям атома могут быть использованы в аналитических целях. Методы анализа, основанные на изменениях энергетического состояния атомов веществ, входят в группу атомно- спектроскопических методов, различающихся по способу получения и регистрации сигнала.
Оптические методы используют энергетические переходы внешних (валентных) электронов, общим для них является необходимость предварительной атомизации (разложение на атомы) вещества.
Атомно-эмиссионная спектрометрия основана на испускании излучения атомами, возбужденными кинетической энергией плазмы, дугового или искрового разряда и т. п.
Атомно-флуоресцентная спектроскопия использует испускание излучения атомами, возбужденными электромагнитным излучением от внешнего источника.
Атомно-абсорбционная спектроскопия основана на поглощении атомами излучения от внешнего источника.
Рентгеновские методы основаны на энергетических переходах внутренних электронов атомов. В зависимости от способа получения и регистрации сигнала различают рентгеноэмиссионную, рентгеноабсорбционную и рентгенофлуоресцентную спектроскопию. Разновидности этих методов — оже-спектроскопию, рентгеновский электронно-зондовый анализ, электронную спектроскопию — используют в основном для исследования строения веществ. Рентгеновские методы не требуют атомизации вещества и позволяют исследовать твердые пробы без предварительной подготовки.
Ядерные методы основаны на возбуждении ядер атомов.
На рис. 5. приведены разные методы, основанные на атомной эмиссии или абсорбции. Эти методы широко применяют, и они отличаются высокой избирательностью, исключительной чувствительностью, скоростью и удобством; они относятся к наиболее селективным аналитическим методам. Этими методами можно определять около 70 элементов. Чувствительность обычно лежит в интервале 10-4—10–10%. Атомный спектральный анализ часто можно выполнить за несколько минут.
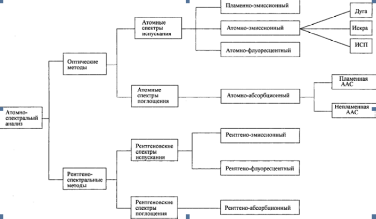
Рис. 5. Классификация методов атомной спектроскопии
