
Сканирующая зондовая микроскопия диссертация
.pdfфакторами, таким практически не контролируемым параметром, как форма острия зонда. От этого параметра зависят площадь контакта между электродами в АСМконфигурации или радиус электронного пучка при туннелировании в СТМконфигурации. Нужно отметить, что корректное извлечение количественных параметров, описывающих проводимость материала, на данный момент не реализовано даже для атомно-силовой микроскопии, несмотря на существенно более простую конфигурацию зазора. Разработанные методики измерения дифференциальных зависимостей могут значительно облегчить переход от качественного сопоставления к количественному анализу свойств материала, так как такие зависимости в значительно меньшей степени зависят от параметров зазора как такового. Поэтому работы в данном направлении будут, несомненно, продолжены.
3.2. Микроструктура тонких пленок на основе допированного SnO2
Близкими аналогами рассмотренных выше керамическим материалов являются наногетерогенные тонкие пленки на основе SnO2 (потенциальные зарядаккумулирующие материалы для эксплуатации как в водных растворах электролитов, так и в качестве электродных материалов для литиевых аккумуляторов). Данные материалы были получены сотрудниками ГНЦ РФ НИФХИ им. Л.Я.Карпова Ю.Е.Рогинской и Г.Г.Постоваловой, совместно с которыми и выполнялись представленные в этом разделе исследования.
Тонкие пленки допированного диоксида олова синтезировались методом термогидролитического разложения растворов солей при их послойном нанесении на подложку с последующим отжигом. Подробное описание методики получения пленок представлено в [715–718]. В качестве допантов выступали титан, цирконий, сурьма в концентрациях до 30 мол.%. Заключительный отжиг готового образца выполнялся, как правило, при 450оС. В качестве подложек использовались пластины кварца, стеклоуглерода и титана. Структурные исследования [716] таких материалов показали, что в этих условиях в составе пленки формируется твердого раствор замещения в структуре рутила, с кристаллами размером 10–15 нм. Кроме того, в пленках присутствует заметное количество аморфного диоксида олова (до 10–30%, в зависимости от типа допирования и условий термообработки). Полная кристаллизация материала может быть достигнута лишь при температурах 550–600оС. По данным рентгеновской фотоэлектронной спектроскопии, пленки в поверхностных слоях значительно гидратированы и содержат большое количество Sn(II).
231
3.2.1. Электрохимическое поведение тонких пленок в водных растворах
Измерения в водных растворах производилось с использованием толстых (более 10 слоев, масса пленки до 1 мг/см2) пленок допированного SnO2 на стеклоуглеродных подложках. Измерения проводились в 0.5М H2SO4 и в фосфатных и ацетатных буферных растворах с pH 3.56, 6.86, 9.18. В настоящем разделе потенциал приводится относительно насыщенного каломельного электрода сравнения. Во всех электрохимических экспериментах измерения проводились в области потенциалов термодинамической устойчивости массивных оксида и гидроксида Sn(IV). Потенциал катодной границы циклирования никогда не снижался ниже 0 В в 0.5M H2SO4 (смещения равновесий SnO2/Sn2+ и Sn(OH)4/Sn2+ в сторону образования восстановленной формы можно ожидать при потенциалах не выше –0.32 и –0.12 В, соответственно [719]). Стационарный потенциал в 0.5 M H2SO4 для всех исследованных материалов составляет около 0.3 В, то есть заведомо положительнее потенциала системы SnO2/Sn2+ даже при низких концентрациях ионов Sn2+ в растворе.
Для всех исследованных пленок в интервале потенциалов 0–1 В наблюдалось обратимое перезаряжение. При длительном циклировании в серной кислоте образцов, допированных титаном, не наблюдается значимого снижения полного заряда. Таким образом, в ходе измерений не происходит растворения оксидной пленки в растворе. Пленки, допированные сурьмой и цирконием, демонстрируют рост обратимо перезаряжаемой емкости в ходе циклирования (рис. 194а). Аналогичная активация пленок, допированных титаном, достигается после кратковременной выдержки при потенциале 2.0 В с последующим циклированием (рис. 194б). Полный заряд в ходе циклирования удается увеличить в 5–10 раз. Активация наиболее выражена для материалов, подвергнутых более длительному отжигу (с меньшим содержанием аморфного диоксида олова и более крупными размерами кристаллов твердого раствора). Образцы, допированные цирконием, демонстрируют примерно на порядок меньшую емкость, чем остальные исследовавшиеся пленки. Возможно, это связано с протеканием процессов перезаряжения в условиях омических ограничений, определяемых очень низкой проводимостью цирконий-содержащего материала.
Существенной особенностью всех регистрируемых вольтамперограмм является наличие четкой пары пиков (формальный потенциал 0.2–0.3 В) при потенциалах значительно (на 0.3–0.4 В) положительнее характерных значений, отвечающих редокспревращениям в оксидно-гидроксидных пленках на металлическом олове [720, 721]. После электрохимической активации разность потенциалов катодного и анодного пиков (∆E) для пленок, допированных сурьмой и цирконием, составляет 0.05–0.12 В (при
232

скорости развертки потенциала 50 мВ/с). Для образцов, допированных титаном, эта величина достигает 0.2 В. При увеличении pH раствора происходит размывание редокспиков и увеличение ∆E. Как правило, в нейтральном и слабощелочном растворах не удается зафиксировать четких катодных пиков. Для материала, допированного титаном, потенциал анодного пика не зависит от pH, тогда как в случае сурьмы он снижается с ростом pH (наклон около 0.05 В/рН). Общая поляризационная емкость для SnO2, допированного сурьмой, несколько снижается с ростом рН (рис. 195, кривая 2). В то же время для титан-содержащего материала наблюдается сначала плавный рост емкости, а затем резкий спад при переходе к щелочному раствору (рис. 195, кривая 3). Наблюдаемое снижение емкости обратимо; после переноса электрода в 0.5 М H2SO4 исходная емкость быстро восстанавливается. Для материала, допированного титаном, в ходе длительного циклирования в растворах с различными рН происходит дополнительная активация электрода, и стабилизированное значение емкости в 0.5 М H2SO4 достигает 40 Ф/г.
а |
б |
Рис. 194. Циклические вольтамперограммы образцов SnO2, допированных 5% Sb2O3 (а) и 10% TiO2 (б), полученные в растворе 0.5 М H2SO4. Образец, допированный титаном (б), циклировался после кратковременной выдержки при потенциале 2.0 В. Скорость развертки потенциала 50 мВ/с. Номера циклов 1 — 1, 2 — 100, 3 — 300, 4 — 500.
Рис. 195. Зависимость общей поляризационной емкости от pH для образцов, содержащих 5% Sb2O3 (1, 2) подвергнутых длительному (1) и быстрому (2) отжигу и 10% TiO2 (3).
233
3.2.2. Электрохимическое поведение тонких пленок при интеркаляции/деинтеркаляции лития
Диоксид олова является также перспективным электродным материалом для использования в литиевых аккумуляторах. Согласно современным представлениям [722, 723], при литировании материалов на основе SnO2 на первом этапе происходит необратимое восстановление олова до металла. В дальнейшем металл обратимо литируется/делитируется благодаря образованию интерметаллида Li4.4Sn. Для обеспечения высоких зарядно/разрядных характеристик необходимо обеспечить высокую дисперсность образующихся металлических частиц, а одной из основных причин снижения обратимой емкости является их укрупнение. Таким образом, нанодисперсные пленки допированного SnO2 получаемые термогидролитическим методом, можно рассматривать как перспективный материал для применения в этой области.
Предварительные исследования показали, что добиться наилучшей деградационной стабильности удается при допировании диоксида олова титаном. В качестве подложки для приготовления электродов, на которых изучались процессы интеркаляции лития, использовались механически полированные титановые пластины. Образцы, как правило, отжигались при температуре 450оС. Электрохимические измерения проводились в 1 M LiN(CF3SO2)2 в диоксолане (содержание воды не более 70 ppm). Использовалась трехэлектродная электрохимическая ячейка с разделенными полипропиленовой мембраной пространствами. Все потенциалы представлены в шкале литиевого электрода сравнения.
С помощью метода рентгеновской дифракции для пленок было подтверждено образование твердого раствора с кристаллической структурой рутила, параметр элементарной ячейки которого закономерно уменьшался с ростом содержания титана (r(Ti4+)=0.064 нм, r(Sn4+)=0.071 нм). Кроме того, было выявлено присутствие значительного количества аморфной составляющей. Наблюдался рост дисперсности и количества дефектов в кристаллитах при увеличении содержания титана. Лишь для не допированой пленки SnO2, для которой уширения рефлексов на дифрактограммах были обусловлены преимущественно дисперсностью, а не дефектностью материала, удалось получить оценки размеров кристаллитов (11 нм). Значительное увеличение доли аморфного диоксида олова с ростом содержания титана в пленках было доказано на основании анализа Месбауэровских спектров образцов.
При катодном восстановлении свежей пленки наблюдается значительная необратимая емкость (рис. 196), которая может быть отнесена в первую очередь к восстановлению SnO2 с образованием металлического олова. Действительно, рентгенофазовый
234

анализ и мессбауэровские спектры пленок SnO2 после длительного циклирования позволяют обнаружить, что лишь 10–15% олова в пленке переходит в металлическое состояние (сохранившаяся фаза SnO2 сильно диспергирована и аморфизована). При последующем циклировании пленки демонстрируют обратимую емкость около 400 мА•ч/г. Допирование титаном позволяет существенно повысить деградационную стабильность пленок в ходе процессов интеркаляции/деинтеркаляции лития (рис. 197). Следует отметить, что небольшое количество металлического олова, образующегося при восстановлении диоксида, не позволяет объяснить наблюдаемые высокие емкости. Нельзя исключить, что одновременно протекают процессы интеркаляции в аморфные фрагменты диоксида олова, подобные процессам в водных растворах. Однако наблюдаемые четкие пики на вольтамперограммах, с учетом данных [722, 723] о характеристических потенциалах, должны быть все таки отнесены к процессам интеркаляции лития в металлическое олово с образованием интерметаллидов.
E, В |
|
|
1.5 |
|
|
3 |
|
|
1 |
2 |
|
1.0 |
а |
б |
0.5
0 |
–800 |
–600 |
–400 |
–200 |
0 |
200 |
400 |
–1000 |
C, мА•ч/г
Рис. 196. Зарядно-разрядные кривые (а), полученные в растворе LiN(CF3SO2)2 в диоксолане для пленок SnO2, допированных 1 — 0%, 2 — 10%, 3 — 20 мол.% TiO2. Плотность тока 80 мА/г. Циклические вольтамперограммы (б) (первый и второй цикл), полученные на образце, содержащем 10% TiO2. Скорость развертки потенциала 75 мкВ/с.
C, мА•ч/г
500
400 



300
200
2 |
3 |
|
100
|
|
|
1 |
|
|
|
|
0 0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
Числоциклов
Рис. 197. Изменение обратимой емкости пленок SnO2, допированных 1 — 0%, 2 — 10%, 3 — 20 мол.% TiO2 в ходе последовательного циклирования в растворе LiN(CF3SO2)2 в диоксолане. Плотность тока 80 мА/г.
235

3.2.3. Микроструктура тонких пленок
Типичная морфология поверхности пленок на стеклоуглероде по данным СТМисследований, полученных с использованием микроскопа Литскан-2, представлена на рис. 198. Размеры частиц в исследуемых образцах не превышают нескольких десятков нанометров, что неплохо согласуется с результатами оценок по данным рентгеновской дифракции [716]. Туннельные вольтамперные характеристики (рис. 199) свидетельствуют о полупроводниковой проводимости материала с n-типом носителей заряда. Наклон ВАХ хорошо согласуется с данными резистометрии таких пленок [717]: при допировании титаном, и, особенно, цирконием, происходит быстрое снижение проводимости материала. С увеличением содержания сурьмы в пленке сначала наблюдается рост, а затем снижение проводимости. Аналогичное поведение, объясняющееся сосуществованием в решетке рутила атомов сурьмы в разной степени окисления (Sb(V) и Sb(III), взаимно компенсирующих влияние друг друга), было обнаружено и для керамики на основе диоксида олова [675, 676]. Перепад высот на вольтвысотных зависимостях для образцов с высокой проводимостью характеризует для данного типа образцов степень кристалличности материала под зондом (рис. 199б). В области межзеренных границ регистрируются перепады высот, превышающие 10–15 нм (кривая 1 рис. 199б), что однозначно свидетельствует о локализации в этих областях аморфных гидратированных фрагментов. Анализ большого массива туннельных спектров показал, что уровень шумов туннельного тока и доля участков поверхности, на которых обнаруживаются большие перепады высот на вольтвысотных зависимостях, коррелируют с содержанием аморфной составляющей в образцах (наивысшее содержание — в образцах, допированных титаном).
Рис. 198. Типичные СТМ-изображения наногетерогенных оксидных пленок SnO2 на стеклоуглероде, допированных 5 мол.% Sb2O3 (а) и 1мол.% ZrO2 (б).
236

Iтун, нА |
|
∆H, нм |
|
30 |
|
4 |
|
1 |
2 |
1 |
3 |
а |
б |
2 |
20 |
|
0 |
3 |
10 |
2 |
|
1 |
|
3 |
|
2 |
|
|
–2–2 |
–1 |
0 |
1 |
2 |
–2 |
–1 |
0 |
1 |
2 |
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
Uтун, В |
|
|
|
|
Uтун, В |
Рис.199. (а) Туннельные вольтамперные характеристики оксидных пленок SnO2, допированных 1 — 1%, 2 — 5%, 3 — 10 мол.% Sb2O3. Положительное туннельное напряжение отвечает положительному потенциалу зонда. (б) Типичные вольтвысотные туннельные спектры, полученные для оксидных пленок SnO2, допированных 5 мол.% Sb2O3: 1 — для областей межзеренных границ, 2,3 — для центральных участков кристаллитов.
Близкие результаты были получены и для материалов на титановых подложках, использовавшихся для изучения процессов интеркаляции/деинтеркаляции лития. СТМ исследование морфологии подложки выявило присутствие на поверхности глубоких царапин (борозд), образовавшихся в ходе полировки (рис. 200). Кроме того, как уже упоминалось ранее в главе 2, поверхность титана легко претерпевает локальное окисление в туннельном зазоре (рис. 72). Морфология пленок диоксида олова значительно отличается от морфологии подложки, СТМ-изображения свидетельствуют о присутствии на поверхности крупных глобул (200–700 нм), состоящих из наноразмерных частиц (рис. 200). Размеры частиц для не допированной пленки, определенные по результатам СТМ измерений и из анализа данных РФА, неплохо согласуются. Увеличение содержания титана в пленке диоксида олова приводит к снижению характерного размера кристаллитов на СТМ-изображениях (рис. 200, 201) и резкому росту сопротивления материала (рис. 202). При введении в состав пленки 20% титана ее сопротивление снижается настолько, что не для всех участков поверхности удается стабилизировать туннельный зазор при рабочих туннельных токах 200–300 пА и напряжении 1.3 В. Локальные вольтамперные спектры указывают на полупроводниковый характер и значительную неоднородность проводимости вдоль поверхности (наклоны спектров в разных точках поверхности отличаются на несколько порядков). Такой результат может быть связан с различиями электрофизических свойств аморфных и кристаллических наноразмерных фрагментов или с локальной неравномерностью степени легирования образующегося композиционного материала.
237

Рис. 200. Типичные СТМ-изображения титановой подложки (a) и наногетерогенных оксидных пленок SnO2, допированных 0% (б), 10% (в) и 20 мол.% (г) TiO2.
Рис. 201. Типичные СТМ-изображения наногетерогенных оксидных пленок SnO2, до-
пированных 0% (a), 10% (б) и 20 мол.% (в, г) TiO2.
238
Iтун, нА |
|
|
1 |
|
4 |
|
|
2 |
|
|
|
|
|
3 |
3 |
|
|
|
|
2 |
|
|
|
|
1 |
|
|
|
4 |
0 |
|
|
|
|
–1 |
–1 |
0 |
1 |
2 |
–2 |
||||
|
|
|
|
Uтун, В |
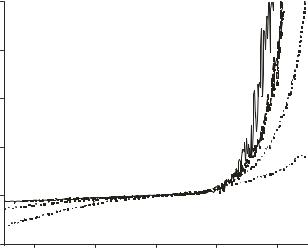
Рис. 202. Туннельные вольтамперные характеристики оксидных пленок SnO2, допированных 1 — 0%, 2 — 10%, 3, 4 — 20 мол.% TiO2 (в разных точках гетерогенного образца). Положительное туннельное напряжение отвечает положительному потенциалу зонда.
Существенная неравномерность локальных свойств выявляется также на вольтвысотных зависимостях, измеренных в разных точках поверхности (рис. 203б). Существенный рост перепада высот на спектрах, особенно при переходе к образцу с 20% TiO2, связан, в первую очередь с тем, что для допированных образцов проводимость материала настолько снижается, что при низких напряжениях становится невозможным поддержание требуемого туннельного тока, и в ходе измерения вольтвысотной кривой зонд переходит в режим механического контакта с поверхностью (рис. 203). Гетерогенность материала подтверждается также результатами дифференциального картирования проводимости (рис. 204). Из-за малого размера частиц при таких измерениях не удается достичь такого же контраста на изображениях, какой был получен при исследовании керамических материалов. Тем не менее, можно сделать однозначный вывод о том, что находящиеся в межзеренных областях аморфные фрагменты обладают худшей электрической проводимостью.
СТМ-измерения на образцах, подвергнутых длительному литированию / делитированию (рис. 205), однозначно свидетельствуют об укрупнении частиц, составляющих пленку. Туннельно-спектроскопические измерения на образцах после циклирования потенциала в растворе электролита свидетельствуют о сохранении полупроводникового характера проводимости и, одновременно, о резком снижении сопротивления пленки. Это, наряду с данными рентгенофазового анализа, свидетельствует о том, что диоксид олова остается одним из компонентов пленки, а также об изменении характера его допирования (с помощью РФА в составе пленки была обнаружена фаза TiO2).
239
|
|
|
|
|
|
60 |
|
|
|
∆нм,H |
10 |
|
|
|
а |
|
|
|
б |
|
|
|
|
∆нм,H |
40 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
-2 |
0 |
2 |
|
|
-2 |
0 |
|
2 |
|
|
|||
|
|
Uтун, В |
|
|
|
|
Uтун, В |
|
|
|
|
|
300 |
|
|
|
|
в |
|
|
|
нм |
200 |
|
|
|
|
|
|
|
|
∆H, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
100 |
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
-2 |
0 |
|
2 |
|
|
|
|
|
|
|
Uтун, В |
|
|
|
|
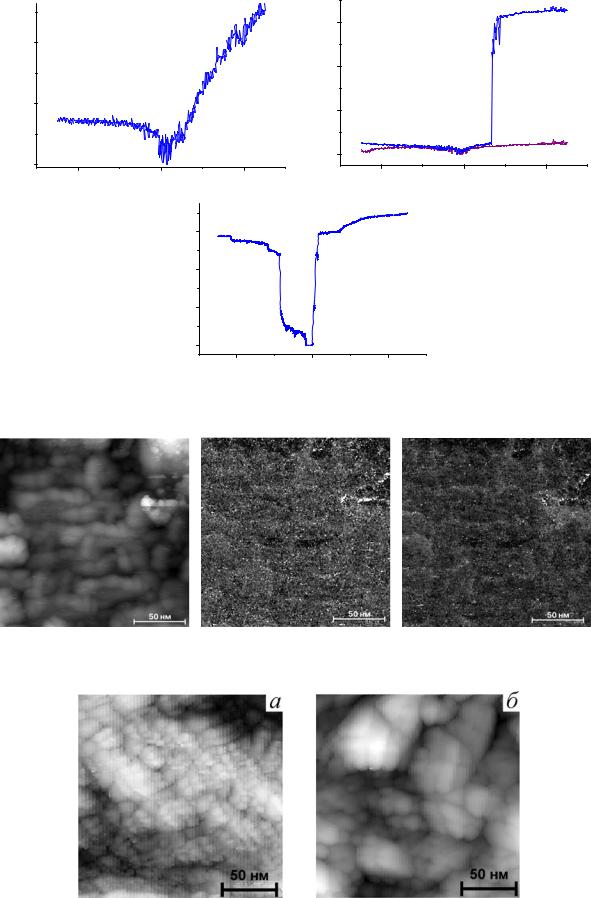
Рис. 203. Вольтвысотные спектры оксидных пленок SnO2, допированных 0% (а), 10% (б), 20 мол.% TiO2 (в).
а |
б |
в |
Рис. 204. Результаты сканирования в дифференциальном режиме пленки SnO2, допированной 10 мол% TiO2. а — топография поверхности, б — величина |dI/dU|, в — сдвиг фаз между током и напряжением.
Рис. 205. Типичные СТМ-изображения наногетерогенных оксидных пленок SnO2, допированных 10 мол.% TiO2, до (а) и после (б) электрохимического литирования/делитирования в растворе LiN(CF3SO2)2 в диоксолане (38 циклов).
240
