
Лекция_1_МКТ
.doc
ОСНОВЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ (МКТ)
ОСНОВНЫЕ ПОНЯТИЯ
-
Плотность
 вещества,
вещества,
![]() ,
,
![]() . (1)
. (1)
![]() -
масса вещества в объеме
-
масса вещества в объеме
![]() .
.
-
Концентрация
 молекул,
молекул,
![]() ,
,
![]() м-3
. (2)
м-3
. (2)
![]() -число
молекул в объеме
-число
молекул в объеме
![]() .
.
-
Давление
![]() ,
,
![]() =Па
(Паскаль). (3)
=Па
(Паскаль). (3)
![]() -
сила, действующая на площадку
-
сила, действующая на площадку
![]() ,
перпендикулярную направлению силы.
,
перпендикулярную направлению силы.
1мм.рт.ст.=133 Па.
-
Количество молекул (атомов) вещества, содержащее столько же молекул, сколько их содержит 12 грамм изотопа углерода
 ,
называется молем вещества.
,
называется молем вещества.
Один моль вещества
содержит
![]() молекул. Это число называется числом
Авогадро
молекул. Это число называется числом
Авогадро
![]() .
Масса моля вещества называется молярной
массой
.
Масса моля вещества называется молярной
массой
![]() .
Молярная масса определяется по таблице
Менделеева, например для воды (
.
Молярная масса определяется по таблице
Менделеева, например для воды (![]() ):
):
![]() г/моль=
г/моль=![]() кг/моль
кг/моль
Количество молей (количество вещества)
![]() ,
,
![]() моль.
(4)
моль.
(4)
-
Масса одной молекулы
 .
Плотность
.
Плотность
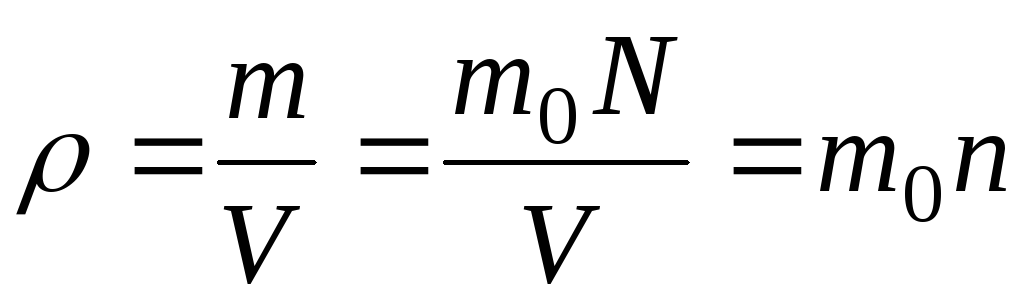 .
.
-
Температура
 по шкале Кельвина связана с температурой
по шкале Кельвина связана с температурой
 по Цельсию:
по Цельсию:
![]() =
=![]() +273
K .
+273
K .
ИДЕАЛЬНЫЙ ГАЗ
Идеальным называется газ, удовлетворяющий трем условиям:
-
можно пренебречь взаимодействием молекул;
-
можно пренебречь собственным объемом молекул;
-
соударения молекул можно рассматривать как абсолютно упругие.
Азот N2, кислород O2 , водород H2, пары воды H2O и другие газы при условиях, близких к нормальным, удовлетворяют условиям идеальности.
Нормальные условия (н.у.):
температура t=0°С и давление p=760 мм.рт.ст.=101,3 кПа.
Законы идеального газа:
-
Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона)
![]() ,
(5)
,
(5)
![]() -давление
газа,
-давление
газа,
![]() -
его объем,
-
его объем,
![]() – масса газа,
– масса газа,
![]() -
молярная масса,
-
молярная масса,
![]() =8,31
Дж/(моль·К) – газовая постоянная,
=8,31
Дж/(моль·К) – газовая постоянная,
![]() – температура в Кельвинах.
– температура в Кельвинах.
Вводя постоянную Больцмана
![]() =1,38·10-23
Дж/K,
=1,38·10-23
Дж/K,
уравнение состояния также записывают в другом виде. Т.к.
![]() =
=![]() =
=![]() ,
то
,
то
![]() ,
(6)
,
(6)
![]() - концентрация
молекул.
- концентрация
молекул.
-
Основное уравнение МКТ (связь давления с энергией поступательного движения молекулы).
![]() ,
(7)
,
(7)
![]() - средняя кинетическая
энергия поступательного движения
молекул. Поступательное – это движение
молекулы без учета ее вращения и колебаний
атомов около положения равновесия.
- средняя кинетическая
энергия поступательного движения
молекул. Поступательное – это движение
молекулы без учета ее вращения и колебаний
атомов около положения равновесия.
![]() - средняя квадратичная
скорость молекул,
- средняя квадратичная
скорость молекул,
![]() .
.
Следствия из основного уравнения МКТ.
-
Перепишем уравнения (7) и (6) :
![]() и
и
![]() .
.
Приравняем правые части. Получаем связь средней кинетической энергии поступательного движения молекул с температурой:
![]() .
(8)
.
(8)
-
Сравнивая уравнение (8) и выражение
 ,
,
получаем, что средняя квадратичная скорость молекул
![]() .
.
Масса одной молекулы
![]() , а
, а
![]() .
.
Тогда
![]() можно записать как
можно записать как
![]() .
.
-
Закон Дальтона: давление
 смеси газов равно сумме парциальных
давлений
смеси газов равно сумме парциальных
давлений
![]() .
(8)
.
(8)
Парциальное давление – это давление, которое оказывал бы один газ из смеси, если бы занимал весь объем сосуда.
Распределение Максвелла молекул по скоростям
Если
![]() - число молекул в каком–либо объеме
газа, а
- число молекул в каком–либо объеме
газа, а
![]() - число молекул со скоростями от
- число молекул со скоростями от
![]() до (
до (![]() +
+![]() ),
то
),
то
![]() - относительное
число молекул из данного объема,
движущихся со скоростью
- относительное
число молекул из данного объема,
движущихся со скоростью
![]() .
.
Вид функции
![]() был установлен Д.Максвеллом,
был установлен Д.Максвеллом,
![]() (13)
(13)
и она носит название «функция Максвелла» (или функция распределения молекул по скоростям). График функции для разных температур представлен на рис.1.
 Рисунок
1.
Рисунок
1.
Свойства функции Максвелла:
-
Площадь, ограниченная функцией Максвелла
 и горизонтальной осью
и горизонтальной осью
 ,
равна единице:
,
равна единице:
![]()
![]() =
=
![]() =
= = 1 .
= 1 .
-
Наиболее вероятная скорость молекул газа.
Наиболее вероятная
скорость
![]() – это скорость, с которой движется
наибольшее число молекул при данной
температуре. Этой скорости соответствует
максимальное значение функции Максвелла.
Значит, производная от
– это скорость, с которой движется
наибольшее число молекул при данной
температуре. Этой скорости соответствует
максимальное значение функции Максвелла.
Значит, производная от
![]() по
по
![]() ,
при
,
при
![]() =
=![]() ,
должна быть равна нулю, т.е.
,
должна быть равна нулю, т.е.
![]() =
0 при
=
0 при
![]() =
=![]() .
.
![]() ,
тогда
,
тогда
![]() =
=
![]()
![]() =
=
=
![]() .
.
Производная равна
нулю, если
![]() =
0. Отсюда получаем значение наиболее
вероятной скорости
=
0. Отсюда получаем значение наиболее
вероятной скорости
![]() , или ,
т.к.
, или ,
т.к.
![]() и
и
![]() ,
то
,
то
![]() .
.
-
Средняя арифметическая скорость
 молекул.
молекул.
![]() =
=
![]() =
=![]() , (14)
, (14)
где
![]() - число молекул, движущихся со скоростью
- число молекул, движущихся со скоростью
![]() ,
а
,
а
![]() - полное число молекул.
- полное число молекул.
Поскольку величина скорости распределена непрерывно, то сумма в выражении (14) переходит в интеграл:
![]() , или
, или
![]()
![]()
Таким образом,
![]() определяется
через функцию Максвелла
определяется
через функцию Максвелла![]() .
В результате интегрирования получено,
что
.
В результате интегрирования получено,
что
![]() , или
, или
![]() . (15)
. (15)
-
Число молекул со скоростями от
 до
до
 .
.
Рассмотрим интеграл
 =
=
 =
=
![]() =
=
![]() .
.
Т.е. относительное
число молекул со скоростями от
![]() до
до
![]() численно равно площади заштрихованного
участка на рисунке 1 и вычисляется через
функцию Максвелла,
численно равно площади заштрихованного
участка на рисунке 1 и вычисляется через
функцию Максвелла,
 .
.
Эффективный диаметр и средняя длина свободного пробега молекулы
Эффективный
диаметр
![]() молекулы – минимальное расстояние, на
которое сближаются молекулы газа при
соударениях.
молекулы – минимальное расстояние, на
которое сближаются молекулы газа при
соударениях.
Средняя длина
свободного пробега
![]() молекулы - среднее расстояние, которое
пролетает молекула между двумя
последовательными соударениями,
молекулы - среднее расстояние, которое
пролетает молекула между двумя
последовательными соударениями,
![]() ,
(16)
,
(16)
![]() -
концентрация молекул.
-
концентрация молекул.
Среднее число
![]()
![]() столкновений молекул за время
столкновений молекул за время
![]() ,
,
![]() =
=
![]() =
=
![]() .
.
Число соударений в единицу времени,
![]() .
(17)
.
(17)
ЯВЛЕНИЯ ПЕРЕНОСА.
К явлениям переноса относятся диффузия, теплопроводность и внутреннее трение (вязкость). Эти явления обусловлены хаотичным тепловым движением молекул и являются необратимыми.
Диффузия –
самопроизвольное перемешивание частиц
соприкасающихся веществ, или одного
вещества, при котором выравнивается
плотность
![]() .
Уравнение диффузии (уравнение Фика)
.
Уравнение диффузии (уравнение Фика)
![]() ,
(18)
,
(18)
![]() - масса вещества,
которая переносится через площадку
- масса вещества,
которая переносится через площадку
![]() за время
за время
![]() в направлении x,
перпендикулярном площадке.
в направлении x,
перпендикулярном площадке.
![]() -
коэффициент диффузии, зависящий от рода
вещества и температуры,
-
коэффициент диффузии, зависящий от рода
вещества и температуры,
![]() - градиент плотности. Знак минус в
уравнении отражает то, что перенос массы
происходит в направлении меньшей
плотности
- градиент плотности. Знак минус в
уравнении отражает то, что перенос массы
происходит в направлении меньшей
плотности
![]() .
.
Теплопроводность
– перенос теплоты
![]() в результате соударений молекул и
передачи ими друг другу своей кинетической
энергии. Уравнение теплопроводности
(уравнение Фурье)
в результате соударений молекул и
передачи ими друг другу своей кинетической
энергии. Уравнение теплопроводности
(уравнение Фурье)
![]() ,
(19)
,
(19)
![]() – теплота, которая
переносится через площадку
– теплота, которая
переносится через площадку
![]() за время
за время
![]() в направлении x,
перпендикулярном площадке;
в направлении x,
перпендикулярном площадке;
![]() - скорость изменения температуры в этом
направлении;
- скорость изменения температуры в этом
направлении;
![]() - коэффициент теплопроводности материала.
Перенос тепла происходит в область с
меньшей температурой.
- коэффициент теплопроводности материала.
Перенос тепла происходит в область с
меньшей температурой.
Внутреннее трение
(вязкость) – сцепление между собой
слоев жидкости или газа. При этом слои,
движущиеся с разными скоростями, за
счет соударений молекул передают друг
другу импульс
![]() ,
что приводит к выравниванию скорости
,
что приводит к выравниванию скорости
![]() движения слоев. Сцепление между собой
слоев приводит к появлению сил трения
между ними. За счет сил трения быстро
движущийся слой замедляет свое движение,
а медленно движущийся – убыстряет.
движения слоев. Сцепление между собой
слоев приводит к появлению сил трения
между ними. За счет сил трения быстро
движущийся слой замедляет свое движение,
а медленно движущийся – убыстряет.
Уравнение внутреннего трения:
![]() ,
(20)
,
(20)
![]() -
импульс, который переносится молекулами
через площадку
-
импульс, который переносится молекулами
через площадку
![]() за время
за время
![]() в направлении
в направлении
![]() ,
перпендикулярном скорости движения
слоев.
,
перпендикулярном скорости движения
слоев.
![]() -
коэффициент вязкости, зависящий от рода
жидкости или газа и их температуры.
-
коэффициент вязкости, зависящий от рода
жидкости или газа и их температуры.
Т.к.
![]() ,
то сила трения между слоями жидкости
или газа, действующая на площадь
,
то сила трения между слоями жидкости
или газа, действующая на площадь
![]() поверхности, равна
поверхности, равна
![]() .
(21)
.
(21)
Если плотность
потока массы
![]() ,
или плотность теплового потока
,
или плотность теплового потока![]() ,
или плотность потока импульса
,
или плотность потока импульса
![]() является величиной постоянной, то в
уравнениях диффузии, теплопроводности
и внутреннего трения можно перейти от
бесконечно малых изменений величин к
конечным разностям и эти уравнения
записать в виде
является величиной постоянной, то в
уравнениях диффузии, теплопроводности
и внутреннего трения можно перейти от
бесконечно малых изменений величин к
конечным разностям и эти уравнения
записать в виде
![]() ,
,
![]() ,
,
![]() .
.
Для твердых тел и
жидкостей коэффициенты
![]() определяются экспериментально, для
идеальных газов
определяются экспериментально, для
идеальных газов
![]() ,
,
![]() ,
,
![]() .
.
![]() - удельная
теплоемкость газа при постоянном объеме
- удельная
теплоемкость газа при постоянном объеме
![]() .
.
