
Проблемы_биокатализа_и_ферменты_Лекция_3_PDF
.pdf
СТРОЕНИЕ ФЕРМЕНТОВ |
СМ. АНИМАЦИИ НА СТР. |
|
КАЛИНИНОЙ! |
||
|
|
|
|
|
|
4. |
МНОЖЕСТВЕННЫЕ ФОРМЫ ФЕРМЕНТОВ |
|
|
|
|
А. ГЕТЕРОФЕРМЕНТЫ РАЗНЫХ БИОЛОГИЧЕСКИХ ВИДОВ
Б. ОРГАНОСПЕЦИФИЧНЫЕ (В ОДНОМ ОРГАНЕ), ОТЛИЧАЮТСЯ КОНФОРМАЦИЕЙ (ИЗОФОРМЫ)
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
21 |

СТРОЕНИЕ ФЕРМЕНТОВ |
СМ. АНИМАЦИИ НА СТР. |
|
КАЛИНИНОЙ! |
||
|
|
|
|
|
|
5. |
ИЗОФЕРМЕНТЫ |
|
|
|
|
- генетически детерминированные ферменты, катализирующие одну и ту же химическую реакцию, но с разной эффективностью:
отличаются физико-химическими свойствами (разные АМК)!
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
22 |

СТРОЕНИЕ ФЕРМЕНТОВ |
СМ. АНИМАЦИИ НА СТР. |
КАЛИНИНОЙ! |
|
|
|
ПРИМЕР: ЛАКТАТДЕГИДРОГЕНАЗА (ЛДГ)
ТЕТРАМЕР – ПОСТРОЕН ИЗ 4-Х СУБЪЕДИНИЦ 2-Х ТИПОВ:
HEART |
|
MUSCLE |
|
|
|
5 РАЗНЫХ ИЗОФЕРМЕНТОВ: HHHH, HHHM, HHMM, HMMM, MMMM:
|
I |
|
II |
|
III |
|
|
IV |
|
V |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
ЛДГ1 |
|
|
ЛДГ2 |
|
|
ЛДГ3 |
|
|
ЛДГ4 |
|
|
ЛДГ5 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СЕРДЕЧНЫЙ ТИП |
|
|
|
|
ПЕЧЕНОЧНЫЙ ТИП |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЛДГ |
|
|
|
|
|
|
|
|
|
|
|
ЛАКТАТ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПИРУВАТ |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
23 |

СТРОЕНИЕ ФЕРМЕНТОВ |
СМ. АНИМАЦИИ НА СТР. |
КАЛИНИНОЙ! |
|
|
|
6. |
МУЛЬТИФЕРМЕНТНЫЕ КОМПЛЕКСЫ |
|
ФУНКЦИОНАЛЬНО-СВЯЗАННЫХ ФЕРМЕНТОВ |
||
|
||
|
|
Например: пируватдегидрогеназный комплекс ферментов и
синтаза высших жирных кислот
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
24 |

СТРОЕНИЕ ФЕРМЕНТОВ |
СМ. АНИМАЦИИ НА СТР. |
КАЛИНИНОЙ! |
|
|
|
Ферменты, активность которых лимитирует всю цепь последовательных метаболических реакций,
часто являются аллостерическими
и считаются ключевыми (их надо знать)!
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
25 |
 ФЕРМЕНТАТИВНАЯ КИНЕТИКА
ФЕРМЕНТАТИВНАЯ КИНЕТИКА
ОПЕРЕДЕЛЕНИЕ СКОРОСТИ ДЕЙСТВИЯ ФЕРМЕНТОВ
ʋ = |
|
dS |
= |
|
|
dP |
|
||
|
|
|
|
|
|
|
|
||
- dτ |
|
|
|
|
|
||||
|
|
dτ |
|
||||||
|
|
|
|
|
|||||
|
CS |
|
|
|
CP |
|
|||
|
|
|
|
|
|
|
|
|
|
Изменение концентрации субстрата (S) и продукта (P)
Изменение времени
Уменьшение |
Увеличение |
концентрации |
концентрации |
субстрата |
продукта |
|
|
Всегда надо осознавать, что мы измеряем на самом деле? Внутри клетки можно измерить только количество фермента (с антителами или по мРНК), но не его активность.
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
26 |

 ЗАВИСИМОСТЬ ОТ КОНФЕНТРАЦИИ СУБСТРАТА
ЗАВИСИМОСТЬ ОТ КОНФЕНТРАЦИИ СУБСТРАТА
Изменение скорости многих ферментов, особенно катализирующх простые реакции, подчиняются уравнению Михаэлиса-Ментен При определенных ограничениях: CS>>CE:
При насыщении фермента субстратом (характеризует эффективность катализа).
ʋ= Vmax. CS
KM + CS
Константа Михаэлиса характеризует сродство фермента к субстрату: чем выше KM, тем менее эффективно превращение субстрата, и наоборот!
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
27 |
 АНАЛИЗ УРАВНЕНИЯ МИХАЭЛИСА-МЕНТЕН:
АНАЛИЗ УРАВНЕНИЯ МИХАЭЛИСА-МЕНТЕН:
ʋ= Vmax. CS
KM + CS
1.Если CS >> KM, то ʋ  Vmax (насыщение фермента субстратом)
Vmax (насыщение фермента субстратом)
|
|
|
V |
. C |
S |
|
2. Если CS = KM, то |
ʋ |
= |
max |
|
= ½ Vmax |
|
|
|
|
CS + CS
т. е. КМ – это такая концентрация субстрата (моль/л), при которой
скорость реакции составляет половину от максимальной (½ Vmax)
|
|
V |
. C |
S |
= k . C |
|
|
3. Если CS << KM, то |
ʋ = |
max |
|
|
- это прямая |
||
|
|
|
S |
||||
KM |
|
||||||
|
|
|
|
|
|||
|
|
|
|
|
|
||
пропорциональная зависимость (начальная скорость реакции)
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
28 |
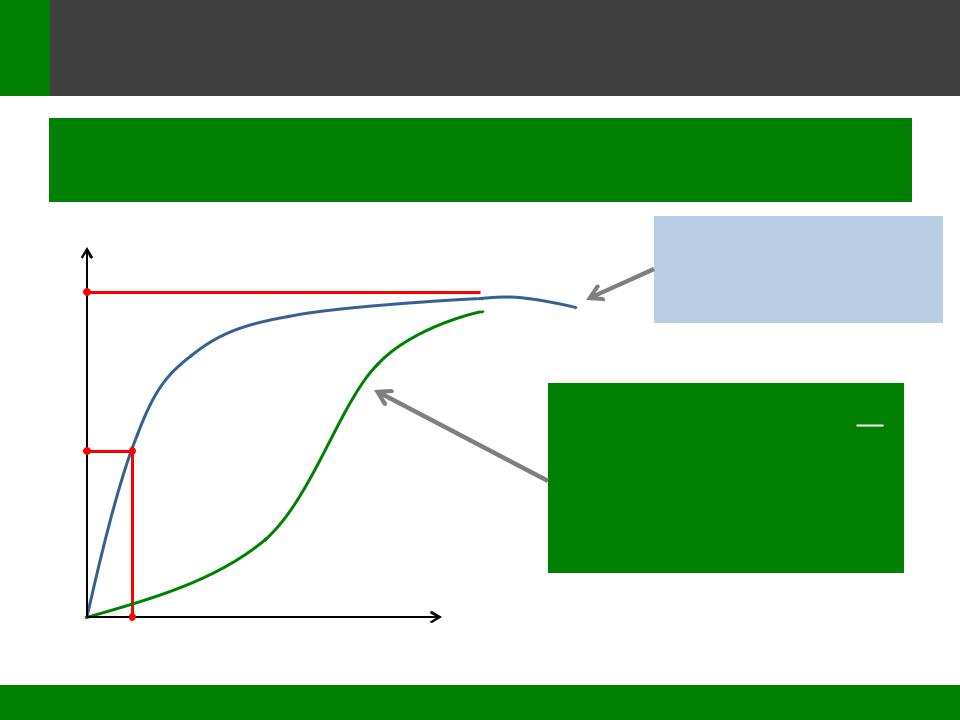
ГРАФИЧЕСКОЕ ИЗОБРАЖЕНИЕ УРАВНЕНИЯ МИХАЭЛИСА-МЕНТЕН
Графическое выражение уравнения Михаэлиса – Ментен
– полуветвь гиперболы.
ʋ, моль/с
Vmax
½ Vmax
0 KM
Возможное ингибирование высокими концентрациями субстрата
Аллостерические ферменты не подчиняются кинетике Михаэлиса – Ментен и описываются
S – образной кривой (сигмоидальной).
CS, моль/л
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
29 |

 ГРАФИК ДВОЙНЫХ ОБРАТНЫХ ВЕЛИЧИН
ГРАФИК ДВОЙНЫХ ОБРАТНЫХ ВЕЛИЧИН
ДЛЯ УПРОЩЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ОПРЕДЕЛЕНИЯ Vmax и KM ПРЕДЛОЖЕНО МНОГО СПОСОБОВ. ПРОСТЕЙШИЙ ИЗ НИХ: ГРАФИК ДВОЙНЫХ ОБРАТНЫХ ВЕЛИЧИН ЛАЙНУИВЕРА - БЭРКА
1/ʋ
|
KM + CS |
||||
1/ʋ = |
|
|
|
|
|
V |
max |
. C |
S |
||
|
|||||
|
|
|
|||
 1/Vmax
1/Vmax
|
|
0 |
1/CS |
- |
1 |
|
|
|
|
||
|
K |
|
|
|
M |
|
|
ФЕРМЕНТЫ И ПРОБЛЕМЫ БИОКАТАЛИЗА. ЧЕРНОВ Н. Н. 2013. |
30 |
