
- •Методические рекомендации для студентов
- •1. Тема: «Свойства буферных растворов. Определение буферной емкости».
- •3. Цели занятия.
- •3.2. Конкретные цели и задачи.
- •4. Вопросы, изученные на предшествующих дисциплинах и необходимые для освоения темы.
- •5. Задания для самостоятельной подготовки к лабораторному занятию:
- •7. Ориентировочная основа действия (одд) для проведения самостоятельной работы студентов в учебное время.
- •8. Задания для контроля уровня сфомированности компетенций в учебное время.
- •9. Учебно-материальнное обеспечение:
- •10. Материальное обеспечение:
7. Ориентировочная основа действия (одд) для проведения самостоятельной работы студентов в учебное время.
Приборы и реактивы. Измерительный прибор Кобра 3, рН-метр, комбинированный рН-электрод, магнитная мешалка, магнитный брусок – ротор, бюретки на 50 мл 4 шт., конические колбы для титрования на 100 мл 10 шт., воронка 4 шт., пипетка на 2 мл, пипетка на 1 мл, пипеттор. Растворы: уксусной кислоты с С(1/1СН3СООН)=0,1 моль/л и С(1/1СН3СООН)=0,3 моль/л, ацетата натрия с С(1/1СН3СООNa)=0,1 моль/л и С(1/1СН3СООNa)=0,3 моль/л, раствор щелочи с С(1/1NaOH)=0,5 моль/л.
Методика выполнения эксперимента.
Первая группа. В пять конических колб для титрования внести при помощи бюреток растворы уксусной кислоты с С(1/1СН3СООН)=0,1 моль/л, и раствор ацетата натрия с С(1/1СН3СООNa)=0,1 моль/л в количествах, указанных в таблице.
Таблица 1.
|
№ раствора |
Состав буферной смеси |
pH раствора расчетный |
pH раствора исх. |
pH раствора кон. | |
|
V, см³ CH3COOH |
V, см³ CH3COONa | ||||
|
1 2 3 4 5 |
44 40 25 10 6 |
6 10 25 40 44 |
|
|
|
Перенести содержимое колбы № 1 в стакан на 150 мл. Поставить стакан на магнитную мешалку, опустить в раствор ротор, установить среднюю скорость перемешивания, погрузить рН-электрод и измерить рН данного раствора. При помощи пипетки добавить 1 мл раствора щелочи с С(1/1NaOH)=0,5 моль/л, подождать 1 минуту затем определить рН.
По вышеописанной методике определить рН исходных растворов и рН после прибавления 1 мл щелочи с С(1/1NaOH)=0,5 моль/л.
Вторая группа. В пять конических колб для титрования внести при помощи бюреток растворы уксусной кислоты с С(1/1СН3СООН)=0,3 моль/л, и раствор ацетата натрия с С(1/1СН3СООNa)=0,3 моль/л в количествах, указанных в таблице.
Таблица.
|
№ раствора |
Состав буферной смеси |
pH раствора расчетный |
pHисх. раствора |
pHкон. раствора |
| |
|
V, см³ CH3COOH |
V, см³ CH3COONa | |||||
|
1 2 3 4 5 |
44 40 25 10 6 |
6 10 25 40 44 |
|
|
|
|
Перенести содержимое колбы № 1 в стакан на 150 мл. Поставить стакан на магнитную мешалку, опустить в раствор ротор, установить среднюю скорость перемешивания, погрузить рН-электрод и измерить рН данного раствора. При помощи пипетки добавить 2 мл раствора щелочи с С(1/1NaOH)=0,5 моль/л, подождать 1 минуту затем определить рН.
По вышеописанной методике определить рН исходных растворов и рН после прибавления 2 мл щелочи с С(1/1NaOH)=0,5 моль/л.
Обработка результатов эксперимента.
1.
Расчёт теоретического значения pH
буферных растворов по формуле:
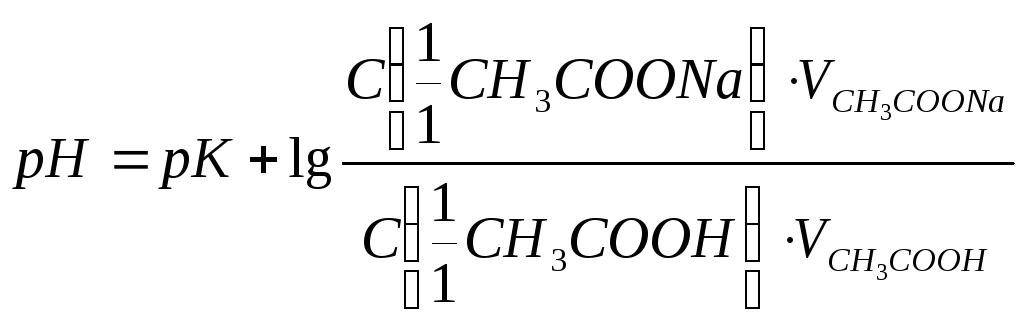 ,
где
,
где
![]() и
и![]() – молярные концентрации эквивалента
раствора ацетата натрия (сопр. основание)
и уксусной кислоты. Сравнить теоретическое
и практическое значениеpH.
– молярные концентрации эквивалента
раствора ацетата натрия (сопр. основание)
и уксусной кислоты. Сравнить теоретическое
и практическое значениеpH.
2. Расчет буферной емкости по формуле:
B=∆CB / ∆pH, где
∆CB = (C(1/1 NaOH) ∙ VNaOH )/ Vбуф.р-ра ;
∆рН = рНисх. – рНкон.
3. Построить график зависимости буферной емкости от рН среды на миллиметровой бумаге.
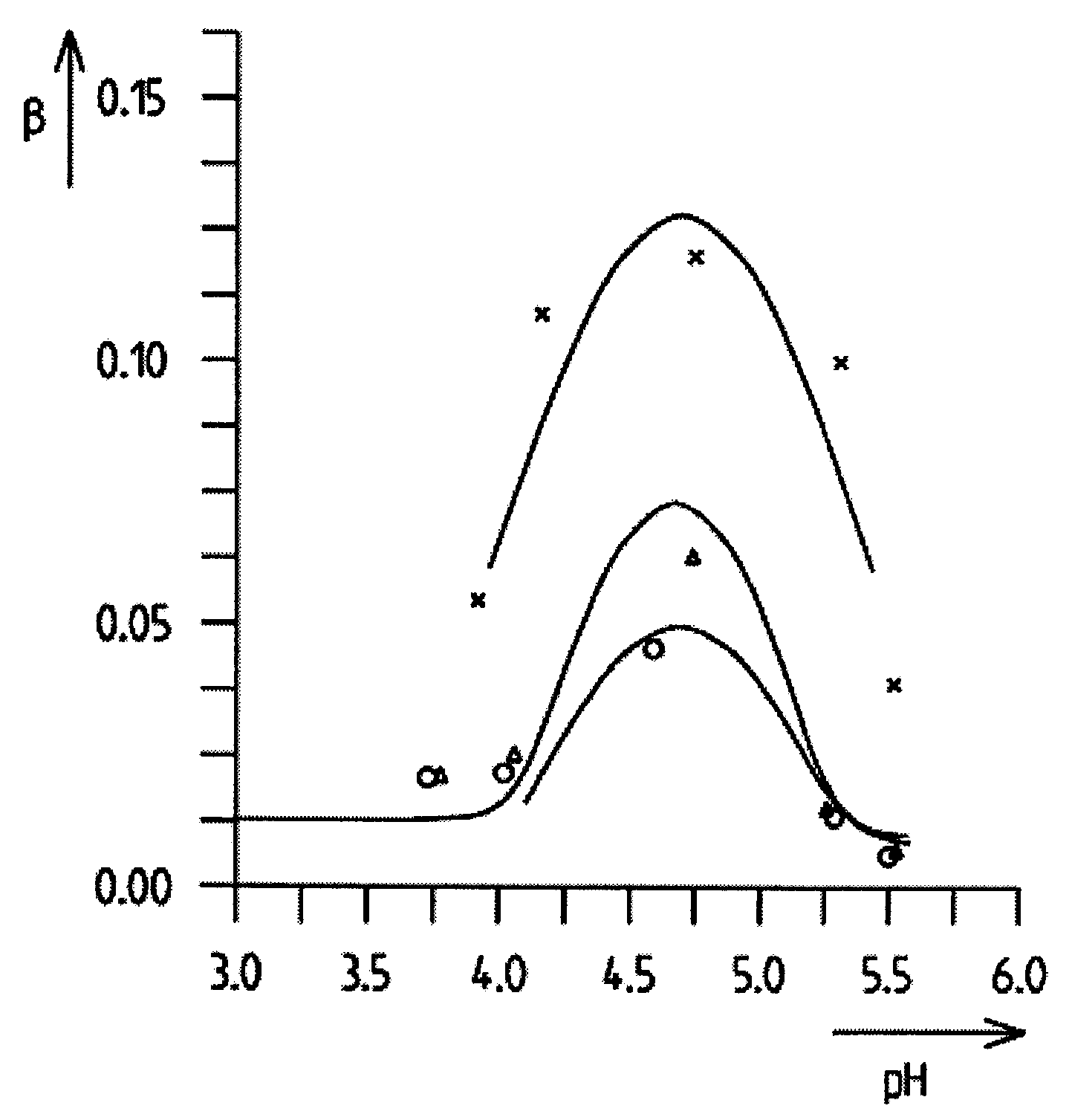
4. По графику определить зону буферного действия.
