
Lektsia_14_Absorbtsia_Vosstanovlen_Lektsia_1
.doc
Лекция №14
Лекция №1. Абсорбция.
Поглощение газов или паров из газовых или паровых смесей жидким поглотителем.
Процесс абсорбции отличает избирательность и обратимость.
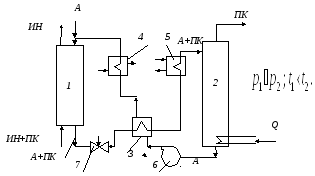
Рис.1. Схема сочетания процессов абсорбции и десорбции: 1 – абсорбер; 2 – десорбер; 3 – теплообменник; 4 – холодильник; 5 – подогреватель; насос; 6 – дроссельный вентиль; «ИН+ПК» - исходная газовая смесь (инерт и + поглощаемый компонент); «А+ПК» - абсорбент + поглощаемый компонент; Q – подвод теплоты.
Требования к абсорбенту.
-
селективность;
-
нелетучесть;
-
дешевизна;
-
нетоксичность;
-
огневзрывобезопасность.
Применение процесса абсорбции.
а) получение целевых продуктов (абсорбция HCL водой в производстве соляной кислоты)
б) выделение ценных компонентов газовых смесей (ацетилена из газов крекинга метана);
в) удаление вредных примесей из газовых смесей (CO, CO2 из азотоводородной смеси при синтезе аммиака).
Физическая абсорбция. Хемосорбция.
Поглощение газа за счет его растворения в абсорбенте – ф. а.
Поглощение газа в результате его химического взаимодействия с абсорбентом. – х.а.
Равновесие в процессах абсорбции.
Равновесие может быть представлено в
форме закона Генри
![]() – закона растворимости газа в жидкости
(уравнение прямой в прямоугольных
координатах
– закона растворимости газа в жидкости
(уравнение прямой в прямоугольных
координатах
![]()
![]() -
тангенс угла наклона), где
-
тангенс угла наклона), где
![]() – коэффициент распределения, есть
отношение Е (константы Генри) к Р (общего
давления газовой фазы), а
– коэффициент распределения, есть
отношение Е (константы Генри) к Р (общего
давления газовой фазы), а
![]() и
и
![]() - равновесные концентрации; или
в форме криволинейной зависимости в
прямоугольных координатах , если
- равновесные концентрации; или
в форме криволинейной зависимости в
прямоугольных координатах , если
![]() – переменная величина (зависит от уровня
концентраций (см. рис.). Закон Генри
«работает» в углу диаграммы фазового
равновесия (область малых концентраций
поглощаемого компонента (ПК).
– переменная величина (зависит от уровня
концентраций (см. рис.). Закон Генри
«работает» в углу диаграммы фазового
равновесия (область малых концентраций
поглощаемого компонента (ПК).

![]()
Влияние температуры и давления на равновесие при абсорбции.
В соответствии с принципом Ле - Шателье при возрастании температуры уменьшается концентрация ПК в жидкой фазе (см. рис.). При возрастании давления, напротив, увеличивается концентрация ПК в жидкой фазе (см. рис.).
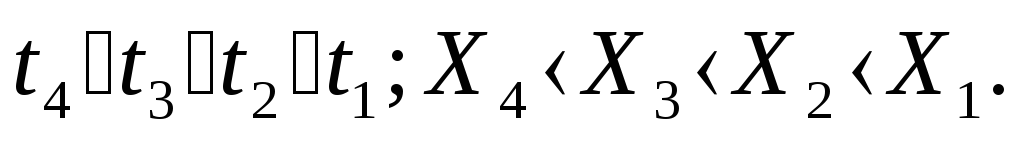

![]()
![]()
![]()
![]()
Рис. Диаграмма фазового равновесия газ
– жидкость. Влияние температуры на
состояние равновесия систем газ –
жидкость.

Проведение процесса абсорбции осуществляют при повышенном давлении и пониженной температуре. Реализация процесса десорбции осуществляется при пониженном давлении и повышенной температуре системы.
Способы проведения процесса абсорбции.
Прямоток (см. раздел «Некоторые общие вопросы процессов массообмена»), противоток (см. там же), противоток с рециркуляцией абсорбента.
Абсорбция с рециркуляцией абсорбента.
К такому способу абсорбции прибегают тогда, когда: стоимость абсорбента велика, и желательно сократить расход свежего абсорбента (в задачах проектирования); требуется увеличить плотность орошения насадки при сохранении расхода свежего абсорбента (в задачах эксплуатации).
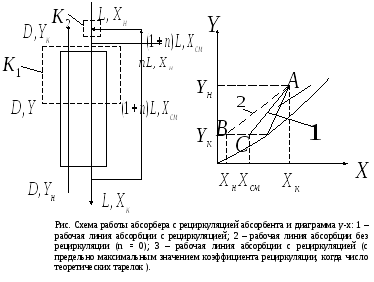 Схема
работы абсорбера с рециркуляцией
абсорбента показана на рисунке.
Схема
работы абсорбера с рециркуляцией
абсорбента показана на рисунке.
![]()
Коэффициент рециркуляции показывает: какая масса отработанного абсорбента возвращается на единицу массы свежего абсорбента, т.е. размерность этой величины есть кг А отраб./кг А свежего.
Для вывода уравнения рабочей линии процесса абсорбции с рециркуляцией абсорбента составляют уравнение материального баланса для контура К1 по ПК
![]() ;
откуда
;
откуда
![]() .
(1.1)
.
(1.1)
Уравнение (1.1) – уравнение рабочей линии процесса абсорбции с рециркуляцией абсорбента.
Для установления связи между составами жидкой фазы на входе в абсорбер составляют уравнение материального баланса для контура К1 по ПК
![]() ,
откуда, при известных значениях
,
откуда, при известных значениях
![]()
![]() и
и![]() ,
можно определить состав смеси
,
можно определить состав смеси
![]() . (2.1)
. (2.1)
При n = 0 уравнение (1.1) с учетом уравнения (2.1) трансформируется в уравнение р.л. для противоточного процесса абсорбции без рециркуляции
![]() .
.
Коэффициент рециркуляции имеет следующие
предельные значения:
![]() - для абсорбции без рециркуляции (на
рисунке – р.л. 2);
- для абсорбции без рециркуляции (на
рисунке – р.л. 2);
![]() - при предельном положении рабочей линии
процесса абсорбции с рециркуляцией (на
рисунке – р.л. 3), когда
- при предельном положении рабочей линии
процесса абсорбции с рециркуляцией (на
рисунке – р.л. 3), когда![]() .
Действительная рабочая линия построена
для
.
Действительная рабочая линия построена
для
![]() и проходит через точки А(
и проходит через точки А(![]() )
и С(
)
и С(![]() ).
).
Зная положение действительной рабочей
линии, определяют число теоретических
тарелок или число единиц переноса массы
и далее по «списку». Заметим, что
минимальное число теоретических тарелок
получают при
![]() ,
максимальное – при
,
максимальное – при
![]() .
.
