
- •Аннотация
- •1. Расчёт горения топлива.
- •2. Расчёт нагрева металла.
- •2.1 Расчёт основных размеров рабочей камеры, параметров теплообмена и времени нагрева.
- •2.2 Методическая зона.
- •2.4 Томильная зона.
- •2.5 Расчёт длины рабочего пода.
- •3. Тепловой баланс методической печи.
- •Температура, оС
- •Толщина стенки, мм
- •4. Выбор горелочных устройств
- •5. Расчет газового, воздушного и дымового трактов нагревательных печей
- •5.1 Определение размеров газопровода
- •5.2 Расчет газового тракта
- •5.3 Расчёт дымового тракта
- •Библиографический список.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
ГОУ ВПО « ЛИПЕЦКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Кафедра теплофизики
КУРСОВАЯ РАБОТА
РАСЧЕТНО-ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
по теплотехнике
на тему: «Расчёт металлургической печи»
Студент ______________________ Илюшин М.В.
Группы ОД-07-2
Руководитель _______________________ Карамышева Е.П.
Липецк-2011
Аннотация
С. . Ил. 8. Табл. 4. Библиогр.: 9 назв.
В данной работе рассчитывается методическая печь с двусторонним обогревом, предназначенная для нагрева изделий из углеродистой стали Ст2 размерами 260´1280´9100. Производительность рассчитываемой печи составляет 160 т/ч. Печь обогревается продуктами сгорания смеси коксо-доменного газа.
СОДЕРЖАНИЕ
Введение…………………………………………………………………………..
Расчёт горения топлива………………………………………………………….
Расчёт нагрева металла……………………………………………………..…..
Расчёт основных размеров рабочей камеры и
параметров внешнего теплообмена…………………………………….……..
1-я ступень нагрева – методическая зона ……………………………..….
2.3. 2-я ступень нагрева – сварочная зона …………………………….………
2.4. 3-я ступень нагрева – томильная зона…………………………………….
2.5. Расчёт длины и напряжённости рабочего пода.……………………...…..
Тепловой баланс методической печи….……………………………………….
Выбор горелочных устройств …….……………………………………………
Расчет газового, воздушного и дымового
трактов нагревательных печей………………...…………………………….............
Определение размеров газо- и воздухопроводов ……………..…..……..
Расчет газового тракта……………………………………………………
Расчет дымового тракта……………………………………………………
6. Расчет дымовой трубы…………………………………………………
Библиографический список….………….…….……………………………………
1. Расчёт горения топлива.
В методических печах обычно применяют горелки типа “труба в трубе” без предварительного смешения газа и воздуха, поэтому принимаем коэффициент расхода воздуха a=1,1.
Из справочной литературы выписываем состав сухих коксового и доменного газов [1. стр17] в процентах.
|
Состав |
СО2 |
СО |
СH4 |
C2H4 |
H2 |
N2 |
О2 |
Всего |
|
Коксовый |
2,3 |
5,4 |
26,5 |
1,7 |
50,8 |
12,3 |
1 |
100 |
|
Доменный |
10 |
27,4 |
0,9 |
- |
3,3 |
58,4 |
- |
100 |
Принимаем влажность газов:
коксового W1=30
 ;
;доменного W2=30
 .
.
Определяем содержание влаги во влажном газе:

коксовый:
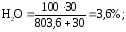
доменный:

Пересчитаем состав сухих газов на влажные:
Коксовый газ.
Содержание СО2во влажном газе:

Аналогично находим содержание других компонентов во влажных газах.
|
Состав |
СО2 |
СО |
СH4 |
C2H4 |
H2 |
N2 |
О2 |
H2O |
Всего |
|
Доменный |
9,64 |
26,42 |
0,87 |
- |
3,18 |
56,3 |
- |
3,6 |
100 |
|
Коксовый |
2,22 |
5,21 |
25,55 |
1,64 |
48,98 |
11,86 |
0,96 |
3,6 |
100 |
Определим низшие теплоты сгорания влажных газов:

Доменного:

Природного:

Находим долю доменного газа в смеси:
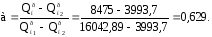
Доля коксового газа:

Определим состав смешанных влажных газов:

где х1и х2– содержание данного компонента в доменном и коксовом
газах соответственно, %.
Содержание СО2в смешанном газе:

Аналогично определяем содержание других компонентов смешанного газа и получаем его состав, %.
|
СО2 |
СО |
СH4 |
C2H4 |
H2 |
N2 |
О2 |
H2O |
Всего |
|
6,89 |
18,57 |
10,00 |
0,607 |
20,13 |
39,86 |
0,36 |
3,62 |
100 |
Для проверки точности расчёта определяем теплоту сгорания смешанного газа:

Разность между расчётной и заданной теплотой сгорания смешанного газа не превышает ±0,5%.
Далее табличным способом рассчитываем удельное теоретическое количество воздуха и продуктов сгорания (см. табл. 1).
Используя данные табл.1
для
 a=1,1
определим:
a=1,1
определим:
удельное количество воздуха:
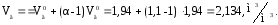
удельное количество продуктов сгорания:

удельное количество азота:
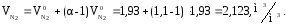
удельное количество кислорода:

Удельное количество других продуктов горения [табл. 1]:


Проверка:
Vп= 0,37+0,45+2,123+0,041=2,964 м3/м3
Таблица 1
Расчёт горения топлива (на 100 м3приa=1,0)
|
Участвуют в горении |
Образуется при горении газообразных продуктов | ||||||||||||||||||
|
Топливо |
Воздух | ||||||||||||||||||
|
Состав-ляющая |
Содержание % |
Кол-во, м3 |
Реакция горения |
О2, м3 |
N2, м3 |
Всего, м3 |
СО2, м3 |
H2O, м3 |
N2, м3 |
Всего, м3 | |||||||||
|
H2 |
20,13 |
20,13 |
H2+0,5O2=H2O |
10,07 |
41,07´3,76=154,44 |
41,07´154,44=195,51 |
— |
20,01 |
— |
20,13 | |||||||||
|
СО |
18,57 |
18,57 |
СО+0,5О2=СО2 |
9,29 |
18,57 |
— |
— |
18,57 | |||||||||||
|
СН4 |
10,00 |
10,00 |
СН4+2О2=СО2+2Н2О |
20,00 |
10,00 |
20,00 |
— |
30,00 | |||||||||||
|
С2Н4 |
0,61 |
0,61 |
С2Н4+3О2=2СО2+2Н2О |
1,8 |
1,22 |
1,22 |
— |
2,44 | |||||||||||
|
CO2 |
6,89 |
6,89 |
— |
— |
6,89 |
— |
— |
6,89 | |||||||||||
|
N2 |
39,86 |
39,86 |
— |
— |
— |
— |
193,27 |
193,27 | |||||||||||
|
О2 |
0,36 |
0,36 |
— |
-0,36 |
— |
— |
— |
— | |||||||||||
|
H2O |
3,62 |
3,62 |
— |
— |
— |
3,62 |
— |
3,62 | |||||||||||
|
Всего |
100 |
100 |
— |
40,80 |
153,41 |
194,21 |
36,68 |
44,85 |
193,27 |
274,92 | |||||||||
|
На 1 м3газа |
0,41 |
1,53 |
1,94 |
0,37 |
0,45 |
1,93 |
2,75 | ||||||||||||
Определим химический состав продуктов горения:




Определи плотность газа и продуктов сгорания:


Составим материальный баланс горения на 1м3газа:
Поступило: - газа rгVг=0,997×1=0,997 кг,
- воздуха rвVв=1,291×2,19=2,83 кг,
- Всего 3,83 кг.
Получено: - продуктов горения rпVп=1,291×2,944=3,8 кг.
Рассчитаем калориметрическую температуру горения. Для этого сначала определим энтальпию продуктов горения:
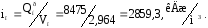
Предварительно примем tк¢=1700оС. Найдём температуру горения при данной температуре:

Так как iп¢<iп, то действительная калориметрическая температура горения больше 1700оС.
Повторно примем tк¢¢=1800оС.

Так как iп¢<iп<i²п, следовательноtп¢<tп<t²п.
Интерполяцией найдём калориметрическую температуру:

Требуемая колориметрическая температура:

где tм– температура металла по заданию,оС;
Dt– рекомендуемая разность температур [1. табл.2];
h- пирометрический коэффициент [1. табл.3].
Так как tк>tкmin, то подогрев воздуха не требуется.
В целях экономии топлива принимаем tв=4000С.
