
- •Методические указания
- •Содержание и форма отчета
- •В. И. Вернадским (1934г) была предложена такая геохимическая классификация элементов:
- •Лабораторная работа 4 Геохимические особенности поведения элементов в магматических процессах
- •Теоретическое обоснование
- •130304.65 «Геология нефти и газа»
- •355029, Г. Ставрополь, пр. Кулакова, 2
Министерство образования и науки Российской Федерации
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
«Северо-Кавказский государственный технический университет»
Методические указания
к лабораторным работам по дисциплине
«Геохимия»
для студентов специальности
130304.65 «Геология нефти и газа»
Ставрополь, 2009
Составители:
Бедина Р.М.
Туманова Е.Ю.
Стерленко З.В.
Рецензент: Вобликов Б.Г
|
| ||||
|
|
|
|
| |
|
|
| |||
СОДЕРЖАНИЕ
-
Лабораторная работа 1 Химическая таблица Д. И. Менделеева и геохимические свойства элементов в земной коре
Лабораторная работа 2 Виды и методы геохимического анализа
Лабораторная работа 3 Геохимические классификации химических элементов
Лабораторная работа 4 Геохимические особенности поведения элементов в магматических процессах
ЛАБОРАТОРНАЯ РАБОТА 1
Химическая таблица Д. И. Менделеева и геохимические свойства элементов в земной коре
Цель и содержание. Закрепление знаний на тему "Периодическая система Д.И, Менделеева" и подготовка студентов к выполнению лабораторных работ по геохимической классификации химических элементов.
Теоретическое обоснование.Теориодический закон Д.И. Менделеева был открыт в 1869г.
Факт существования семейств сходных элементов поставил перед Д.И. Менделеевым задачу найти связь между элементами, даже относящиеся к разным семействам. За основу сравнения элементов Д.И. Менделеев принял их относительные атомные массы как "коренное" постоянное свойство их атомов.
Расположив все химические элементы в порядке возрастания относительных атомных масс, начиная с водорода – элемента с наименьшей атомной массой. Пронумеровав элементы в том порядке, в котором они разместились в ряду, каждый химический элемент получил свой номер, который назвали порядковым номером этого элемента.
Ряды элементов, в пределах которых свойства изменяются последовательно, как, например, ряд из восьми элементов от лития до неона или от натрия до аргона (начинающийся щелочным металлом и заканчивающийся инертным элементом), Менделеев назвал периодами. Периоды, в свою очередь, подразделяются на малые (первый, второй, третий) и большие (четвертый, пятый, шестой). Номер периода показывает, сколько электронных слоев имеют атомы элементов этого периода.
Разделив все элементы на периоды, и располагая один период под другим так, чтобы сходные по свойствам и типу образуемых соединений элементы приходились друг под другом, Менделеев составил таблицу, названную им периодической системой элементов по группам и рядам. Она состоит из десяти горизонтальных рядов и восьми вертикальных столбцов, или групп. В восьмом ряду после лантана идут четырнадцать элементов, называемых лантаноидами (или лантанидами), которые чрезвычайно сходны с лантаном и между собой. Ввиду этого сходства, обусловленного особенностью строения их атомов, лантаноиды обычно помещают вне общей таблицы, лишь в клетке для лантана их положение в системе. Десятый ряд, составляющий седьмой период, - пока незаконченный, - период, содержит девятнадцать элементов, из которых первый и последние тринадцать получены лишь сравнительно недавно искусственным путем. Следующие за актинием четырнадцать элементов сходны по строению их атомов с актинием: поэтому их под названием актиноиды (или актиниды) помещают, подобно лантаноидам, вне общей таблицы. Номер группы показывает количество свободных электронов на внешнем энергетическом уровне.
В рядах, например, от лития до неона одинаково изменяются свойства с возрастанием относительной атомной массы, а именно:
ослабляются металлические свойства;
усиливаются неметаллические свойства;
изменяются свойства соединений элементов: от основных через амфотерные к кислотным.
В периодах наблюдается обратная зависимость.
Начиная с четвертого периода каждую группу периодической системы можно разбить на две подгруппы: «четную», состоящую из элементов верхних рядов, и «нечетную», образованную элементами нижних рядов. Элементы малых периодов Менделеев назвал типическими. Типические элементы расположены в главной подгруппе, а другие, – элементы нечетных рядов, сдвинутые вправо, расположены в побочной подгруппе. У атомов элементов главных подгрупп число электронов в наружном электронном слое совпадает с номером группы. В каждой главной подгруппе с возрастанием порядкового номера элементов металлические свойства усиливаются, а неметаллические ослабевают.
Если наружный слой содержит наибольшее число электронов, какое может вместить, он называется завершенным, а если меньше – незавершенным. Распределение электронов в различных слоях атомов в сокращенном варианте показано в таблице 1.
Таблица1-Распределение электронов в различных оболочках атомов
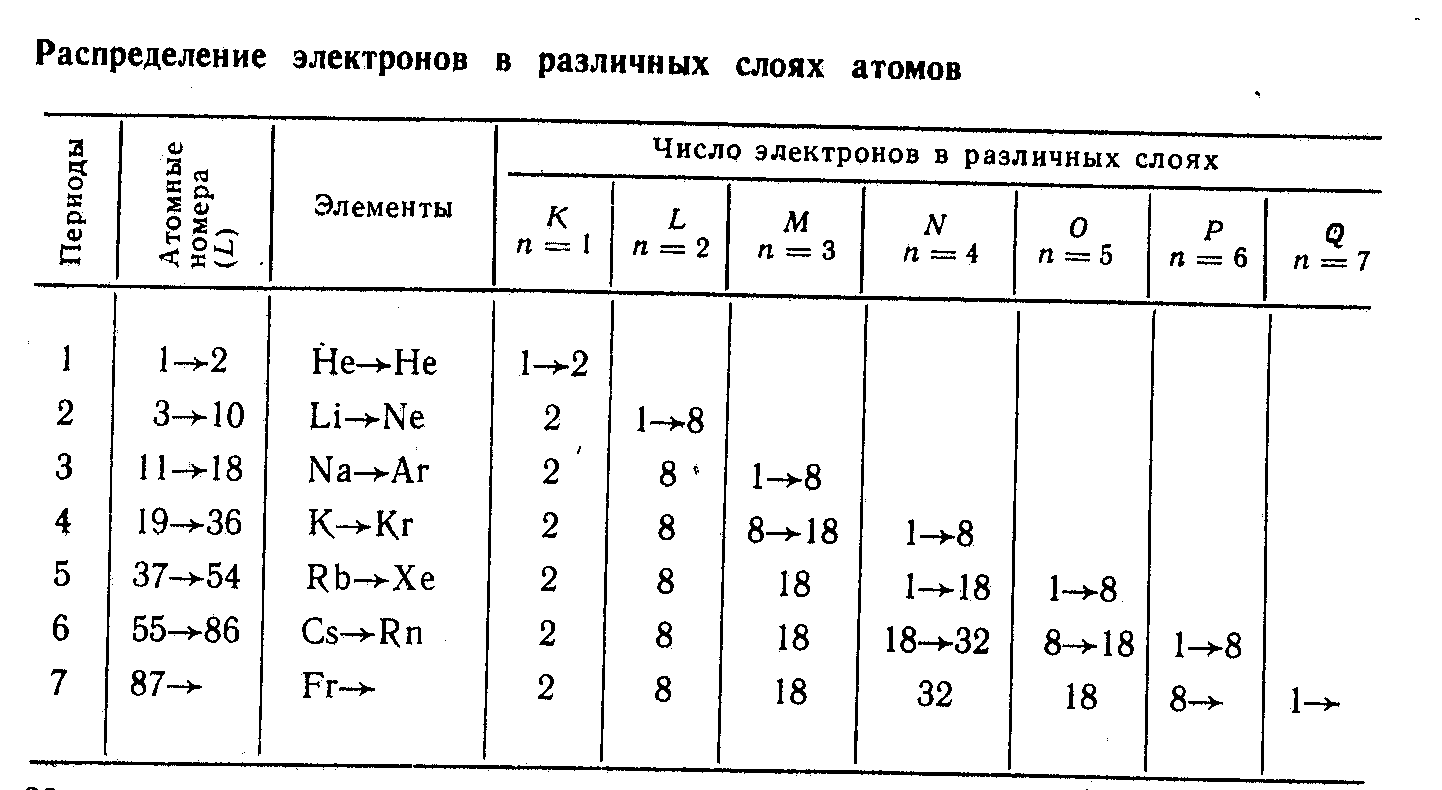
Максимально возможное число электронов в каждом слое равно 2n2, где n- номер оболочки, в К-оболочке – не больше 2, в L-оболочке не больше 8, в М-оболочке не больше 18 и т. д.
Состояние электронов в атоме можно представить в виде модели. Каждый электрон в атоме движется около ядра. Электроны, облака которых имеют шаровидную форму, как электронное облако атома водорода, называют s – электронами. Электроны, облака которых имеют форму вытянутой восьмерки, называются p – электронами. Электроны, облака которых имеют форму двух взаимно перпендикулярных восьмерок, называются d – электронами и т. д.
Таким образом, в периодической системе свойства элементов, их атомная масса, валентность, химический характер изменяются в известной последовательности, как в горизонтальном, так и в вертикальном направлениях. Место элемента в таблице определяется, следовательно, его свойствами, и, наоборот, каждому месту соответствуют элемент, обладающий определенной совокупностью свойств. Поэтому, зная положение элемента в таблице, можно довольно точно указать его свойства.
Аппаратура и материалы Таблицы, графики, рисунки.
Мероприятия по технике безопасности не предусматриваются
Методика и порядок выполнения работы
Задание.
В качестве объекта изучения избирается химический элемент системы Менделеева , который предлагается студенту.
По периодической системе Менделеева:
1.Охарактеризовать положение химического элемента в периодической системе Менделеева.(период, группа, подгруппа, атомный номер, атомный вес, электронная формула)
По справочнику по геохимии:
2. Дать характеристику ионного радиуса, потенциалов ионизации атомов и ионов, термические свойства элементов (температуры плавления, кипения, удельная теплоемкость.).
Используя таблицу Менделеева :
3.Дать характеристику 1.2.3 периодов.
4. Дать характеристику 4.5.6. периодов.
5. Какие элементы называются переходными и почему? Перечислите их.
Используя таблицы приложения справочника по геохимии:
6.Как изменяется ионный радиус элементов в направлениях:
а) слева на право - от натрия к аргону
б) сверху вниз - от углерода до свинца
в) по диагонали - от лития к рению.
Сделайте общий вывод – в каком направлении отмечается рост ионных радиусов и почему?
