
- •1 Начало термодинамики и его применение к изопроцессам в идеальных газах. Теплоемкости при постоянном объеме и давлении. Энтальпия.
- •1 Начало термодинамики. Адиабатный процесс. Уравнение адиабаты. Политропный процесс.
- •Билет №11 Вопрос №1 Инерциальные системы отсчета. Преобразования Галилея. Принцип относительности Галилея.
- •2 Начало термодинамики. Понятие об энтропии и ее статистическое толкование. Возрастание энтропии при необратимых процессах.
2 Начало термодинамики. Понятие об энтропии и ее статистическое толкование. Возрастание энтропии при необратимых процессах.
Второе начало термодинамики является фундаментальным законом природы. Оно охватывает самый широкий круг природных явлений и указывает направление, в котором самопроизвольно протекают термодинамические процессы.
Второе начало термодинамики, как и первое, имеет несколько формулировок.
Невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, полностью в работу.
Эти формулировки показывают, что тепловые процессы являются необратимыми. Мерой необратимости процесса, мерой хаотичности является энтропия.
![]()
Возрастание энтропии системы при необратимом процессе выражает тот факт, что тепло само по себе не может переходить от менее нагретых к более нагретым телам. Последнее утверждение можно рассматривать также как формулировку второго начала термодинамики.
![]() ,
где
константа k=1,38·10−23 Дж/К названа Планком
постоянной Больцмана, а Omega — статистический
вес состояния, является числом возможных
микросостояний (способов), с помощью
которых можно составить данное
макроскопическое состояние.
,
где
константа k=1,38·10−23 Дж/К названа Планком
постоянной Больцмана, а Omega — статистический
вес состояния, является числом возможных
микросостояний (способов), с помощью
которых можно составить данное
макроскопическое состояние.
Энтропией называется термодинамическая величина, изменение которой в системе пропорционально ее тепловой энергии, деленной на абсолютную температуру.
Знак неравенства ΔS > 0 относится к необратимым процессам. В реальных системах все процессы необратимы. Например, расширение газа, выравнивание температуры. Таким образом, второе начало термодинамики формулируется и как закон возрастания энтропии. Во всех необратимых процессах в замкнутой системе энтропия всегда возрастает.
Возрастание энтропии сопровождается выравниванием температуры или плотности газа. Это можно связать с порядком и беспорядком. Под порядком будем понимать сосредоточение частиц или энергии в определенном месте пространства, а под беспорядком (хаосом) - равномерное распределение их во всем объеме. Тогда возрастание энтропии при совершающихся без внешних воздействий необратимых процессах отражает природное стремление систем переходить от состояния более упорядоченного в состояние менее упорядоченное. Этот процесс сопровождается рассеянием энергии.
Билет №14
Вопрос №1
Вращательное движение твердого тела. Кинематические характеристики вращательного движения, угловое перемещение, угловая скорость, угловое ускорение и их связи с соответствующими линейными характеристиками.
Под вращательным движением абсолютно твердого тела понимают его движение как целого вокруг неподвижной оси, наз. осью вращения. При этом все точки твердого вращаются вокруг этой оси в параллел. плоскостях, описывая окружности с центрами лежащими на оси вращения. Все точки этого тела имеют разные по величине и направлению скорости.
Поэтому для описания вращ. движения вводятся угловые кинематические характеристики, единые для всего тела: угловое перемещение, угловая скорость и угловое ускорение.
Угловое перемещение есть акс. вектор равный отношению длины дуги, описываемой точкой, к радиусу вращения и направленный вдоль оси вращения по правилу винта:
![]() ,
гдеk
– орт оси вращения.
,
гдеk
– орт оси вращения.
Угловой скоростью наз. предел, к которому стремиться отношение малого углового перемещения, определенного за некоторый интервал, к величине этого интервала при его стремление к нулю.
![]() Угловая скорость показывает быстроту
изменения угла поворота.
Угловая скорость показывает быстроту
изменения угла поворота.
Угловое
ускорение: ![]()
Угловая скорость и угловое ускорение также явл. акс. векторами.
Связь между линейной и угловой скоростью.
По рис.dl=Rdφ.
Абсолютная величина угловой скорости
определяется соотношением
![]()
Поэтому
![]() ,
а так как (dl/dt)
есть линейная скорость точки, то
,
а так как (dl/dt)
есть линейная скорость точки, то
![]()
Связь между
линейным и угловым ускорением.
![]()
Билет №14
Вопрос №2
Явления переноса. Внутреннее трение (вязкость). Закон Ньютона. Коэффициент динамической вязкости идеального газа.
Явления переноса объединяют группу процессов, связанных с неоднородностями плотности, температуры или скорости упорядоченного перемещения отдельных слоев вещества. Выравнивание неоднородностей приводит к возникновению явления переноса.
Явления переноса в газах и жидкостях состоят в том, что в этих веществах возникает упорядоченный, направленный перенос массы (диффузия), импульса (внутренняя энергия) и внутренней энергии (теплопроводность). При этом в газах нарушается полная хаотичность движения молекул и распределение молекул по скоростям.
Вя́зкость (вну́треннее тре́ние) — свойство текучих тел (жидкостей и газов) оказывать сопротивление перемещению одной их части относительно другой. В результате происходит рассеяние в виде тепла работы, затрачиваемой на это перемещение.
В газах внутреннее
трение обусловлено переносом импульса,
в жидкостях – взаимодействием молекул.
Явление вязкости или внутреннего трения
наблюдается, когда соприкасающиеся
слои жидкости или газа движутся с
различными скоростями. Если │![]() 2│>│
2│>│![]() 1│,
то для поддержания такого движения
нужно приложить силуF
в направлении скорости движения, равную
силе внутреннего трения. Величина этой
силы равна:│F
│=s*η*(│
1│,
то для поддержания такого движения
нужно приложить силуF
в направлении скорости движения, равную
силе внутреннего трения. Величина этой
силы равна:│F
│=s*η*(│![]() 2-
2-![]() 1│)/∆z
и называется законом Ньютона для силы
внутреннего трения.
1│)/∆z
и называется законом Ньютона для силы
внутреннего трения.
Коэффициент
динамической вязкости идеального газа:
![]()
Билет №15
Вопрос №1
Динамика гармонических колебаний. Дифференциальное уравнение гармонических колебаний. Энергия гармонических колебаний. Примеры свободных колебательных систем: пружинный маятник, математический маятник, физический маятник.
Гармоническими колебаниями называются такие колебания, при которых колеблющаяся величина изменяется со временем по закону синуса или косинуса. Уравнение гармонических колебаний имеет вид x=ACos(wt+ф) или x=ASin(wt+ф) где x - смещение колеблющейся величины от положения равновесия.
Дифференциальное уравнение гармонических колебаний
Составим
дифференциальное уравнение гармонических
колебаний на примере пружинного маятника
Сначала запишем уравнении динамики
2ой закон Ньютона:
![]()
![]() И
теперь:
И
теперь:![]() Делим
на m и обозначаем
Делим
на m и обозначаем![]() :
:![]() Это
уравнение решается.
Это
уравнение решается.
Энергия гармонических колебаний
По
определению кинетическая энергия тела
массой m,
движущегося со скоростью ![]() равна
равна![]()
![]()
![]()
Потенциальная
энергия равна
![]()
Полная
энергия равна
![]()
Пружинный маятник
- это груз массой m, закрепленный на
абсолютно упругой пружине и совершающий
гармонические колебания под действием
упругой силы Fупр= - k x, где k - коэффициент
упругости, в случае пружины называемый
жесткостью. Уравнение движения маятника
![]() или
или![]() . Из приведенных выражений следует, что
пружинный маятник совершает гармонические
колебания по закону х = A cos (w0
t +j),
с циклической частотой
. Из приведенных выражений следует, что
пружинный маятник совершает гармонические
колебания по закону х = A cos (w0
t +j),
с циклической частотой
![]() и
периодом
и
периодом![]()
Математический
маятник - материальная точка, совершающая
под действием силы тяжести колебания
вдоль дуги окружности, расположенной
в вертикальной плоскости. Период
![]() длина нити
длина нити
Физический маятник
- абсолютно твердое тело, совершающее
малые колебания под действием силы
тяжести вокруг неподвижной горизонтальной
оси, не проходящей через его центр
тяжести.
![]()
Билет №15
Вопрос №2
Рапределение молекул по кинетическим энергиям ɛ их поступательного движения. График f(). Вычисления вероятнейшей ɛвер и средней <ɛ> кинетической энергии поступательного движения молекул.
Функция
распределения по значениям кинетической
энергии поступательного движения
молекул , характеризующая вероятность
попадания значений кинетической энергии
в интервал :
![]() .Приравняв
вероятности
.Приравняв
вероятности
![]() или
или
![]() ,
и используя подстановку
,
и используя подстановку
![]() и
и
![]() ,
имеем:
,
имеем:
 .
Это распределение справедливо только
для равновесного состояния термодинамической
системы. Вследствие достаточно общего
метода его получения, оно применимо не
только для газов, но и для любых систем,
движение микрочастиц которых описывается
уравнениями классической механики.
.
Это распределение справедливо только
для равновесного состояния термодинамической
системы. Вследствие достаточно общего
метода его получения, оно применимо не
только для газов, но и для любых систем,
движение микрочастиц которых описывается
уравнениями классической механики.
Вероятнейшее
значение
Определим
производную функции
![]() и
приравняем её нулю:
и
приравняем её нулю:
![]() .Тогда
имеем выражение для наиболее вероятного
значения кинетической энергии:.
.Тогда
имеем выражение для наиболее вероятного
значения кинетической энергии:.
![]()
Среднее значение: т.к. i=3, то <E>=3/2*k*T
Билет №16
Вопрос №1
Понятие о моменте силы и моменте импульса относительно точки. Гироскоп. Прецессия гироскопа.
Пусть О - какая-либо неподвижная точка в инерциальной системе отсчета. Ее называют началом или полюсом. Обозначим через r радиус-вектор, проведенный из этой точки к точке приложения силы F (рис. 1) .
Моментом силы F
относительно точки О называется векторное
произведение радиуса-вектора r
на силу F:
![]() ,
,![]() ,
(1) α- угол между векторамиr
и F;
направление M
выбирается так, чтобы последовательность
векторов r,
F,
M
образовывала правовинтовую систему,
т. е. если смотреть вдоль вектора M,
то поворот по кратчайшему пути от первого
сомножителя в (1) ко второму осуществлялся
по часовой стрелке, таким образом M
совпадает с направлением поступательного
движения правого буравчика, рукоятка
которого вращается от r
к F
по наикратчайшему пути.
,
(1) α- угол между векторамиr
и F;
направление M
выбирается так, чтобы последовательность
векторов r,
F,
M
образовывала правовинтовую систему,
т. е. если смотреть вдоль вектора M,
то поворот по кратчайшему пути от первого
сомножителя в (1) ко второму осуществлялся
по часовой стрелке, таким образом M
совпадает с направлением поступательного
движения правого буравчика, рукоятка
которого вращается от r
к F
по наикратчайшему пути.
Моментом импульса материальной точки относительно точки О называется векторное произведение радиуса-вектора r на импульс p:
![]() .
(3)
.
(3)
Для системы n материальных точек моментом импульса относительно некоторой точки О называется векторная сумма моментов импульсов этих точек относительно того же начала:
![]() .
(4)
.
(4)
Гироско́п — устройство, способное реагировать на изменение углов ориентации тела, на котором оно установлено, относительно инерциальной системы отсчета.
Прецессия гироскопа
Наблюдать прецессию достаточно просто. Нужно запустить волчок и подождать, пока он начнёт замедляться. Первоначально ось вращения волчка вертикальна. Затем его верхняя точка постепенно опускается и движется по расходящейся спирали. Это и есть прецессия оси волчка.
Главное свойство прецессии — безынерционность: как только сила, вызывающая прецессию волчка, пропадёт, прецессия прекратится, а волчок займёт неподвижное положение в пространстве. В примере с волчком этого не произойдет, поскольку в нём вызывающая прецессию сила — гравитация Земли — действует постоянно.
Билет №16
Вопрос №2
Случайные величины и их описание. Функции распределения. Связь функции распределения с вероятностью. Условия нормировки. Средние значения. Понятие о флуктациях.
Случайная величина - величина, измеряемая в исследуемых экспериментах, исходы которых заранее неизвестны и зависят от случайных причин. Дискретная - принимает конечное или счетное множество значений; задается законом распределения, который позволяет установить вероятность любого возможного значения случайной величины. Непрерывная принимает все значения из некоторого конечного или бесконечного промежутка; характеризуется плотностью вероятности (плотностью распределения) f(x) - непрерывной функцией, позволяющей вычислить вероятность попадания величины X на интервал (a,b): P(a<X<b) =интеграл от a до b f(x)dx
Условие нормировки

В частности по
этой формуле может быть найдено среднее
значение параметра x:

Флуктуации - случайные колебания, отклонения (от средних показателей); несистематические изменения каких-либо явлений или процессов, вызываемые случайными факторами.
Билет №17
Вопрос №1
Кинематика гармонических колебаний. Амплитуда, циклическая частота и фаза гармонических колебаний. Скорость и ускорение при гармонических колебаниях. Векторная диаграмма. Комплексное представление гармонических колебаний.
Гармоническими наз. колебания в любой физической системе, которые описываются величиной, изменяющейся по закону синуса или косинуса.
.
Амплитуда — модуль максимального отклонения тела от положения равновесия
Цикл. частота w - есть число колебаний осциллятора за 2π секунд: w = 2p/Т, Величина, обратная периоду колебаний Т, называется частотой ν = 1/Т = w/2p. Частота - есть число колебаний осциллятора за одну секунду.
Фаза колебания есть значение колеблющейся величины в данный момент времени.
Фаза гармонических колебаний Ф линейно растет со временем. При t = 0 значение Ф равняется j0, которое называется начальной фазой. Начальная фаза задает значение x в начальный момент времени. Начальную фазу и амплитуду гармонического осциллятора можно рассчитать исходя из начальных условий, подставив в уравнение колебательного движения и выражение для его скорости υ = dx/dt значение времени t = 0. Проделав соответствующие операции, получим:х(0) = х0 = А·cos(j0).u(0) = u0 = -А·w·sin(j0).где υ - скорость колеблющейся системы. Решив эту систему уравнений, получим, что величины амплитуды и начальной фазы опр. начальными условиями для рассматриваемой системы. A = (x02 + υ02/ω2)1/2; tg φ0 = -υ0/(x0·ω).
Найдем величины скорости и ускорения колебательного движения, описываемого уравнением: x = A·sin(w·t + j0). Поскольку ск-ть u - есть производная от координаты по времени, а ускорение - производная от скорости a = dυ/dt, то для гармонических колебаний, описываемых уравнением, эти величины зависят от времени также по гармоническим законам:u = A·w·cos(w·t + j0) = A·w·sin(w·t + j0 + p/2); a = -A·w2·sin(w·t + j0) = -w2·x. Для гармонических механических колебаний скорость опережает по фазе смещение на p/2, а ускорение - на p. Наличие пропорциональной зависимости ускорения от величины смещения от положения равновесия явл. характерным признаком гарм. колебат. движения.
Комплексное представление гармонических колебаний
Векторные диаграммы можно считать вариантом (и иллюстрацией) представления колебаний в виде комплексных чисел. При таком сопоставлении ось Ox соответствует оси действительных чисел, а ось Oy — оси чисто мнимых чисел (положительный единичный вектор вдоль которой есть мнимая единица). Тогда вектор длиной A, вращающийся в комплексной плоскости с постоянной угловой скоростью ω с начальным углом φ0 запишется как комплексное число
![]() а его действительная
часть
а его действительная
часть
![]()
Билет №17
Вопрос №2
Критическое состояние. Критические параметры и их выражение через постоянные Ван-дер-Ваальса.
Состояние вещества, характеризуемое критическими параметрами Ркр (давление), Vкр (удельный объем), Ткр (температура), называется критическим состоянием.
Критическая температура - температура, при которой исчезают различия в физических свойствах между жидкостью и ее насыщенным паром.
На этих изотермах
хорошо просматривается участок, где
давление растёт с ростом объёма. Этот
участок не имеет физического смысла. В
области, где изотерма делает зигзагообразный
изгиб, изобара пересекает её три раза,
то есть, имеется три значения объёма V
при одинаковых значениях параметров P
и T.
Это соответствует существованию трёх
действительных корней уравнения![]() .
При повышении температуры волнообразный
участок уменьшается и превращается в
точку (см. точка К на рис.). Эта точка
называется критической,
а значения
.
При повышении температуры волнообразный
участок уменьшается и превращается в
точку (см. точка К на рис.). Эта точка
называется критической,
а значения
![]() ,
,![]() и
и![]() в
этой точке называютсякритическими
параметрами.
Критической точке соответствуют три
совпадающих корня уравнения. При
температурах, превышающих критическую,
изотермы Ван-дер-Ваальса становятся
монотонно убывающими функциями
P(V). Критические
параметры
в
этой точке называютсякритическими
параметрами.
Критической точке соответствуют три
совпадающих корня уравнения. При
температурах, превышающих критическую,
изотермы Ван-дер-Ваальса становятся
монотонно убывающими функциями
P(V). Критические
параметры
![]() ,
,![]() и
и![]() можно
найти из условия, что в критической
точке изотерма Ван-дер-Ваальса имеет
как экстремум, так и точку перегиба:
можно
найти из условия, что в критической
точке изотерма Ван-дер-Ваальса имеет
как экстремум, так и точку перегиба:
![]() ,
, .Решая эти
два уравнения совместно с
.Решая эти
два уравнения совместно с
 можно получить
можно получить![]() ,
,![]() ,
,![]()
Билет №18
Вопрос №1
Векторная диаграмма. Сложение гармонических колебаний одного направления и одинаковой частоты. Сложение взаимно-перпендикулярных колебаний.

Билет №18
Вопрос №2
Реальный газ. Понятие о вандерваальсовых силах. Уравнение Ван-дер-Ваальса. Другие уравнения состояния реального газа.
Реальный газ -газ, свойства которого существенно зависят от взаимодействия молекул
![]() ;
Zr =
Zr (p,T) — коэффициент
сжимаемости газа
;
Zr =
Zr (p,T) — коэффициент
сжимаемости газа
Вандерваальсовские силы - слабые силы взаимного притяжения, способствующие сцеплению между соседними атомами или молекулами. Силы вызваны распространением электронов в соседние атомы или молекулы.
Уравнение
Ван-дер-Ваальса
![]()
Поправка a учитывает силы притяжения между молекулами (давление на стенку уменьшается, так как есть силы, втягивающие молекулы приграничного слоя внутрь), поправка b — объем молекул газа.
Уравнение Дитеричи — уравнение состояния, связывающее основные термодинамические величины в газе. Первое уравнение Дитеричи для умеренных давлений значительно лучше уравнения Ван-дер-Ваальса, но зато совершенно непригодно для больших давлений.
![]()
Уравнение Бертло́ — двухпараметрическое уравнение состояния реального газа.
![]() .
.
Билет №19
Вопрос №1
Динамика гармонических колебаний. Дифференциальное уравнение гармонических колебаний. Двухатомная молекула как линейный гармонический осциллятор. Приведенная масса.
С вободными
или собственными колебаниями называют
колебания, которые происходят в системе,
выведенной из положения равновесия и в
дальнейшем предоставленной самой
себе.
вободными
или собственными колебаниями называют
колебания, которые происходят в системе,
выведенной из положения равновесия и в
дальнейшем предоставленной самой
себе.
В связи с тем, что гармонические колебания характеризуются при движении изменением скорости и ускорения системы, необходимо найти причины этих колебаний, т.е. силы. Например, при колебаниях на тело (м.т.), закрепленное на нити, действуют сила тяжести и сила натяжения нити. Под действием равнодействующей этих сил и происходит процесс колебания тела (рис. 6.12).
Причем при движении маятника от положения II к положению I и обратно направление силы периодически изменяется от - Fmax до + Fmin.
Согласно второму
закону Ньютона вектор ускорения м.т.,
совершающей гармонические колебания,
 .
.
Дифференциальное
уравнение гармонических колебаний
имеет вид:
![]() .
.
Гармони́ческий осцилля́тор (в классической механике) — система, которая при смещении из положения равновесия испытывает действие возвращающей силы F, пропорциональной смещению x (согласно закону Гука):
![]()
где k — коэффициент жёсткости системы.
Приведенная масса - условная характеристика распределения масс в движущейся механич. или смешанной (напр., электромеханич.) системе, зависящая от физ. параметров системы (масс, моментов инерции, индуктивности и т. д.) и от закона её движения. В простейших случаях П. м. m определяют из равенства
T=mv2/2,
Билет №19
Вопрос№ 2
Изотермы Ван-дер-Ваальсовского газа. Опытные изотермы реального газа. Метастабильные состояния. Фазовая диаграмма жидкость-газ. Уравнение Клапейрона-Клаузиуса.
Метастабильное состояние — состояние квазиустойчивого равновесия физической системы, в котором система может находиться длительное время.
Метастабильные состояния соответствуют одному из минимумов термодинамического потенциала системы при заданных внешних условиях. Устойчивому (стабильному) состоянию отвечает самый глубокий минимум. Однородная система в метастабильном состоянии удовлетворяет условиям устойчивости равновесия термодинамического Cр>Cv>0, (dP/dV)_T<0, относительно малых возмущений физических параметров (энтропии, плотности и др.). При достаточно больших возмущениях система переходит в абсолютно устойчивое состояние.
Уравнение Клапейрона
— Клаузиуса — термодинамическое уравнение,
относящееся к квазистатическим (равновесным)
процессам перехода вещества
из одной фазы в
другую (испарение, плавление, сублимация,
полиморфное превращение и др.). Согласно
уравнению, теплота фазового перехода
(например, теплота
испарения, теплота
плавления)
при квазистатическом процессе определяется
выражением
![]() ,
где
,
где ![]() —
удельная теплота фазового перехода,
—
удельная теплота фазового перехода, ![]() —
изменение удельного объёма тела при
фазовом переходе.
—
изменение удельного объёма тела при
фазовом переходе.
Билет №20
Вопрос №1
Понятие о затухающих колебаниях. Дифференциальное уравнение затухающих колебаний. Зависимость амплитуды колебаний от времени. Коэффициент затухания. Логарифмический декремент затухания.
Механическими колебаниями называют движения тел, повторяющиеся точно или приблизительно через одинаковые промежутки времени.
Свободные механические колебания всегда оказываются затухающими, те колебаниями с убывающей амплитудой.
Диф. Уравнение
затухающих колебаний:
![]() , где
, где![]() ,
а
,
а![]() .
.
Амплитуда колебаний постепенно уменьшается, и через некоторое время после начала колебаний становится равной нулю.
Коэффициент затухания – скорость затухания колебаний, определяемая величиной β=r/2m. Коэффициент затухания обратен по величине тому промежутку времени, за который амплитуда уменьшилась в е раз. (βτ=1, где τ , время, за которое амплитуда уменьшится в е раз.)
Отношение значений амплитуд, соответствующих моментам времени, отличающимся на период, равно a(t) / a(t+T)= eβT. Это отношение называют декрементом затухания, а его логарифм — логарифмическим декрементом затухания: Λ=lna(t)/a(t+T)=βT
Последнюю величину обычно используют для характеристики затухания колебаний. Выразив β через λ и Т в соответствии с (73.12), закон убывания амплитуды можно записать в виде а = а0 е -λ/T· tЗа время т, за которое амплитуда уменьшается в е раз, система успевает совершить Ne = τ/Т колебаний.Из условия е -λ·τ/T =е-1 получается, что λ·τ/T = λNe = 1.Следовательно, логарифмический декремент затухания обратен по величине числу колебаний, совершаемых за то время, за которое амплитуда уменьшается в е раз.
Билет №20
Вопрос №2 !!!!!!!
Внутренняя энергия реального газа. Адиабатные процессы в реальных газах. Эффект Джоуля-Томсона. Точка инверсии. Кривая инверсии.
Вну́тренняя эне́ргия термодинамической системы (обозначается как E или U) — это сумма энергий теплового движения молекул и межмолекулярных взаимодействий.
Термодинамическое
определение внутренней энергии указывает
на способ измерения этой величины. В
математическом выражении для первого
начала термодинамики:
![]()
где
![]() —
подведённое к телу количество теплоты,
—
подведённое к телу количество теплоты,![]() —работа,
совершаемая телом против внешних сил.
—работа,
совершаемая телом против внешних сил.
Адиабатным называют такой процесс, в котором к системе не подво-дится тепло и от системы не отводится тепло. При адиабатном процессе должна быть обеспечена идеальная теплоизоляция от внешней среды, в отличие от изотермического процесса, требующего идеального теплового контакта со средой. В реальных условиях процесс является адиабатным, если система снабжена хорошей теплоизоляцией или если процесс протекает настолько быстро, что не происходит заметного теплообмена с внешней средой.
|
|
|
Если газ будет расширяться или сжиматься без теплообмена с внешней средой и без совершения внешней работы, то согласно первому началу термодинамики его внутренняя энергия должна оставаться постоянной. Для газа, энергия которого определяется формулой (121.1), должно при этом соблюдаться условие dUкм=CVdT +a/V2км dV км= 0
откуда
следует, что dТ и dVKM имеют разные знаки.
Следовательно, при расширении в таких условиях газ должен всегда охлаждаться, а при сжатии—нагреваться.
Э ффект
Джоуля — Томсона Пропуская газ по
теплоизолированной трубке с пористой
перегородкой, Джоуль и Томсон обнаружили,
что при расширении, которым сопровождается
прохождение газа через перегородку,
температура его несколько изменяется.
В зависимости от начальных давления и
температуры изменение температуры ∆T
имеет тот или иной знак и, в частности,
может оказаться равным нулю. Это явление
получило название эффекта Джоуля —
Томсона. Если температура газа понижается
(∆T<0), эффект считается положительным;
если газ нагревается (∆T>0), эффект
считается отрицательным. Отметим, что
эффект Джоуля — Томсона всецело
обусловлен отклонениями газа от
идеальности. Для идеального газа pV
= RT и условие (122.2) превращается в Tt +
RT,=CVT2 + RT2, откуда следует, что Т1 = Т2.
ффект
Джоуля — Томсона Пропуская газ по
теплоизолированной трубке с пористой
перегородкой, Джоуль и Томсон обнаружили,
что при расширении, которым сопровождается
прохождение газа через перегородку,
температура его несколько изменяется.
В зависимости от начальных давления и
температуры изменение температуры ∆T
имеет тот или иной знак и, в частности,
может оказаться равным нулю. Это явление
получило название эффекта Джоуля —
Томсона. Если температура газа понижается
(∆T<0), эффект считается положительным;
если газ нагревается (∆T>0), эффект
считается отрицательным. Отметим, что
эффект Джоуля — Томсона всецело
обусловлен отклонениями газа от
идеальности. Для идеального газа pV
= RT и условие (122.2) превращается в Tt +
RT,=CVT2 + RT2, откуда следует, что Т1 = Т2.
Билет №21
Вопрос №1
Понятие о вынужденных колебаниях. Дифференциальное уравнение вынужденных колебаний. Зависимость амплитуды вынужденных колебаний от частоты изменения вынуждающей силы. Механический резонанс. Резонансная частота. Резонансная амплитуда.
Колебания под действием внешних периодически изменяющихся сил называются вынужденными колебаниями.
Диф. Уравнение
вынужденных колебаний:
![]() ,
где
,
где![]() ,
,![]() -
коэффициент затухания.
-
коэффициент затухания.
Зависимость амплитуды вынужденных колебании от частоты вынуждающей силы приводит к тому, что при некоторой определенной для данной системы частоте амплитуда колебаний достигает максимального значения. Колебательная система оказывается особенно отзывчивой на действие вынуждающей силы при этой частоте. Это явление называется резонансом, а соот- ветствующая частота — резонансной частотой
Явление возрастания амплитуды установившихся вынужденных колебаний до максимального значения при приближении частоты изменения внешней силы к частоте свободных колебаний системы называется резонансом.
Амплитуда при резонансе получается при подстановке найденного выражения ωрез в формулу для A(ω).
 .
.
При β << ω0:
 .
.
При ω = 0 отклонение системы от положения равновесия
![]() .
.
Найдем отношение Aрез / A0при условии β << ω0:
 ,
,
здесь Q - добротность.
Добротность показывает (при β << ω0 ) во сколько раз амплитуда при резонансе больше смещения при ω = 0.
График зависимости A(ω) при различных β носят название резонансных кривых.
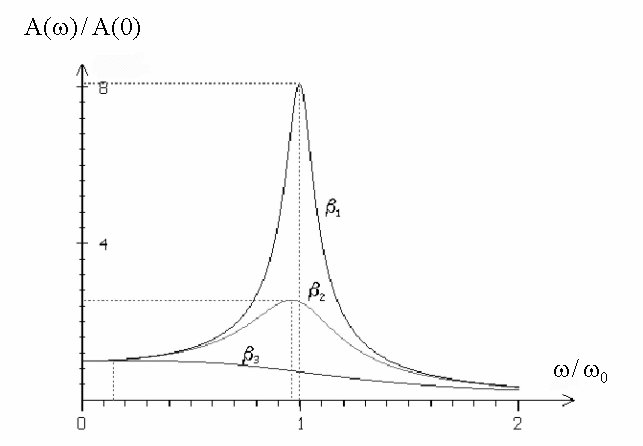
Билет №21
Вопрос №2
Связь коэффициента теплопроводности, вязкости и диффузии и их зависимости от давления, температуры и размеров молекул. Классификация течений газа в зависимости от числа Кнудсена. Особенности явлений переноса в ультраразреженных газах.
Связь:
![]()
![]()
Коэффициент
вязкости не зависит от числа молекул в
единицы объема, а значит и от
давления(P=n*k*T), возрастает с температурой
несколько быстрее, чем
![]() и прямо пропорционален
и прямо пропорционален![]() .
Коэффициент теплопроводности – зависит
от давления и температуры так же, как
и коэф-т вязкости, обратно пропорционален
.
Коэффициент теплопроводности – зависит
от давления и температуры так же, как
и коэф-т вязкости, обратно пропорционален![]() .
Коэф-т диффузии обратно пропорционален
числу молекул в единице объема, а значит
и давлению, от температуры – такая же,
обратно пропорционален
.
Коэф-т диффузии обратно пропорционален
числу молекул в единице объема, а значит
и давлению, от температуры – такая же,
обратно пропорционален![]() .
.
В зависимости от
числа Кнудсена( ![]() течение
газа можно разделить на три основ-ные
области:
течение
газа можно разделить на три основ-ные
области:
1 Если ![]() 0,01, то
средняя длина пробега молекул меньше 1
% от толщины
пограничного слоя, в этом случае течение
считается сплошным. В этом случае
газодинамические параметры
воздуха (
0,01, то
средняя длина пробега молекул меньше 1
% от толщины
пограничного слоя, в этом случае течение
считается сплошным. В этом случае
газодинамические параметры
воздуха (![]() являются
непрерывными величи-нами, то есть имеет
место область обычной газовой динамики.
являются
непрерывными величи-нами, то есть имеет
место область обычной газовой динамики.
2 Если ![]() 1,
то длинна свободного пробега молекул
мала по сравне-нию с размером обтекаемого
тела, но соизмерима с толщиной пограничного
слоя. В этом случае течение называется
течением со скольжением.
1,
то длинна свободного пробега молекул
мала по сравне-нию с размером обтекаемого
тела, но соизмерима с толщиной пограничного
слоя. В этом случае течение называется
течением со скольжением.
3 Если ![]() 1,
то длинна свободного пробега больше
или соизмеримы по вели-чине с толщиной
пограничного слоя. В этом случае имеется
область свободно молекулярных
течений. В этой области элементарные
частицы не взаимодейст-вуют между собой
и пограничного слоя фактически нет.
1,
то длинна свободного пробега больше
или соизмеримы по вели-чине с толщиной
пограничного слоя. В этом случае имеется
область свободно молекулярных
течений. В этой области элементарные
частицы не взаимодейст-вуют между собой
и пограничного слоя фактически нет.
Поведение ультраразреженных газов отличается целым рядом особенностей. В условиях вакуума нельзя говорить о давлении одной части газа на другую. При обычных условиях молекулы часто сталкиваются друг с другом. Поэтому по любой поверхности, которой можно мысленно разграничить газ на две части, будет происходить обмен импульсами между молекулами, и, следовательно, одна часть газа будет действовать по поверхности раздела на вторую с давлением р. В вакууме молекулы обмениваются импульсами только со стенками сосуда, так что имеет смысл лишь понятие давления газа на стенку. Внутреннее трение в газе также отсутствует. Однако тело, движущееся в ультраразреженном газе, будет испытывать действие силы трения, обусловленной тем, что молекулы, ударяясь об это тело, будут изменять его импульс. Рассмотрим этот вопрос более подробно.
Пусть в ультраразреженном газе движутся параллельно друг другу две пластинки (рис. 257). Скорости пластинок равны «i и и2. Взаимодействие между молекулой н пластинкой в момент удара приводит к тому, что молекула, отскочив от пластинки, имеет в дополнение к тепловой скорости составляющую, равную по величине и направлению скорости пластинки.
Коэффициент теплопроводности, равный 1/6 ρϋcv, оказывается в ультраразреженном газе пропорциональным плотности газа. Следовательно, теплопередача от одной стенки к другой будет с понижением давления уменьшаться, в то время как теплопроводность газа при обыч-* ных условиях не зависит, как мы видели, от давления
Билет №22
Вопрос №1
Уравнение плоской бегущей волны в тригонометрической и комплексной формах. Длина волны. Волновое число. Графическое изображение волны.
Пусть в начале
координат находится твердая плоскость,
которая колеблется по гармоническому
закону и вынуждает частицы упругой
среды, находящейся рядом с ней, колебаться
по этому же закону. Направим ось х
перпендикулярно этой плоскости. Тогда
вдоль этой оси будет распространяться
плоская гармоническая продольная волна.
Наша задача - найти
![]() -
уравнение волны, если задано.
-
уравнение волны, если задано.

Колебания до
волновой поверхности, удаленной от
начала координат на расстояние x, дойдут
через время
![]() ,
значит уравнение волн
,
значит уравнение волн![]()
Длиной волны λ называется расстояние между двумя ближайшими максимумами или минимумами возмущения (расстояние между двумя точками, колеблющимися в одинаковых фазах).
Волновое число, величина, связанная с длиной волны λ соотношением: k = 2π/λ (число волн на длине 2π).
Графическое изображение волны
Билет №22
Вопрос №2
Опытные изотермы реального газа. Фазовая диаграмма жидкость-газ. Фазовые переходы. Насыщенный пар. Метастабильные состояния.
Переход вещества от одной фазы в другую – фазовый переход – всегда связан с качественными изменениями свойств вещества. Примером фазового перехода могут служить изменения агрегатного состояния вещества или переходы, связанные с изменениями в составе, строении и свойствах вещества (например, переход кристаллического вещества из одной модификации в другую).Различают фазовые переходы двух родов. Фазовый переход первого рода (например, плавление, кристаллизация и т.д.) сопровождается поглощением или выделением вполне определённого количества теплоты, называемой теплотой фазового перехода.
Насыщенный пар, пар, находящийся в термодинамическом равновесии с жидкостью (или твёрдым телом) того же химического состава. Между жидкостью и её Н. п. существует динамическое равновесие: число молекул, вырывающихся в единицу времени из жидкости и переходящих в паровую фазу, равно числу молекул пара, возвращающихся в жидкость за то же время. Н. п., не содержащий взвешенных частиц жидкости, называют сухим, а содержащий капельки жидкости, — влажным Н. п. Состояние сухого Н. п. крайне неустойчиво, так как при малейшем отводе от него теплоты пар частично конденсируется и превращается во влажный, а при малейшем подводе теплоты превращается в перегретый.
Метастабильное состояние в термодинамике, состояние неустойчивого равновесия физической макроскопической системы, в котором система может находиться длительное время.
Возможность реализации М. с. связана с особенностями перехода системы из одного устойчивого состояния в другое (с кинетикой фазовых переходов). Фазовый переход начинается с возникновения зародышей новой фазы: пузырьков пара в случае перехода жидкости в пар, микрокристалликов при переходе жидкости в кристаллическое состояние и т.п.
Билет №23
Вопрос №1
Волновое движение. Волны продольные и поперечные. Волновая поверхность. Фронт волны. Плоская и сферическая волна. Скорость распространения колебаний в среде.
Билет №23
Вопрос №2
Понятие о диффузии в жидкости и твердом теле. Зависимость коэффициента диффузии от температуры. Вязкость жидкости. Зависимость коэффициента вязкости от температуры.
(Есть в др. билетах).
Билет №24
Вопрос №2
Сравнительные характеристики твердого, жидкого и газообразного состояний вещества. Понятие о радиальной функции распределения. Ближний и дальний порядок. Тепловое движение молекул в жидкости. Время оседлой жизни молекул.
Агрегатные состояния вещества - состояния одного и того же вещества в различных интервалах температур и давлений.
Газовая фаза - агрегатное состояние вещества, молекулы которого: обладают бОльшей энергией, чем молекулы жидкости; слабо связаны силами взаимного притяжения; и движутся хаотически.
Жидкая фаза - агрегатное состояние вещества, промежуточное между твердым и газообразным состояниями. В этом состоянии молекулы вещества: обладают бОльшей энергией, чем молекулы твердого тела; менее плотно соединены друг с другом; способны преодолевать силы взаимного притяжения.
Твердая фаза - агрегатное состояние вещества, характеризуемое жесткой молекулярной структурой. В этом состоянии молекулы вещества совершают малые колебания около фиксированных положений равновесия.
Дальний порядок и ближний порядок - упорядоченность во взаимном расположении атомов или молекул в твёрдых телах и жидкостях. Упорядоченность на расстояниях, сравнимых с межатомными, называется ближним порядком, а упорядоченность, повторяющаяся на неограниченно больших расстояниях, - дальним порядком. В жидкостях и аморфных телах существует ближний порядок - некоторая закономерность в расположении соседних атомов. На больших расстояниях порядок "размывается" и постепенно переходит в "беспорядок", т. е. дальнего порядка в жидкости и аморфных телах нет.
В кристаллах атомы расположены правильными рядами, и правильное чередование атомов на одних и тех же расстояниях друг относительно друга повторяется для сколь угодно отдалённых атомов, т. е. существует Д.п. и б. п.
Тепловое движение молекул (атомов) жидкости представляет собой сочетание малых колебаний около положений равновесия и частых перескоков из одного положения равновесия в другое. Последние и обусловливают существование в жидкостях лишь ближнего порядка в расположении частиц, а также свойственные им подвижность и текучесть.
Время “осёдлой жизни” - время колебаний около положения равновесия.
Билет №25
Вопрос №1
Дифференциальное волновое уравнение. Понятие о фазовой и групповой скорости. Энергия, переносимая волной. Поток энергии.
Уравнение волны
в дифференциальной форме обычно называют
волновым
уравнением;
вид этого уравнения следующий:
![]() или
или![]() ΔS
-оператор Лапласа:
ΔS
-оператор Лапласа:![]() .
Уравнение синусоидальной волны является
решением волнового уравнения (можно
проверить подстановкой). Общее же решение
волнового уравнения следующее:
.
Уравнение синусоидальной волны является
решением волнового уравнения (можно
проверить подстановкой). Общее же решение
волнового уравнения следующее:![]() .
ЗдесьА
и В
- произвольные константы, а f1
и f2
- произвольные дважды дифференцируемые
функции. Первое слагаемое описывает
волну, распространяющуюся слева направо,
второе - встречную волну.
.
ЗдесьА
и В
- произвольные константы, а f1
и f2
- произвольные дважды дифференцируемые
функции. Первое слагаемое описывает
волну, распространяющуюся слева направо,
второе - встречную волну.
Скоростью волны v называется скорость перемещения волновой поверхности (фазовая скорость). Экспериментально ее можно найти, определив скорость перемещения фронта волны
Групповая скорость — это скорость перемещения группы или цуга (пакета) волн: скорость перемещения огибающей волнового пакета. При отсутствии поглощения в среде групповая скорость совпадает со скоростью перемещения энергии этой группы волн. Если среда, в которой распространяется рассматриваемая группа волн, не обладает дисперсией (или форма волны изменяется в результате дисперсии не очень быстро), то групповая скорость совпадает с фазовой, так как все волны, входящие в группу, распространяются с одной и той же фазовой скоростью.
Распространение
волн связано с переносом энергии. При
этом частицы среды не переносятся
волной, а совершают колебание около
положения равновесия. Скорость
колеблющейся частицы равна:
![]() Кинетическая
энергия частиц, заключенных в объеме
Кинетическая
энергия частиц, заключенных в объеме
![]() ,
равна
,
равна
![]() .
Масса выделенного объемаm
равна:
.
Масса выделенного объемаm
равна:
![]() ,
где ρ
- плотность среды. Тогда значение
кинетической энергии выделенного объема
равно:
,
где ρ
- плотность среды. Тогда значение
кинетической энергии выделенного объема
равно:
![]() .
Выделенный объем обладает также
потенциальной энергией
.
Выделенный объем обладает также
потенциальной энергией
![]() .
Можно показать, что
.
Можно показать, что
![]() ,
где
,
где
![]() .
Следовательно, кинетическая энергия
выделенного объема равна потенциальной
энергии. Полная энергия равна сумме
кинетической и потенциальной энергии
.
Следовательно, кинетическая энергия
выделенного объема равна потенциальной
энергии. Полная энергия равна сумме
кинетической и потенциальной энергии
![]() .
Полная энергия, возникающая в упругой
среде при распространении в ней плоской
гармонической волны, равна
.
Полная энергия, возникающая в упругой
среде при распространении в ней плоской
гармонической волны, равна![]() Плотностью
энергии
называется энергия, заключенная в
единице объема, т. е.
Плотностью
энергии
называется энергия, заключенная в
единице объема, т. е.
![]() Из формулы следует, что плотность энергии
в каждый момент времени в разных точках
пространства различна. Среднее значение
плотности энергии определяется средним
значением квадрата синуса
Из формулы следует, что плотность энергии
в каждый момент времени в разных точках
пространства различна. Среднее значение
плотности энергии определяется средним
значением квадрата синуса![]() Следовательно,
среднее по времени значение плотности
энергии в данной точке среды равно
Следовательно,
среднее по времени значение плотности
энергии в данной точке среды равно![]()
Поток энергии
Билет №25
Вопрос №2
Конденсированные состояния. Кристаллы. Основные типы структур. Общине характеристики простейших структур: координационное число, число атомов в элементарной ячейке, коэффициент упаковки. Тепловое движение атомов в твердом теле. Классическая теория теплоемкости твердого тела.
Конденсированное состояние - твёрдое и жидкое состояния вещества. В отличие от газообразного состояния, у вещества в конденсированном состоянии существует упорядоченность в расположении частиц (ионов, атомов, молекул). Кристаллические твёрдые тела обладают высокой степенью упорядоченности — дальним порядком в расположении частиц. Частицы жидкостей и аморфных твёрдых тел располагаются более хаотично, для них характерен ближний порядок.
Криста́ллы (от греч. κρύσταλλος, первоначально — лёд, в дальнейшем — горный хрусталь, кристалл) — твёрдые тела, в которых атомы расположены закономерно, образуя трёхмерно-периодическую пространственную укладку — кристаллическую решётку.
Металлы имеют относительно сложные типы кубических решеток - объемно центрированная (ОЦК) и гранецентрированная (ГЦК) кубические решетки.
В основе классической
теории теплоёмкости твёрдых тел
(кристаллов) лежит закон равнораспределения
энергии по степеням свободы. Твёрдое
тело рассматривается как система N
независимых друг от друга атомов, имеющих
по три колебательных степени свободы.
Атомы совершают тепловые колебания
около положений равновесия, и если они
малы, то их можно рассматривать как
гармонические. На каждую степень свободы
приходится в среднем энергия kT ( в виде
кинетической и в виде потенциальной,
k – постоянная Больцмана, T – абсолютная
температура тела). Имея в виду, что число
колебательных степеней свободы равно
3N, получим, что внутренняя энергия одного
моля атомов U=3NA kT=3RT, где NA – число
Авогадро, R=kNA – универсальная газовая
постоянная. Отсюда молярная теплоёмкость
твёрдого тела: .
![]()
