- •Лабораторний практикум з фізичної хімії
- •091706 – Технологія зберігання, консервування та переробки плодів і овочів)
- •Передмова
- •Запам’ятайте!
- •Тема 1: хімічна термодинаміка Загальні теоретичні відомості
- •Лабораторна робота №1 визначення теплової сталої калориметра і теплоти розчинення калію хлориду у воді
- •Лабораторна робота №2
- •Лабораторна робота №3 визначення теплоти гідратоутворення купрум (II) сульфату
- •Контрольні питання
- •Тема 2: хімічна рівновага Загальні теоретичні відомості
- •Лабораторна робота №4
- •Розрахунок рівноважних концентрацій речовин
- •Контрольні питання
- •Тема 3. Фазові рівноваги
- •Теоретичні відомості
- •Лабораторна робота №5 визначення коефіцієнта розподілу речовини між незмішуваними рідинами
- •Методика виконання роботи
- •Контрольні питання
- •Тема 3: фазові рівноваги
- •Загальні теоретичні відомості
- •Побудова та аналіз діаграм плавкості і3 простою евтектикою
- •Лабораторна робота № 6 Побудова діаграми фазової рівноваги бінарної евтектичної системи
- •Методика виконання роботи
- •Лабораторна робота №7 кристалізація бінарних сумішей (система NaNо3 – kno3)
- •Методика виконання роботи
- •Контрольні питання
- •Тема 4: електрохімія Потенціометрія Загальні теоретичні відомості
- •Лабораторна робота №8
- •Методика виконання роботи
- •Контрольні питання
- •Загальні теоретичні відомості
- •Лабораторна робота №9 визначення ступеня й константи дисоціації слабкого електроліту методом електричної провідності
- •Методика виконання роботи
- •Питома електрична провідність розчину кCl
- •Контрольні питання
- •Тема 5. Х і м і ч н а к і н е т и к а Загальні теоретичні відомості
- •Лабораторна робота №10 вивчення швидкості інверсії цукру Загальні теоретичні відомості
- •Методика в и к о н а н н я р о б о т и
- •Контрольні питання
- •Лабораторна робота №11 вивчення швидкості йодування ацетону
- •Методика в и к о н а н н я р о б о т и
- •Контрольні питання
- •Кінетика гетерогенних процесів Загальні теоретичні відомості
- •Лабораторна робота №12 вивчення кінетики розчинення твердої кислоти у воді
- •Методика виконання роботи.
- •Котрольні питання
- •Тема 6. Будова молекул, електричні та оптичні властивості
- •Лабораторна робота 13 Рефрактометричне визначення концентрації розчину
- •Методика виконання роботи
- •Лабораторна робота 14
- •Лабораторна робота 15
- •Контрольні питання
- •Список рекомендованої літератури
Контрольні питання
Які термодинамічні і кінетичні ознаки рівноважного стану?
Через які величини можна виразити константу хімічної рівноваги? Яка залежність існує між константами рівноваги, вираженими різними способами?
Які фактори впливають на значення констант рівноваги Кр і Кс?
Як, виходячи з принципу Ле-Шательє, передбачити вплив температури або тиску на константу рівноваги?
Які ознаки свідчать про досягнення рівноваги? Як, на підставі експериментальних даних, визначити константи рівноваги хімічних реакцій при даних температурах?
Як можна змістити рівновагу при постійній температурі? Як впливає тиск, концентрації вихідних речовин і продуктів реакції на рівноважний вихід?
Як розрахувати тепловий ефект реакції, знаючи константи рівноваги при різних температурах?
У яких координатах залежність константи рівноваги від температури виражається прямою лінією? Який нахил має ця пряма у випадку екзо- і ендотермічної реакції?
Тема 3. Фазові рівноваги
ТРИКОМПОНЕНТНІ СИСТЕМИ. РОЗПОДІЛ РЕЧОВИНИ МІЖ ДВОМА РІДКИМИ ФАЗАМИ
Теоретичні відомості
Розчинена речовина у системі з двох незмішуваних рідин підпорядковується закону розподілу Нернста: речовина, розчинена в двох незмішуваних рідинах, розподіляється між ними так, що відношення концентрацій її в обох рідинах при даній температурі є величина постійна. Ця величина називається коефіцієнтом розподілу К:
|
|
(3.1) |
де СI і СII – рівноважні концентрації розчиненої речовини в розчинах І і ІІ.
Цей вираз закону розподілу справджується в тому разі, коли молекулярна маса розподілюваної речовини однакова в обох фазах, тобто коли відсутня дисоціація або асоціація частинок, і коли додавання речовини до системи не викликає зміни взаємної розчинності рідких фаз.
У загальному випадку, коли ураховують вплив дисоціації і асоціації молекул речовини застосовують рівняння Шилова-Лєпінь:
|
|
(3.2) |
де n – величина, що не має певного фізичного смислу, але залежить від температури і природи всіх трьох речовин, які утворюють систему.
Величина разраховується за рівнянням:
|
|
(3.3) |
де
![]() і
і
![]() – молярна
маса розчиненої речовини в першому і
другому розчинниках.
– молярна
маса розчиненої речовини в першому і
другому розчинниках.
Якщо в одній з фаз розчинена речовина дисоціює, а в іншій асоціює, то коефіцієнт розподілу змінюється з концентрацією, при цьому рівняння (3.1) матиме вигляд:
|
|
(3.4) |
де — ступінь дисоціації у фазі 1;
n — число молекул в асоційованому комплексі у фазі 2.
Рівняння (3.4) є загальним аналітичним вираженням закону розподілу Нернста-Шилова. Якщо речовина не дисоціює і не асоціює, рівняння (3.4) переходить у рівняння (3.1). Якщо речовина асоціює тільки в другій фазі, то рівняння (3.5) перетвориться в:
|
|
(3.5) |
де п — відношення середніх молекулярних мас у першому і в другому розчинниках: п=М1 /М2.
У загальному випадку важко передбачити, чи буде молярна маса розчиненої речовини однаковою в обох рідких фазах. Тому експерементально визначають ряд рівноважних концентрацій речовини в першому і другому розчинниках, і підставляють значення у лінійну форму рівняння Шилова-Лєпінь:
|
|
(3.6) |
Якщо на
осі ординат відкладати lg
![]() ,
а на осі абсцис — lg
,
а на осі абсцис — lg
![]() то одержимо пряму, тангенс кута нахилу
якої дорівнює n,
а відрізок, що відтинається прямою на
осі ординат – lgK.
Рівняння (3.6) дозволяє, таким чином,
графічно визначати n
і К з експериментальних даних розподілу
речовини між двома розчинниками при
різних його концентраціях.
то одержимо пряму, тангенс кута нахилу
якої дорівнює n,
а відрізок, що відтинається прямою на
осі ординат – lgK.
Рівняння (3.6) дозволяє, таким чином,
графічно визначати n
і К з експериментальних даних розподілу
речовини між двома розчинниками при
різних його концентраціях.
Із закону розподілу випливає, що коефіцієнт розподілу К не залежить від концентрації розчиненої речовини в обох рідинах, але залежить від температури та природи розчиненої речовини й розчиників.
Коефіцієнт розподілу використовується для експериментального визначення ступеня асоціації чи дисоціації розчиненої речовини в тому чи іншому розчиннику, активності розчинених речовин і інших подібних величин.
Закон розподілу лежить в основі процесу екстрагування. Екстракцією називають процес вилучення із розчину однієї або декількох розчинених речовин за допомогою другого розчинника (екстрагента), що не змішується з першим.
Метою екстракції є поділ сумішей, підвищення концентрації будь-якої речовини, звільнення розчинника від домішок, заміна розчинника.
Закон розподілу дозволяє розраховувати кількість видаленої речовини, що залишилася у вихідному розчині (рафінаті), після n вилучень екстрагентом заданого об'єму при даній температурі:
|
|
(3.7) |
де m1 - маса речовини, що залишились у вихідному розчині 1 після n вилучень його розчинником 2;
V1 - об'єм вихідного розчину (1);
V2 - об'єм екстрагенту (2);
m0 – маса речовини у вихідному розчині (1);
К – коефіцієнт розподілу.
З формули (3.7) видно, що екстрагувати краще послідовно невеликими порціями, чим одноразового великим об’ємом розчинника. При екстракції коефіцієнтом розподілу умовно називають відношення концентрації розчину, з якого екстрагується розчинена речовина, до концентрації розчину, яким екстрагують.
Присутність інших розчинених речовин часто впливає на процес екстрагування. При цьому можуть змінюватися властивості розчинника чи властивості розчиненої речовини. Так, розчинність органічних речовин у воді знижується при насиченні води неорганічною сіллю, що не розчиняється в органічному розчиннику («висолювання»). Розчинність слабких органічних кислот у воді знижують, додаючи мінеральні кислоти, що зменшують ступінь дисоціації слабких кислот.
Екстракцію застосовують при визначенні загальної кількості жиру в м'ясних продуктах, у продуктах переробки плодів та овочів; при розділенні та вивченні білків біологічних об'єктів, при виділенні смол із рослинної сировини тощо.


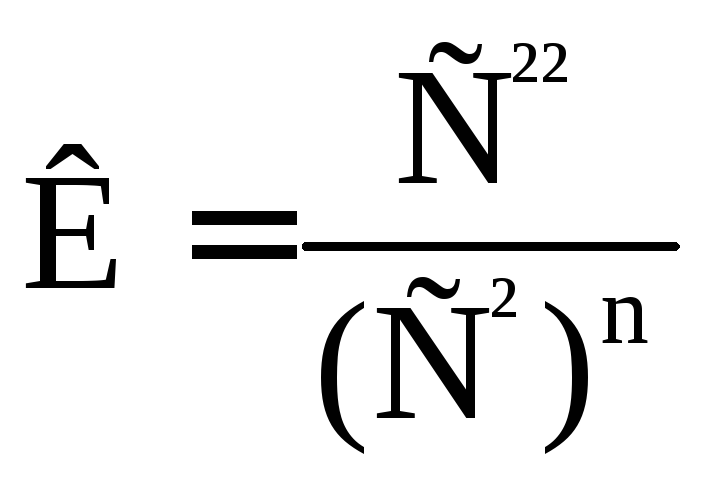
 ,
,
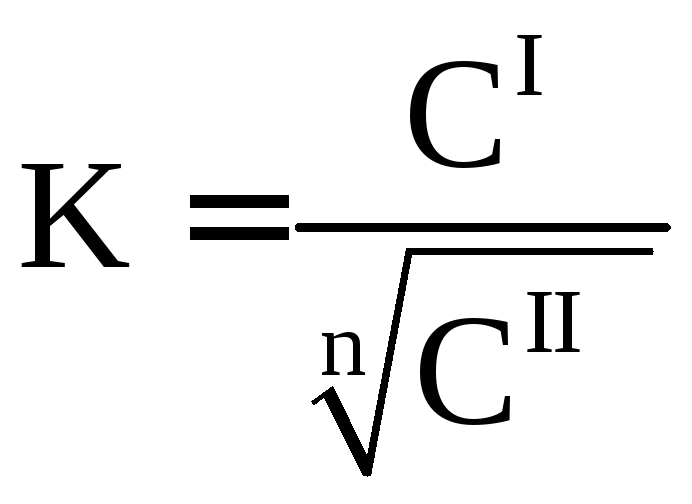 ,
чи
,
чи