
Бх FiBO-2012
.pdf
Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
O |
КoQ10 |
|
|
|
|
|
O |
CH3 |
|
|
|
|
|
H3C |
|
|
|
|
|
|
H3C O |
|
|
|
|
|
|
O |
CH3 CH3 CH3 CH3 CH3 |
CH3 |
CH3 |
CH3 |
CH3 |
CH3 |
• |
Окисляетсяцитохромами |
|
|
|
|
|
• |
Этоколлекторэлектроновнескольких FAD- |
|
||||
|
зависимыхДГ |
|
|
|
|
|
08.03.2012 |
|
|
|
|
273 |
|
Комплекс II (Сукцинат-КoQ редуктаза)или
СДГ
• Комплекс II содержит
FAD и 7-8 Fe-S белковв
3 кластерах
• Комплекс II СДГ,
одновременнофермент ЦТК иинтегральный белок внутренней мембраныМх
• МассаСДГ от100 до 140 kD
08.03.2012 |
274 |
Комплекс II и III
•КoQ акцептируетэлектронысобеихкомплексовI и II ипереноситнакомплексIII.
08.03.2012 |
275 |
91
Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
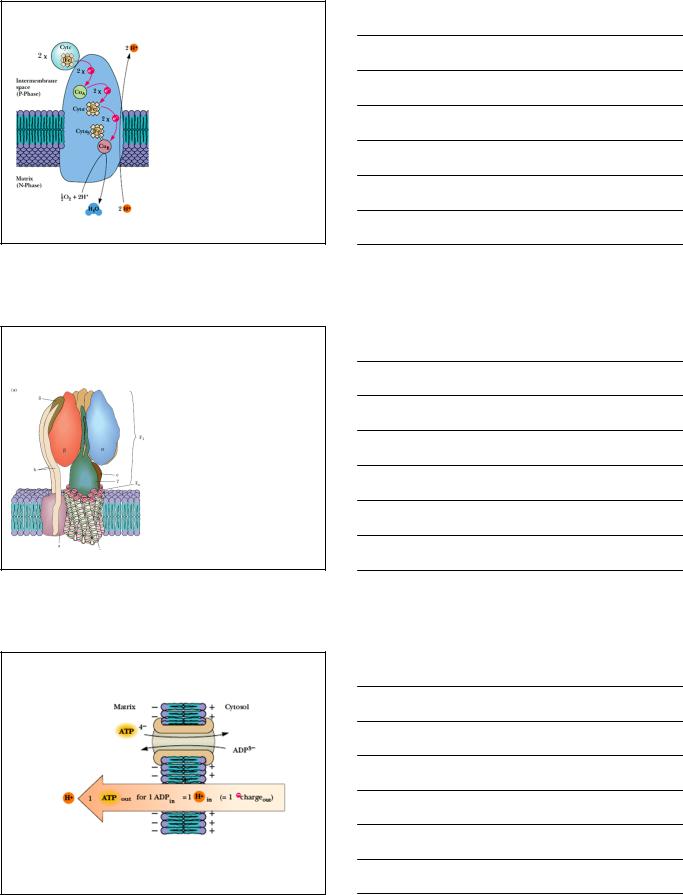
Комплекс IV: Цитохром c Оксидаза
• Комплекс IV назван
Цитохром c Оксидазойпотому что акцептирует электроныс цитохромаси направляетдля4-х электронного восстановленияO2 до H2O
08.03.2012 |
276 |
Комплекс V H+-АТФ-аза
(АТФ-синтаза )
• |
Ионныеградиентына |
|
внутреннеймембране -форма |
|
хранениябиологически |
|
конвертируемойэнергии, |
|
которая совершаетполезную |
|
работу,когдапотокионовидет |
|
вобратномнаправлении |
• |
ОбратныйпотокH+ противего |
|
электрохимическогоградиента |
|
черезАТФ-синтазу–источник |
|
синтеза АТФизАДФиФн |
• |
Этотвездесущийфермент |
|
играетрольтурбины |
|
превращающейэнергию |
08.03.2012 |
протонногоградиентавАТФ |
277 |
ATФ/AДФ - транслоказа
• Транспорт АТФ из Мх (ч/з ATФ/AДФ транслоказу) происходит в мембране Мх по электрохимическому
08.03.2012 потенциалу (∆µH+) 278
92

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
Функционирование ДЦ
08.03.2012 |
279 |
The Structures of Several Inhibitors of ETC
and OP
08.03.2012 |
280 |
Действие разобщителей ОФ
O- H+ OH
NO2 |
NO2 |
NO2 NO2
•2,4-динитрофенол (2,4-ДНФ),какслабаякислота связываетпротонвмежмембранномпространствеи переноситеговматрикс Мх (рассеиваяэнергию
DmH+ ) |
281 |
08.03.2012 |
93

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
2,4-ДНФ снижает DmH+
H+ |
H+ |
H+ |
H+ H+ |
H+ |
H+ H+ H+ |
H+ H+ |
25:1 H+ |
|||
Межмембранно |
H+ |
H+ |
H+ |
H |
+ H+ |
H+ |
H |
+ H+ |
|
|
е пространство |
H+ |
H+ |
H+ |
H+ |
- |
H+ |
H+ |
|
||
|
|
|
|
|
|
O |
|
|
|
|

 NO2
NO2
NO2
NO2
O2N
OH
Матрикс Мх
|
H+ |
08.03.2012 |
282 |
Биоэнергетика Дж. Николс. М. Мир. 1985
08.03.2012 |
283 |
Эндогенныеразобщителигенерируюттепло
•Некоторыеживотныевпроцессеадаптациикхолоду, анабиоза,атакженоворожденныеживотные содержат БЖТ и производятбольшоекол-вотепла засчетразобщенияОФ
•БЖТэтихорганизмовсодержатмногоМх,во внутреннеймембране которыхмалоАТФ-синтетазы, но присутствуетбелоктермогенинилибелокразобщитель,образующийпассивныепротонный канал,рассеивающийэнергиюDmH+ ввидетепла
08.03.2012 |
284 |
94

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
Мх БЖТ
• Протонный цикл в Мх БЖТ имеет утечку, которую м остановить ГДФ
• Это часть мех-ма теплопродукции, использующего ЖК.
• Норадреналин активирует мобилизацию ЖК
285
Разобщающие белки
Uncoupling Proteins (UCP 1-5)
Вразных тканях человека иживотных выделено 5 видов UCP 1-5, уровень экспрессии ифункциикоторых различны:
Разобщение ОФ (регуляция продукции АТФ)
Генерация тепла (адаптация к холоду)
Предотвращение образования АФК
Предотвращение апоптоза идр.
08.03.2012 |
286 |
Энергетика
Протонная:
В Мх Дц формируется ΔµН+ энергия которого конвертируется в другие виды (химич,
осмотич, механич, тепловую, световую и др.)
Натриевая:
Энергия АТФ образованного
вМх в цитоплазме при помощи Na/K- АТФазы обратимо (?) конвертируется
вградиент концентрации Na (ΔµNa+), которая используется клеткой для совершения разных видов работ (осмотич. – транспорт в-в, механ. передача сигнала и др.)
08.03.2012 |
287 |
95

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
Нарушения митохондриального ОФ
•Согласно концепции D. Wallace (1998-2008) любой ткани необходим минимально допустимый (пороговый) уровень производства АТФ
•Снижениеэтогоуровня ведеткнарушению энергозависимыхфункций
•РезкийдефицитАТФвнаиболееэнергозависимых тканях(нервная,сетчатка,миокард,скелетнаям-
ра,железистая) «дает»симптоматикупоражения именноэтихтканей – в виде энцефалопатий,
ретинопатий, кардиомиопатий миопатий и
08т.03..д2012. 288
Митохондриальныеболезни
(Митохондриальная медицина)
•Мхсодержат кольцевую ДНК (mtDNA)
•13 белков ДЦ из1000 белков Мх кодируются вmtDNA ,другие-вядерной
•Описаны некоторые заболевания и синдромы, связанные сповреждением mtDNA
08.03.2012 |
289 |
Некоторые Мхзаболевания
•НазванияМхзаболеванийобразуютсяпутемаббревиатур (сокращений).Клиническипротекаютввидекомплекса синдромовпораженияэнергозависимыхтканей
•LHON, Lebers hereditary optical neuropathy;
•MERRF, myoclonic epilepsy and ragged-red-fiber
disease;
•MELAS, mitochondrial encephalomyopathy, lactic acidosis, and strokelike episodes;
•NARP, neurological muscle weakness,ataxia, and retinitis pigmentosa;
•Leigh disease — SNE, subacute necrotizing encephalomyelopathy;
•KSS, Kearns–Sayre syndrome;
•CPEO, chronic progressive external
ophthalmoplegia.
08.03.2012 290
96

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
КлиническиепроявленияилечениеМх заболеваний
•Манифестация
–Мышечныесудорогии слабость
–Высокаяутомляемость,
–Лактат-ацидоз,
–Нарушениефункций ЦНС,
–Нарушениезрения.
•Лечение
–Оченьтрудноеичастомалоэффективное
–ОблегчаетсостояниеназначениеКоQ,менадиона, витаминовВ1, В2,РР,С,К, N-ацетилкарнитина, сукцинатаиглутамата
08.03.2012 |
291 |
Биологическое окисление-3
Микросомальное и перекисное окисление
Лекция 8
Лектор: д.м.н., проф. Грицук А. И.
зав. кафедрой биохимии Гомельского государственного медицинского университета
Мх -источник образования АФК
08.03.2012 |
293 |
97

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
Микросомальное окисление
(Монооксигеназная система)
(IIпутьпотребленияО2 )
•Субстраты мб. окислены внедрением в них атома O2.
•Ферменты монооксигеназы, или цит P450 или
оксидазы со смешанной функцией
•Ферменты ассоциированы с гладкой ЭПС, выделяемой в виде микросом.
•RH + O2 + NADPH + H+ R-OH + H2O + NADP+
08.03.2012 |
294 |
Микросомальное окисление
(II путь потребления О2 )
•Микросомы (МС)–искусств.евезикулы,образованные изобрывковЭПСпригомогенизацииткани.
•ВмембранахМСрасположеныМСДЦ основные функциикоторых:
–СинтезБАВ(гормоны,медиаторы,Pg, LT, TXA)
–Детоксикация ксенобиотиков
•Восновереакциймикросомальногоокисления реакцийлежитодное- восстановление О2
08.03.2012 |
295 |
Микросомальное окисление
(Монооксигеназная система)
•Субстраты мб. окислены внедрением в них атома O2.
•Ферменты монооксигеназы, или цит P450 или
оксидазы со смешанной функцией
•Ферменты ассоциированы с гладкой ЭПС, выделяемой в виде микросом.
•RH + O2 + NADPH + H+ R-OH + H2O + NADP+
08.03.2012 |
296 |
98

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
Сравнительная характеристика Мх и Мс ДЦ
Сходство |
Различие |
•Общие переносчики • Локализация (Мх и цитоплазма)
ДЦ (NAD, FP,
цитохромы) |
• В Мх (энергетические функции |
|
|
• Одинаковые |
О2) энергия е- депонируется в |
форме ΔµН+ (АТФ, осмотич, |
|
переносчики в начале |
механич, тепло и др.) |
и конце ДЦ |
|
•В Мс (пластические функции О2)
•Одинаковый ОВП и энергия е- не депонируется, а
уровень энергии е- |
идет на активацию О2 (обр. |
|
вступающих в ДЦ |
АФК), атакующего субстрат |
297 |
08.03.2012 |
|
Цитохром P450 монооксигеназы важнаясистемадетоксикациимногихлекарстви
гидроксилированиястероидов
• Цитохром P450 -суперсемейство гемсодержащих монооксигеназ, известно > 1000 ферментов
NADH и NADPH поставляют Н+ и е- для восстановления цитохромов, которые окисляют субстраты в реакциях именуемых
гидроксилазным циклом
08.03.2012 |
298 |
Функционированиемикросомальной ДЦ
e- e- O2
FMN |
Cyt b5 |
Cyt P450 |
|
|
H2O |
NADPH+H+ NADP+ |
|
RH R-OH |
08.03.2012 |
|
299 |
99

Кафедра биохимии ГомГМУ, 2012 |
08.03.2012 |
РольцитохромаP450 вмикросомальном окислении
08.03.2012 |
300 |
Механизммикросомального окисления
08.03.2012 |
301 |
Циклцитохрома Р450
08.03.2012 |
302 |
100
