
- •2. Технологический расчет времени контакта по средней степени превращения твердого реагента. Смесь частиц с различными, но постоянными размерами в режиме идеального вытеснения.
- •10. Применение функций распределения для расчета степени превращения реагентов в реальных реакторах.
- •13. Расчет реакторов, работающих в различных тепловых режимах. Изотермический режим. Проектное уравнение рис-н-и.
- •14. Расчет реакторов, работающих в различных тепловых режимах. Изотермический режим. Проектное уравнение рив-и.
- •15.Расчет реакторов, работающих в различных тепловых режимах. Политропный режим. Проектное уравнение рис-н-п.
- •24. Оптимальный температурный режим для различных схем химических реакций. Обратимые экзотермические реакции.
- •25. Оптимальный температурный режим для различных схем химических реакций. Обратимые эндотермические реакции.
- •27. Оптимальный температурный режим для различных схем химических реакций. Необратимые экзотермические реакции.
- •30. Топохимические процессы. Кинетика процессов взаимодействия газа (ж) с частицами сферической формы, протекающих в внешнедиффузионной области.
- •31. Топохимические процессы. Кинетика процессов взаимодействия газа (ж) с частицами сферической формы, протекающих в внутридиффузионной области.
- •32. Топохимические процессы. Кинетика процессов взаимодействия газа (ж) с частицами сферической формы, протекающих в кинетической области.
- •33. Топохимические процессы. Экспериментальные методы определения областей протекания тхп.
10. Применение функций распределения для расчета степени превращения реагентов в реальных реакторах.
В реальных реакторах частицы потока взаимодействуя друг с другом и образует глобулы. Такое состояние потока называется макроскопическим состоянием. Образование глобул обусловлена различными видами Вандер-ваальсовских взаимодействии. В движущемся потоке глобулы проявляют себя отдельной самостоятельной структурной единицей, параметры которых одинаковы для каждой частицы входящих в эту глобулу.
Пусть каждая из глобул находится в реакторе в течение определенного времени τ и из проточного реактора выходит n-глобул. Доля глобул, находящееся в реакторе в течение времени от τ до Δτ сост. производные E(τ)= Δτ.
Доля реагента не вступившего в реакцию за это время равно:
 или для всех глобул
или для всех глобул

Для проточного реактора РИС-Н функция имеет вид:

Если
в реакторе при этом протекает реакция
1 порядка, то
 или
или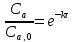
Тогда

После интегрирования:

В то же время для РИС-Н:
 или
или

Для реакции 2 порядка конечный результат расчета для потока имеет вид:

13. Расчет реакторов, работающих в различных тепловых режимах. Изотермический режим. Проектное уравнение рис-н-и.
Изотермические реакции проводят на практике только в непрерывных реакторах, так как для поддержания постоянной температуры в реакторе периодического действия отвод тепла должен изменяться во времени, что в промышленных условиях осуществить трудно. В связи с этим изотермические реакторы периодического действия на практике не применяются и здесь не рассматриваются. В изотермических реакторах путем подвода или отвода тепла поддерживается постоянная температура в течение всего процесса. В тех случаях, когда температура реакционной смеси на входе в реакторы равна температуре на выходе из него (т.е. Т = Т0), для РИВ-И и РИС-Н-И можно записать:
![]()
![]()
14. Расчет реакторов, работающих в различных тепловых режимах. Изотермический режим. Проектное уравнение рив-и.
Изотермические реакции проводят на практике только в непрерывных реакторах, так как для поддержания постоянной температуры в реакторе периодического действия отвод тепла должен изменяться во времени, что в промышленных условиях осуществить трудно. В связи с этим изотермические реакторы периодического действия на практике не применяются и здесь не рассматриваются. В изотермических реакторах путем подвода или отвода тепла поддерживается постоянная температура в течение всего процесса. В тех случаях, когда температура реакционной смеси на входе в реакторы равна температуре на выходе из него (т.е. Т = Т0), для РИВ-И и РИС-Н-И можно записать:

15.Расчет реакторов, работающих в различных тепловых режимах. Политропный режим. Проектное уравнение рис-н-п.
При политропическом режиме температура в реакторе непостоянна, при этом часть тепла может отводиться от реакционной смеси или подводиться к ней.


16. Расчет реакторов, работающих в различных тепловых режимах. Политропный режим. Проектное уравнение РИС-П-П.
При политропическом режиме температура в реакторе непостоянна, при этом часть тепла может отводиться от реакционной смеси или подводиться к ней.


17. Расчет реакторов, работающих в различных тепловых режимах. Политропный режим. Проектное уравнение РИВ-П.
При политропическом режиме температура в реакторе непостоянна, при этом часть тепла может отводиться от реакционной смеси или подводиться к ней.


18. Расчет реакторов, работающих в различных тепловых режимах. Адиабатический режим. Проектное уравнение РИС-Н-А.
При адиабатическом режиме в реакторе отсутствует теплообмен с окружающей средой и тепло химической реакции полностью расходуется на изменение температуры реакционной смеси.
![]()
19. Расчет реакторов, работающих в различных тепловых режимах. Адиабатический режим. Проектное уравнение РИВ-А.
При адиабатическом режиме в реакторе отсутствует теплообмен с окружающей средой и тепло химической реакции полностью расходуется на изменение температуры реакционной смеси.
![]()
20. Расчет реакторов, работающих в различных тепловых режимах. Адиабатический режим. Проектное уравнение РИС-П-А.
При адиабатическом режиме в реакторе отсутствует теплообмен с окружающей средой и тепло химической реакции полностью расходуется на изменение температуры реакционной смеси.


23. Оптимальный температурный режим для различных схем химических реакций. Необратимые эндотермические реакции.
Оптимальный температурный режим и способы его осуществления в промышленных реакторах
Температурный (тепловой) режим проведения химического процесса, обеспечивающий экономически целесообразную максимальную производительность единицы объема реактора (интенсивность) по целевому продукту, называют оптимальным.
Подход к разработке оптимального температурного режима может быть различным в зависимости от типа химической реакции. Очевидно, что максимальная интенсивность реактора будет достигнута при проведении процесса с максимально возможной скоростью. Рассмотрим поэтому, как влияет тип кинетического уравнения на выбор температурного режима.
Уравнение скорости необратимых экзо- и эндотермических реакций можно записать в виде ,
 (1)
(1)
Например, для реакции первого порядка
 (2)
(2)
Скорость химической реакции является функцией нескольких переменных: температуры и степеней превращения реагентов (или их концентраций). С ростом температуры константа скорости реакции в соответствии с уравнением Аррениуса монотонно возрастает. Из уравнений (1) и (2) видно, что принципиальных ограничений повышения температуры с целью увеличения скорости необратимых реакций нет. С ростом степени превращения реагентов скорость реакции падает. Для компенсации этого уменьшения целесообразно увеличивать температуру.
Эндотермическая реакция сопровождается поглощением теплоты. Следовательно, такие реакции невыгодно проводить в адиабатических условиях, так как по мере протекания реакции ее скорость будет падать как из-за увеличения степени превращения, так и из-за уменьшения температуры. Более разумно проводить эндотермические процессы в реакторах с подводом теплоты (изотермических или в реакторах с промежуточным тепловым режимом), поддерживая температуру, максимально допустимую по конструкционным соображениям. Необходимо при этом дополнительно провести оптимизацию температурного режима, сопоставив экономические показатели: увеличение прибыли вследствие роста производительности реактора и возрастания расходов на поддержание высокой температуры.
