
МДФд_26
.pdf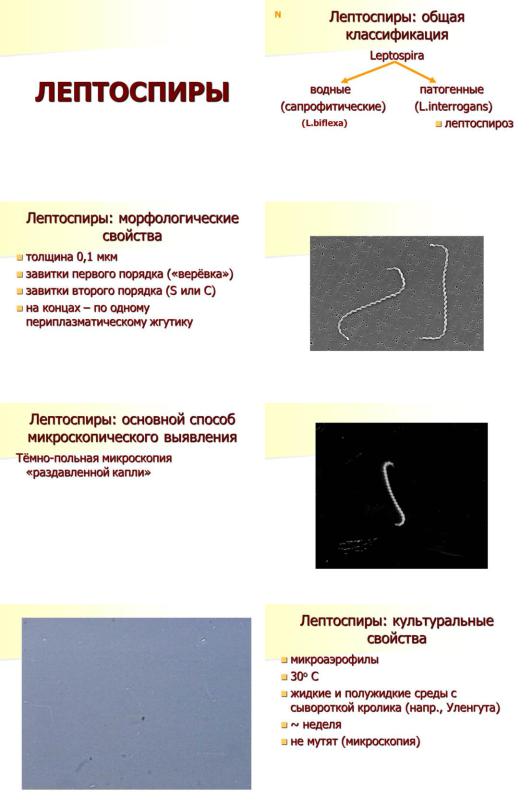
МДФд. Занятие № 26 |
- 21 - |
|
|
|
|
|
|
|
|
МДФд. Занятие № 26 |
- 22 - |
|
|
|
|
|
|
|
|
МДФд. Занятие № 26 |
- 23 - |
|
|
|
|
|
|
|
|

МДФд. Занятие № 26 |
- 24 - |
|
|
|
|
|
|
|
|
|
|

МДФд. Занятие № 26 |
- 25 - |
МДФд-26В. Теоретический материал
ОБЩАЯ ХАРАКТЕРИСТИКА СПИРОХЕТ
Спирохеты – это извитые формы бактерий, длинные (3-500 мкм) и тонкие (до 0,1 мкм).
По сравнению с остальными бактериями, спирохеты имеют уникальную ультраструктуру: цитоплазматический цилиндр у них переплетен с одной или несколькими осевыми фибриллами, состоящими из флагеллина, один конец которых прикреплен к субтерминальному диску (блефаропласту, как у простейших). На противоположенных концах клетки спирохет расположены по блефаропласту, соответственно две фибриллы (или два пучка фибрилл) направлены друг навстречу другу с противоположенных концов клетки и пересекаются в ее середине, а затем выходят за пределы клетки, уподобляясь жгутикам обычных бактерий. Из-за того, что у большинства спирохет сократительные фибриллы располагаются в периплазматическом пространстве (а клеточная стенка у них – грамотрицательного типа), их часто называют периплазматическими жгутиками.
Вследствие такого устройства спирохеты двигаются за счет сокращения самого тела клетки, совершая вращательные, сгибательные и штопорообразные (винтообразные) движения.
Патогенные спирохеты относятся к порядку Spirochaetales. Роды Treponema и Borrelia вхо-
дят в семейство Spirochaetaceae, род Leptospira – в одноименное семейство Leptospiraceae.
Спирохеты, кроме боррелий, плохо воспринимают анилиновые красители. Основной (и дифференцирующий) метод их окраски – по Романовскому-Гимзе. Для выявления в патологическом материале трепонем используют также обработку по Морозову. Для обнаружения спирохет (особенно – лептоспир) широко используется темнопольная микроскопия.
ТРЕПОНЕМЫ
Род Treponema содержит три патогенных для человека вида: T. pallidum, T. carateum и T. vincentii.
T. pallidum содержит три подвида: pallidum (вызывает сифилис), pertenue (вызывает тропическую гранулему, или фрамбезию) и endemicum (вызывает беджель, или эндемичный сифилис).
T. carateum является возбудителем пинты (карате).
T. vincentii в ассоциации с Fusobacteriumnucleatum вызывает язвенно-некротическую анги-
ну.
T. pallidum, var. pallidum имеет от 8 до 14 равномерных завитков, от обеих концов клетки отходят по три периплазматических жгутика. Возбудитель сифилиса может образовывать L- формы, а также цисты (представляющие собой свернутые в шар трепонемы, покрытые непроницаемой муциновой оболочкой). По Романовскому-Гимзе окрашиваются в бледно-розовый цвет.
Возбудитель сифилиса растет (медленно) на средах с почечной или мозговой тканью в строго анаэробных условиях при 350С, но теряет при этом вирулентность и изменяет другие свои свойства. Такие трепонемы называются «культуральными». Для того, чтобы получить культуру T. pallidum с сохраненными свойствами, ее культивируют в ткани яичка кролика; такие трепонемы называются «тканевыми».
Биохимические свойства возбудителя сифилиса изучены мало.
Антигенная структура T. pallidum, var. pallidum сложна и плохо изучена. Известны два основных антигена: трепонематозный (специфический), представляющий собой термолабильный белок, и липоидный (неспецифический), который идентичен липоидному экстракту бычьего сердца.
Вирулентность возбудителя сифилиса определяет его устойчивость к фагоцитозу, высокая
МДФд. Занятие № 26 |
- 26 - |
инвазивная активность, эндотоксин и липопротеины (последние участвуют в развитии иммунопатологических процессов).
СИФИЛИС
Размножения возбудителя в месте внедрения сопровождается развитием здесь твердого шанкра (язвы) и, вследствие лимфогенной миграции трепонем, – регионального лимфоаденита. Эти два основных клинических признака определяют картину первичного сифилиса. Через некоторое время шанкр зарастает и наступает период видимого выздоровления, прерываемый появлением сыпи, как внешнего проявления генерализации инфекции гематогенным путем. Эта стадия заболевания определяется как вторичный сифилис. Диссеминация T. pallidum по различным органам сопровождается образованием в них гранулем (гумм), характерных для третичного сифилиса. И, наконец, в случае поражения центральной нервной системы, развивается нейросифилис (его иногда называют четвертичным сифилисом).
Вцелом, сифилис является циклическим заболеванием, для которого характерно последовательная (правда, не всегда) смена стадий (периодов), с образованием возбудителем в организме больного L-форм и цист.
Втечение сифилиса различают инкубационный период, первичный сифилис, вторичный сифилис, третичный сифилис и нейросифилис (четвертичный сифилис).
Инкубационный период при сифилисе длится от 10 до 90 суток (в среднем – 24 дня).
При первичном сифилисе в месте внедрения возбудителя, как уже говорилось, образовывается язва на хрящевидной основе – твердый шанкр. Через 7-10 суток развивается региональный лимфаденит. Постепенно твердый шанкр заживает и рубцуется.
Вторичный период сифилиса наступает через 6-7 недель после появления твердого шанкра
ихарактеризуется рецидивирующей сыпью. У 25% больных после этого периода наступает выздоровление, у 25% болезнь переходит в латентную фазу, которая длится от 3 до 30 лет, а у 50% – развивается третичный сифилис.
Третичный сифилис наступает обычно через 3-4 года после заражения. Распад и рубцевания образовывающихся на этой стадии заболевания гумм (гранулем) может привезти к серьезным нарушениям функции внутренних органов, в связи с чем этот период часто называют висцеральным сифилисом.
Нейросифилис развивается у некоторых больных при неадекватном лечении, наступает в среднем через 8-15 лет после заражения и характеризуется тяжелым поражением ЦНС со смертельным, как правило, исходом.
При инфицировании плода во вторую половину беременности или при инфицировании ребенка при прохождении через родовые пути больной женщины, развивается врожденный сифилис.
При этом внутриутробное инфицирование плода может привести к выкидышу или мертворождению. В случае рождения жизнеспособного ребенка, у него развивается или ранний врожденный сифилис (клинические проявления болезни развиваются сразу после рождения) или поздний врожденный сифилис (клинические проявления болезни развиваются через 5-15 лет).
Восприимчивость человека к сифилису очень высока.
Клеточный иммунный ответ, формирующийся во время заболевания, и развивающаяся инфекционная аллергия (ГЗТ) способствуют фиксации возбудителя (образование гранулем), но не способны элиминировать его из организма. Гуморальный иммунный ответ при сифилисе не эффективен. Постинфекционный иммунитет не формируется (сифилис – пример заболевания, при котором формируется так называемый нестерильный иммунитет).
С особенностями иммунитета и особыми свойствами возбудителя связан и рецидивирующий характер сыпи при вторичном сифилисе: на высоте иммунного ответа T. pallidum, уходя от действия антител, образовывает цисты, которые локализуются в сосудистой стенке – наступает стадия ремиссии; при снижении напряженности (в отсутствие контакта иммунного системы с трепонематозным антигеном) иммунного ответа, трепонемы возвращаются в вегетативную форму, что и обуславливает рецидив сыпи. Так происходит при вторичном сифилисе несколько раз.
Источником инфекции при сифилисе служит больной человек (в первичной и вторичной стадии болезни). Основной механизм передачи – контактный (чаще – половой), дополнительный механизм передачи – трансплацентарный (начиная с 5 месяца беременности).
Возбудитель сифилиса малоустойчив вне организма человека, чувствителен к дезинфектантам, но долго сохраняется во влажной среде (в матерчатых тканях, например, до 50 суток).
Неспецифическая профилактика сифилиса заключается в своевременном выявлении и лечении больных, целеноправленном обследовании доноров, беременных (для претовлащения возникновения врожденного сифилиса беременную женщину необходимо вылечить в первую половину беременности), групп риска (наркоманов, лиц, практикующих промискуитет); постоянный половой партнер – это тоже один из способов профилактики заболевания сифилисом.
МДФд. Занятие № 26 |
- 27 - |
Специфическая профилактика сифилиса не разработана.
Для лечения сифилиса используют антибиотики пенициллинового ряда. Микробиологическая диагностика сифилиса основана на бактериоскопическом методе, ко-
торый применяют при первичном (микроскопируютотделяемое шанкра, пунктат региональным лимфатических узлов) и, реже, вторичном (микроскопируют соскобы с элементов сыпи) сифилисе. Во всех периодах развития болезни, начиная с 4 недели заболевания, применяют серологический метод диагностики, выявляя соответствующие антитела в сыворотке крови, а при нейросифилисе
– и в ликворе.
Микроскопируютнативныйпрепарат а темном поле, мазок, длительно окрашенный по Ро- мановскому-Гимзе, препарат, обработанный серебрением (по Морозову).
При оценке микроскопической картины необходимо оттидеренцировать возбудитель сифилиса от нитей фибрина, а также от сапрофитических трепонем.
Из последних на наружных половых органах в норме обитает T. refringens (для которой характерны выраженная подвижность и отсутствие сгибательных движений), а в ротовой полости –
T.denticola (с короткими завитками, имеющими остроугольную форму).
Всерологическом методе диагностики сифилиса применяют неспецифические (с кардиолипиновым антигеном) и специфические (с трепонематозным антигеном) тесты. К первым относится реакция преципитации на стекле, применяемая для предварительного обследования. Ко вторым – реакция иммобилизации, РИФ, ИФА, РНГА. Наиболее широко применяемая серологическая реакция для диагностики сифилиса – реакция связывания комплемента в модификации Вассермана, которую можно ставить как с кардиолипиновым, так и с трепонематозным антигенами.
БЫТОВЫЕ ТРЕПОНЕМАТОЗЫ
Фрамбезия распространены в тропических странах. Пинта формирует эндемические очаги в прибрежных районах центральной Америки, экваториальной Африки, южной Азии. Эндемические очаги беджеля существуют в Африке, на Балканах, в Турции, на Аравийском полуострове, в Индии, Пакистане, Австралии, Гаити.
Основной путь передачи бытовыхтрепонематозов – контактный (очень редко – половой), через поврежденные кожные покровы. Фрамбезия и пинта могут передаваться мухами. Беджелем наиболее часто болеют дети 2-10 лет.
Клиническая картина фрамбезии схожа с сифилисом, прогноз благоприятный, хотя заболевание может затягиваться до 30 лет. Развивается стойкий постинфекционный иммунитет.
При пинте на коже появляются красные или сине-фиолетовые пятна с последующим формированием на их месте очагов депигментации. Может развиваться полиаденит, реже – поражения внутренних органов, нервной системы и костей.
Клиническая симптоматика беджеля схожа с клиникой вторичного и третичного сифилиса, но поражения внутренних органов не развиваются.
Диагностики бытовых трепонематозов проводится с учетом клинических и эпидемиологических особенностей соответствующего заболевания. Из микробиологических методов используется микроскопия и обнаружение специфических антител (с помощью РСК, РИФ).
Лечение бытовыхтрепонематозов аналогично лечению сифилиса.
БОРРЕЛИИ
Патогенные для человека боррелии можно разделить на три основные группы: возбудитель эпидемического возвратного тифа, передающийся платяной вошью, возбудители клещевых спирохетозов, передающиеся клещами-орнитодоринами, и возбудители болезни Лайма, передающимися иксодовыми клещами.
Внешне боррелиипохожи на червей, являются строгими анаэробами, культивируются на средах с животными белками и в куриных эмбрионах.
Антигенная структура боррелий очень сложная, для них характерна чрезвычайная антигенная вариабельность вследствие присущей этим микроорганизмам способности к внутригеномной рекомбинации генов, детерминирующих антигенные свойства.
ЭПИДЕМИЧЕСКИЙ ВОЗВРАТНЫЙ ТИФ
Возбудителем эпидемического возвратного тифа является обитающая в гемолимфе платя-
ных вшей Borreliarecurrentis.
Borreliarecurrentis, попадая с укусом инфицированной вши в организм человека, размножа-
МДФд. Занятие № 26 |
- 28 - |
ется здесь в клетках лимфомакрофагальной системы. При достижении определенного уровня концентрации, боррелии выходят из клеток в кровь, что приводит к усиленной выработке защитных антител. Специфические антитела, во-первых лизируют возбудитель, что приводит к появлению в кровяном русле продуктов распада боррелий и развитии, как результат, лихорадки (собственно, приступ тифа). После того, как кровь очищается от боррелий, лихорадка спадает (наступает период нормальной температуры). Однако, боррелии, в силу своей способности к антигенной изменчивости, успевают, путем изменения антигенного состава, «уйти» от действия антител и часть их популяции сохраняется в организме, продолжая размножаться внутриклеточно. Со временем новый серовар вновь выходит в кровь, вызывая новый приступ лихорадки, и вся цепочка событий повторяется снова. Чередование приступов лихорадки с периодами нормальной температуры будет продолжаться до тех пор, пока все образующиеся серовары возбудителя не будут уничтожены. Обычно при эпидемическом возвратном тифе регистрируется 5-6 таких приступов.
Кроме того, антитела вызывают агрегирование боррелий с тромбоцитами, вызывая нарушения местного кровообращения.
При микробиологической диагностике возвратного тифа на высоте приступа лихорадки берут кровь, микроскопируют ее, и в случае обнаружение боррелий, поставив предварительный диагноз, заражают морскую свинку. Через 2-4 суток у морской свинки берут кровь для микроскопии. Обнаружение боррелий свидетельствует, что морская свинка больна, что, в свою очередь, свидетельствует о наличии у пациента эндемического возвратного тифа (клещевого спирохетоза). Отсутствие в крови лабораторного животного боррелий означает, что у пациента – эпидемический возвратный тиф (поскольку Borreliarecurrentis не патогенна для морской свинки и, соответственно, не вызывает у нее спирохетемии).
КЛЕЩЕВЫЕ СПИРОХЕТОЗЫ (ЭНДЕМИЧЕСКИЕ ВОЗВРАТНЫЕ ТИФЫ)
Эндемичные очаги клещевых спирохетозов (эндемических возвратных тифов) расположены на всех континентах, кроме Австралии. В каждом природном очаге циркулирует свой вид и вариант возбудителя.
К возбудителям клещевых спирохетозов относятся B. duttoni, B. uzbekistanica, B. persica, B. caucasica и другие виды боррелий, отличающиеся друг от друга своей антигенной структурой.
БОЛЕЗНЬ ЛАЙМА
Возбудителями болезни Лайма являются три вида боррелий, отличающиеся друг от друга антигенной структурой: B. burgdorferi, B. garinii и B. afzelii.
Источники инфекции – мелкие грызуны, олени, лоси. Переносчики – клещи рода Ixodes, ареал обитания которых и определяет район распространения болезни Лайма.
Инфицирование происходит при укусе клеща (возбудители содержаться в слюне насекомого). В месте укуса возникает папула, боррелии проникают в кровь и вызывают поражения внутренних органов, в патогенезе которых определенную роль играет аутоиммунный компонент.
В общих чертах, болезнь Лайма начинается как локальное поражение кожи в виде кольцевой мигрирующей эритемы, после чего развивается хронический процесс с поражением суставов, сердечнососудистой системы, нервной системы.
Более подробно клинические проявления болезни лайма можно классифицировать на три группы.
Начинается все с локального поражения кожи в месте укуса с формированием кольцевой мигрирующей эритемы (мигрирующей она названа потому, что меняет и свои размеры и свои очертания).
Через несколько недель или месяцев развиваются диссеминированные поражения, в процесс вовлекаются суставы, нервная система, сердечнососудистая система, опорно-двигательный аппарат.
Через несколько месяцев или лет развивается третья стадия болезни: развиваются артриты, поражения сердечнососудистой системы, у детей – менингиты или менингоэнцефалиты, у взрослых – мононевриты; редко – тромбозы артерий.
Выделить культуру возбудителя из ткани эритемы, крови, ликвора хоть и возможно, но трудно. Можно выявить наличие специфического антигена в ткани эритемы с помощью РИФ. На практике более доступен серологический метод диагностики: с помощью иммуноблоттинга на 3-6 неделе после инфицирования выявляют IgM, а через несколько месяцев после инфицирования – IgG. Можно также использовать ПЦР.
МДФд. Занятие № 26 |
- 29 - |
ЛЕПТОСПИРЫ
Все многочисленные серовары лептоспир объединены в два рода: сапрофитические обитатели водоемов – в вид L. biflexa, а патогенные для человека возбудители лептоспироза – в вид
L.interrogans.
Толщина лептоспир составляет 0,1 мкм, что меньше разрешающей способности светового микроскопа. Увидеть их в нем позволяет то, что клетка лептоспир формирует очень тесные завитки (так называемые, завитки первого порядка), превращающие бактерию в некое подобие витой веревки. В световой микроскоп видна фактически не толщина клетки лептоспиры, а амплитуда ее первичных завитков. Патогенные лептоспиры, кроме того, изгибаются своими концами, формируя своеобразные крючья, или завитки второго порядка, направленные или в разные стороны (тогда клетка лептоспиры становится похожа на латинскую букву S) или – в одну (и тогда клетка лептоспир становится похожа на букву С). На обеих полюсах клетки их нее выходит по одному периплазматическому жгутику.
Из-за их чрезвычайно малой толщины, основным способом микроскопического выявления лептоспир является темнопольная микроскопия препарата «раздавленная капля».
Лептоспиры относятся к микроаэрофилам, они культивируются при 300С на жидких и полужидких питательных средах с сывороткой кролика. Самая простая из этих сред – среда Уленгута, представляющая собой водопроводную воду с добавлением кроличьей сыворотки. Растут лептоспиры долго, примерно неделю, видимых изменений среды культивирования не вызывают – чтобы обнаружить их рост, каплю среды микрокопируют «в темном поле».
Вид L.interrogans включает в себя более 200 сероваров, объединенных в 38 серогрупп. На территории СНГ встречаются 27 сероваров патогенных лептоспир, относящиеся к 13 серогруппам.
Лептоспиры чувствительны к действию прямого солнечного света, высокой температуры, высушиванию, дезинфектантам. Долго (до 200 суток) сохраняются в заболоченной почве.
Основной фактор вирулентности лептоспир – эндотоксин, ответственный за развитие общей интоксикации и геморрагий. Высокая подвижность лептоспир обеспечивает их высокую инвазивность. Кроме того, вирулентность лептоспир обусловлена их устойчивостью к фагоцитозу и наличием таких ферментов вирулентности, как фибринолизин, плазмокоагулаза, липаза, а также цитотоксинами и гемолизином.
Распространены лептоспиры повсеместно.
ЛЕПТОСПИРОЗ
Из организма инфицированных животных лептоспиры с мочой попадают на объекты окружающей среды, контакт с которыми человека (через слизистые оболочки и поврежденную кожу) приводит к его заражению. Наиболее часто лептоспироз передается через воду (не зря его называют еще «водной лихорадкой»). Кроме того, возможна передача через почву и пищевые продукты.
Ворганизм человека L.interrogans проникает через кожные покровы и слизистые оболочки в лимфу, затем попадает в лимфоузлы и появляется в крови. Дальнейшее зависит от клинической формы заболевания. При поражении сосудов развиваются геморрагии, печени – желтуха, при поражении почек лептоспиры присутствуют в моче, а о поражении лептоспирами ЦНС свидетельствует симптоматика менингизма.
Множественные геморрагии при лептоспирозе возникают из-за повышения проницаемости сосудистой стенки вследствие механического воздействия возбудителей на эндотелий.
Поражение лептоспирами печени обусловлено, во-первых, механическим повреждением гепатоцитов активно подвижными лептоспирами, а во-вторых – токсическим действием метаболитов и продуктов распада бактериальных клеток.
Избирательное депонирование лептоспир на поверхности эпителиальных клеток почек и в межклеточном пространстве тканей этого органа вызывает тяжелое повреждение почечных канальцев и, как следствие, нарушение мочеобразования.
Менингиальные явления при лептоспирозе обусловлены как непосредственным действием на ЦНС самих бактерий, так и действием их токсинов и продуктов распада бактериальных клеток.
Для иммунопрофилактики лептоспироза используют убитую поливалентную вакцину и иммуноглобулин.
При микробиологической диагностике лептоспироза патологический материал микроскопируют, выделяют культуру на питательных средах и проводят биопробу. Два последних метода позволяют поставить окончательный диагноз. Выявляют также специфические антитела в сыворотке крови. Можно использовать ПЦР.
Вкачестве патологического материала при лептоспирозе на первой неделе берут кровь, со второй недели – мочу, при менингиальных симптомах – ликвор.
МДФд. Занятие № 26 |
- 30 - |
Микроскопический метод диагностики лептоспироза заключается в микроскопировании в темном поле препарата «раздавленная капля». Однако, этот метод при лептоспирозе малочувствителен и недостаточно специфичен.
В культуральном методе чаще всего используется среда Уленгута. Каждые два дня каплю среды микроскопируют для выявления роста лептоспир. Полученную культуру идентифицируют с помощью реакции микроагглютинации и лизиса.
При биологическом методе диагностики лептоспироза патологическим материалом внутрибрюшинно заражают морскую свинку. За животным наблюдают, признаками его заболевания являются потеря веса и появление желтухи. Экссудат из брюшной полости заболевшей морской свинки используют для выделения культуры или для непосредственного обнаружения в нем лептоспир с помощью реакции микроагглютинации и лизиса.
Серологический метод диагностики лептоспироза проводят со второй недели заболевания. Используется реакция микроагглютинации и лизиса, РСК с поливалентнымдиагностикумом, так как между различными сероварами лептоспир нет перекрестного иммунитета. При лептоспирозе титр антител достигает очень больших величин и долго сохраняется на высоком уровне.
МДФд-26Г. Тестовые вопросы по теме занятия
Хронический гастрит вызывают: трепонемы боррелии лептоспиры спириллы волинеллы кампилобактеры -хеликобактеры
Язвенную болезнь желудка и двенадцатиперстной кишки вызывают: трепонемы боррелии лептоспиры спириллы волинеллы кампилобактеры -хеликобактеры
Грамотрицательные изогнутые (2-3 изгиба) подвижные палочки, часто располагающиеся в мазке попарно:
трепонемы
боррелии
лептоспиры
спириллы
волинеллы -кампилобактер -хеликобактер
Температура культивирования – 42С: трепонемы боррелии лептоспиры спириллы волинеллы -кампилобактер хеликобактер
Какие бактерии культивируются на искусственных питательных средах приповышенной концентрации углекислого газа и пониженной концентрации кислорода:
трепонемы
боррелии
лептоспиры
спириллы
волинеллы -кампилобактер
