
МДФд_10
.pdfМДФд. Занятие № 10 |
- 11 - |
фельда-Якоба) инфекции.
Б. Формирование в современной человеческой популяции большой доли иммунодефицитных генотипов имеет следствием заметное возрастание к концу ХХ века заболеваемости инфекци-
онными болезнями.
В. Для современного человечества, особенно – населения т.н. «развитых» стран, характерно зна-
чительное число (до 20%) больных аллергиями, а такие состояния – тоже предмет рассмот-
рения иммунологии.
Г. Недостаток иммунологических знаний практических врачей явился причиной упрощенного отношения к вакцинации. Увы, но представление, что от вакцинации одна лишь польза является заблуждением и заблуждением вовсе не безобидным.
Д. Тот же недостаток иммунологических знаний обуславливает и неоправданно легкое назначение иммуностимуляторов, оправдываемое пагубным представлением о том, что «чем больше иммунитета, тем лучше для больного».
Е. Наконец, или иммунологические идеи или методы диагностикииспользуются сегодня врачами всех специальностей.
23.2. Понятие об иммунитете Под иммунитетом понимают защитные механизмы, которые реализуются с участием лимфоци-
тов и направлены на распознавание и элиминацию из внутренней среды организма группы молекул или даже частей молекул, рассматриваемые как «чужеродная метка». Для обозначения такой метки, которую иммунитет расценивает как «свое» или «чужое», используется термин антиген. Распознавая эти «метки» – антигены, иммунитет удаляет из внутренней среды организма:
собственные, ставшие по разным причинам ненужными, клетки,
микроорганизмы,
пищевые, ингаляционные и аппликационные внешние вещества,
трансплантаты.
23.3. Разделы современной иммунологии Современная иммунология – развитая и высокоструктурированная наука, включающая в виде са-
мостоятельных разделов молекулярную иммунологию, клеточную иммунологию, иммунохимию, физиологию иммунитета, иммуногенетику, эволюционную иммунологию, вакцинологию, аллергологию, иммуноонкологию, трансплантационную иммунологию, иммунопатологию, иммуногематологию. Однако, прежде всего следует обратить внимание на разделение иммунологии на две части, в зависимости от того, о каком антигене идет речь.
А. Защитные механизмы, направленные на распознавание и элиминацию микробного антигена (бактериального, вирусного, грибкового, принадлежащего простейшим и гельминтам), изучает
инфекционная иммунология.
Б. Защитные механизмы, направленные на распознавание и элиминацию всякого иного антигена (например, трансплантата) изучает неинфекционная иммунология.
24. ОБЩАЯ ХАРАКТЕРИСТИКА ФАКТОРОВ И МЕХАНИЗМОВ ЗАЩИТЫ ЧЕЛОВЕКА ОТ ПАТОГЕННЫХ ОБЪЕКТОВ
24.1. Уровни защиты человеческого организма от инфекций Защита человеческого организма от инфекционного начала (микроорганизма), как и от неинфек-
ционных антигенов окружающей среды, осуществляется на трех уровнях (тремя группами способов или механизмов).
А. Первый уровень защиты осуществляется еще до попадания инфекционного начала во внутреннюю средумакроорганизма.
1.Ментальная поведенческая защита включает в себя избегать контактов с зараженными лицами, стремление одеваться в зависимости от погодных условий, мыть руки и т.п.
2.Покровные ткани (кожа и слизистые оболочки) в норме – т.е. при сохраненной целостности
– не проницаемы для подавляющего числа патогенных микроорганизмов.
Б. Следующий уровень защиты осуществляется на границе с внутренней средоймакроорганизма.
1.Покровные ткани кроме механической защиты от патогена, угнетают жизнедеятельность попавших на них микробов за счет так называемых микробоцидныхэкзосекретов. К ним относится соляная кислота желудочного сока, бактерицидные компоненты слюны, секрета сальных и потовых желез, литические пищеварительные ферменты кишечника и т.п.
2.Защитную роль играют также сосудистые реакции, вызывающие быстрый локальный отек в очаге поражения.
В. И, наконец, основной уровень защиты осуществляется макроорганизмов уже в своей внутрен-
нейсреде.
МДФд. Занятие № 10 |
- 12 - |
1.Инфекционный патоген уничтожается с помощью первичного (доиммунного) фагоцитоза.
2.Во внутренней среде действуют белки острой фазы и другие микробоцидные вещества.
3.В случае неэффективности всего перечисленного вступает в дело самый совершенный и эффективный механизм защиты от инфекционного начала – лимфоцитарный иммунитет.
24.2. Механизмы защиты внутренней среды человеческого организма, реализуемые в ней самой Остановимся более подробно на тех механизмах защиты человеческого организма от инфекционного начала, которые реализуются во внутренней среде макроорганизма. Эти механизмы классифицируются (правда, как мы увидим ниже, условно) на доиммунные и иммунные.
А. Доиммунные механизмы – это все те механизмы защиты, которые осуществляются и без участия лимфоцитов. Эти факторы называются еще факторами неспецифической резистентности. Именно они формируют так называемый естественный иммунитет (или неспецифическую резистентность), уровень которого у всех людей примерно одинаков, так как дан нам природой в качестве видового признака Homosapiens.
1.К клеточным факторам неспецифической резистентности относятся фагоциты и другие лейкоциты общевоспалительного назначения. Кроме того, в качестве фактора неспецифической резистентности могут выступать и NK-клетки.
2.К гуморальным факторам неспецифической резистентности относятся комплемент, лизоцим, белки острой фазы, пептиды-антибиотики и другие микробоцидные вещества внутрен-
ней среды макроорганизма.
Б. Иммунные механизмы защиты осуществляют лимфоциты. Именно они – действующее начало того явления, которое определяется термином «иммунитет». Именно эти механизмы обуславли-
вают иммунологическую реактивность и определяют формирование приобретенного иммуни-
тета. Приобретенный иммунитет формируется в течение жизни конкретного индивидуума и его уровень, в отличие от естественного иммунитета, индивидуален для каждого человека.
24.3. Уникальные свойства лимфоцитов Лимфоцит – уникальная клетка макроорганизма, которая отличается от всех других клеток четырьмя основными свойствами.
А. Лимфоциты могут взаимодействовать со всеми клеткамимакроорганизма.
1.В кровяном русле они взаимодействуют с клетками крови и клетками эндотелия сосудов.
2.Проникая через стенки сосудов в ткани, они могут взаимодействовать со всеми другими клетками – практически всех тканей и всех систем (за исключением клеток ороговевшего эпителия и так называемых забарьерных тканей).
Б. Через специфические рецепторы лимфоциты воспринимают информацию от нервной и эндокринной систем, обеспечивая тесное функциональное единство иммунной, нервной и эндокринной систем макроорганизма.
В. Лимфоциты обладают механизмом молекулярного распознавания антигена (см. следующий раздел).
Г. Лимфоциты могут «запоминать» антиген, обеспечивая при повторном контакте с ним более быстрый и сильный защитный эффект (так называемый вторичный иммунный ответ). Это явление называется иммунологической памятью и о нем будет более подробно рассказано ниже.
24.4. Молекулярное распознавание Молекулярное распознавание – уникальное свойство лимфоцитов распознавать антиген (т.е. взаи-
модействовать с ним). Так как антиген – это молекула или даже часть молекулы, то его распознавание (т.е., повторимся, взаимодействие) происходит по определению на молекулярном уровне. Молекулярное распознавание осуществляется специфическим антигенраспознающим рецептором лимфоцита. В конце ХХ века считалось, что на одном конкретном лимфоците все антигенраспознающие рецепторы – одной специфичности. Другими словами с конкретным антигеном может взаимодействовать, т.е. распознавать его, только один клон лимфоцитов – та клетка (и ее потомки), которая несет антигенраспознающий рецептор соответствующей специфичности. Примерно с 2000 г. это положение уточнено: антигенраспознающий рецептор лимфоцита – живой и гибкий, поэтому один и тот же клон лимфоцитов может взаимодействовать с несколькими антигенами (т.е. распознавать их). Тем не менее, наибольшее соответствие он имеет с одним конкретным антигеном и именно с ним взаимодействует наиболее полно, а, следовательно, наиболее эффективно его распознает. В этом заключается, забегая вперед, клональный принцип действия иммунной системы.
24.5. Виды приобретенного иммунитета Существует классификация приобретенного иммунитета в зависимости от его происхождения, со-
гласно которой он подразделяется на естественный (не путать с естественным иммунитетом, обусловленным факторами неспецифической резистентности) и искусственный.
МДФд. Занятие № 10 |
- 13 - |
А. Естественный приобретенный иммунитет формируется естественным путем (откуда и название).
1.Активный естественный приобретенный иммунитет формируется в результате перенесенной инфекции и поэтому называется постинфекционным.
2.Пассивный естественный приобретенный иммунитет формируется за счет материнских антител, поступающих в организм плода через плаценту, а после рождения – в организм ребенка с материнским молоком. Вследствие этого этот вид иммунитета называется материнским.
Б. Искусственный приобретенный иммунитет формируется у пациента врачом.
1.Активный искусственный приобретенный иммунитет формируется в результате вакцинации и поэтому называется поствакцинальным.
2.Пассивный искусственный приобретенный иммунитет формируется в результате введения лечебно-профилактических сывороток и поэтому называется постсывороточным.
24.6. Механизм осуществления иммунологической реактивности Иммунологическая реактивность осуществляется в результате взаимодействия органов, клеток и молекул иммунной системы в ходе иммунного ответа.
24.7. Принципиальные отличия иммунологической реактивности от неспецифической резистентности
В завершение общей характеристики факторов и механизмов защиты человека от патогенных объектов к месту будет, на наш взгляд, акцентировать внимание на принципиальных отличиях иммунологической реактивности (т.е. собственно иммунитета) от неспецифической резистентности.
А. Факторы иммунологической реактивности обладают высокой специфичностью. Если, к примеру, кожа как фактор неспецифичной резистентности защищает и от дифтерийной палочки и от вируса гриппа с одинаковым эффектом, то те факторы иммунологической реактивности, которые формируют иммунный ответ против дифтерийной палочки, практически не будут участвовать в формировании иммунного ответа против вируса гриппа.
Б. Для факторов иммунологической реактивности характерно активация антигеном. Т.е. сам контакт с антигеном приводит к активации того клона лимфоцитов, который и обеспечивает формирование иммунного ответа против этого конкретного антигена.
В. Факторам иммунологической реактивности, а именно – лимфоцитам, как уже упоминалось, свойственна иммунологическая память, которая и обуславливает возможность формирования вторичного иммунного ответа.
25. ЕСТЕСТВЕННЫЙ ИММУНИТЕТ
25.1. Факторы естественного иммунитета (неспецифической резистентности) Охарактеризуем основные факторы неспецифической резистентности (естественного иммунитета), действующие во внутренней среде макроорганизма, о которых уже говорилось в разделе 24.2 (наиболее важным из них – комплементу и фагоцитам будут посвящены особые разделы).
А. Эндогенные пептиды-антибиотики состоят из 13 – 18 аминокислот и обладают бактерицидным эффектом. У эукариотических организмов описано около 400 эндогенных пептидовантибиотиков. У млекопитающих (включая человека) к этой группе веществ относятся дефензи-
ны.
1.Альфа-дефензины концентрируются в гранулах нейтрофилов.
2.Бета-дефензины синтезируются клетками эпителия дыхательных путей и желудочнокишечного тракта.
Б. Пропердин является одним из белков γ-глобулиновой фракции сыворотки крови. Пропердин, являясь одним из факторов системы комплемента («фактор Р»), способствует его активации по альтернативному пути, стабилизируя соответствующую конвертазу (см. ниже).
В. Лизоцим – протеолитический фермент секрета слизистых оболочек и некоторых других биологических жидкостей макроорганизма (в частности, содержится в крови). Лизоцим разрушает клеточную стенку бактерий, активирует фагоцитоз и антителообразование, участвует в механизмах внутриклеточнойцитотоксичности фагоцитов.
Г. Бета-лизины – белки сыворотки крови. Синтезируются тромбоцитами. Антимикробное действие β-лизинов обуславливается повреждением бактериальной цитоплазматической мембраны.
Д. Фибронектин – белок плазмы крови и тканевой жидкости. Синтезируется макрофагами. С одной стороны, фибронектин связывается с поверхностью бактерий и обуславливает их неспецифическое выведение из макроорганизма. С другой стороны, фибронектин может взаимодействовать с рецепторами адгезии и тем самым блокировать процесс адгезии бактерий к чувствительным клеткам.
Е. Белки острой фазы – это особые белки сыворотки крови. В норме их содержание очень мало,
МДФд. Занятие № 10 |
- 14 - |
однако резко увеличивается при тяжелых системных воспалительных процессах. Синтезируются в печени под влиянием цитокинов. Наибольшее значение из них имеют С-реактивный белок (С-реактивный протеин, CRP) и маннансвязывающий (используется также вариант – маннозосвязывающий) лектин.
1.С-реактивный белок связывается с клеточной стенкой ряда бактерий и одноклеточных грибов, вызывая их опсонизацию и активируя на их поверхности комплемент по классическому пути.
2.Маннансвязывающийлектин (лектинами называют белки, способные с высокой прочностью связывать углеводы) опсонизирует микробную клетку для фагоцитоза моноцитами, а также вызывает активацию комплемента по лектиновому пути.
Ж. Интерфероны – низкомолекулярные белки. Являются и факторами неспецифической резистентности и, будучи цитокинами, молекулами иммунной системы.
1. Интерфероны классифицируются на три класса.
а. Альфа-интерфероны (α-ИФН) продуцируются лейкоцитами, оказывают противовирусное и противоопухолевое действие.
б. Бета-интерфероны (β-ИНФ) продуцируются фибробластами и оказывают противоопухолевое действие.
в. Гамма-интерфероны (γ-ИФН) продуцируются лимфоцитами и оказывают иммуномодулирующее действие.
2. Индукторами синтеза в макроорганизмеинтерферонов являются чужеродные белки, двухцепочечные РНК, вирусы, бактерии и продукты их жизнедеятельности, а также некоторые синтетические полимеры (например, полианионы).
З. NK-клетки представляют собой большие гранулированные лимфоциты, не относящиеся ни к Т- ни к В-лимфоцитам.
1.Существуют две субпопуляцииNK-клеток.
а. Циркулирующие в кровиNK-клетки уничтожают инфицированные вирусами клетки, на поверхность которых «сели» антитела (т.е. осуществляют так называемую антителозависимуюцитотоксичность, окоторой пойдет речь ниже).
б. ТканевыеNK-клетки локализуются в слизистых оболочках (особенно репродуктивных органов), красной пульпе селезенки, в печени (именно NK-клетки, расположенные в печени, представляют собой лимфоидный барьер для крови воротной вены, обеспечивая формирование иммунологической толерантности к пищевым антигенам).
2.NK-клетки осуществляют внеклеточный киллинг опухолевых и других клеток, несущих чужеродный антиген (но, в отличие от цитотоксических лимфоцитов, без предварительной сенсибилизации – другими словами, можно сказать, активации – антигеном).Механизм внеклеточного киллинга обусловлен действием на клетку-мишень синтезируемых NK-клетками специфических белков – перфоринов, которые формируют в оболочке клетки-мишени трансмембранные каналы (аналогично действию мембранатакующего комплекса комплемента).
а. Через формируемые перфоринами трансмембранные каналы впрыскиваются гранзимы – белки, также синтезируемые NK-клетками. Гранзимы активируют в клетке-мишени каспазы (сериновые протеазы), которые, в свою очередь, активируют эндонуклеазы, осуществляющие фрагментацию ДНК. Другими словами, NK-клетки запускают в клетке-мишени процесс апоптоза.
б. Разрушение клетки-мишени происходит также и за счет осмолиза, что приводит к некрозу.
25.2. Роль лихорадки в неспецифической резистентности Кроме перечисленных факторов, большую роль в неспецифической резистентности играет лихо-
радка (т.е. повышение температуры), которая есть ни что иное, как нормальная защитная реакция макроорганизма от внедрившегося в его внутреннюю среду патогена. Механизм поднятия температуры в ответ на внедрение инфекционного агента заключается в следующем (рис.25.2-1).

МДФд. Занятие № 10 |
- 15 - |
Рис. 25.2-1. Роль лихорадки в неспецифической резистентности (объяснения в тексте)
А. Микроорганизм содержит в своем составе или продуцирует в процессе своей жизнедеятельности так называемые экзогенные пирогены: эндотоксин, белковые токсины, пептидогликан и др.
Б. Экзогенныепирогены стимулируют продукцию фагоцитами эндогенного пирогена – интерлей- кина-1 (ИЛ-1).
В. Действие ИЛ-1 в макроорганизмемноговекторно и не ограничивается только повышением температуры тела – лихорадка является лишь одним из эффектов действия этого цитокина.
1.Действие ИЛ-1 на центральную нервную систему (а именно на гипоталамус) приводит к повышению температуры тела, что, в свою очередь активирует фагоцитоз.
2.Под влияние ИЛ-1 гепатоциты продуцируют большое количество С-реактивного белка, кото-
рый, в свою очередь, активирует комплемент.
3.ИЛ-1 вызывает также и активацию лимфоцитов.
Г. Все перечисленное служит одной главной цели – защита от попавшего во внутреннюю среду макроорганизма микроба.
26. СИСТЕМА КОМПЛЕМЕНТА
26.1. Общее понятие Комплемент – сложный белковый комплекс сыворотки крови.
А. Система комплемента состоит из 30 белков (компонентов, или фракций, системы комплемента).
Б. Активируется система комплемента за счет каскадного процесса: продукт предыдущей реакции исполняет роль катализатора последующей реакции. Причем при активации фракции компонента происходит, у первых пяти компонентов, ее расщепление. Продукты этого расщепле-
ния и обозначаются как активные фракции системы комплемента.
1.Больший из фрагментов (обозначаемый буквой b), образовавшихся при расщеплении неактивной фракции, остается на поверхности клетки – активация комплемента всегда происходит на поверхности микробной клетки, но не собственных эукариотических клеток. Этот фрагмент приобретает свойства фермента и способность воздействовать на последующий компонент, активируя его.
2.Меньший фрагмент (обозначается буквой a) является растворимым и «уходит» в жидкую
фазу, т.е. в сыворотку крови.
В. Фракции системы комплемента обозначаются по-разному.
1.Девять – открытых первыми – белков системы комплемента обозначаются буквой С (от английского слова complement) с соответствующей цифрой.
2.Остальные фракции системы комплемента обозначаются другими латинскими буквами или
их сочетаниями.
Г. Значение комплемента для макроорганизма велико и разнообразно (подробнее – см. раздел
26.6).
1.Часть активных фракций системы комплемента являются протеазами.
2.Некоторые – связываются с комплексом антиген-антитело (иммунным комплексом).
МДФд. Занятие № 10 |
- 16 - |
3.Другие – активируют тучные клетки и, связанные с ними сосудистые реакции воспаления.
4.И, наконец, часть фракций комплемента осуществляет перфорацию оболочек бактериальных клеток.
26.2. Пути активации комплемента Существуют три пути активации комплемента: классический, лектиновый иальтернативный.
А. Классический путь активации комплемента является основным. Участие в этом пути активации комплемента – главная функция антител.
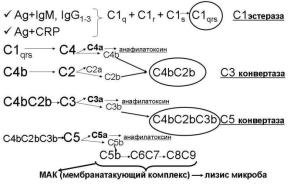
Рис 26.2-2. Схема классического пути активации комплемента
1.Активацию комплемента по классическому пути запускает иммунный комплекс: комплекс антигена с иммуноглобулином (класса G – первых трех подклассов – или М). Место антитела может «занять» С-реактивный белок – такой комплекс также активирует комплемент по классическому пути.
2.Классический путь активации комплемента осуществляется следующим образом (рис 26.2- 1).
а. Сначала активируется фракция С1: она собирается из трех субфракций (C1q, C1r, C1s) и превращается в фермент С1-эстеразу (С1qrs).
б. С1-эстераза расщепляет фракцию С4.
в. Активная фракция С4bковалентно связывается с поверхностью микробных клеток (но не с собственными эукариотическими клетками макроорганизма) с здесь присоединяет к себе фракцию С2.
г. Фракция С2 в комплексе с фракцией С4b расщепляется С1-эстеразой с образованием ак-
тивной фракции С2b.
д. Активные фракции С4b и С2bв один комплекс – С4bС2b – обладающий ферментативной активностью. Это так называемаяС3-конвертаза классического пути.
е. С3-конвертаза расщепляет фракцию С3, нарабатываю большие количества активной фракции С3b.
ж. Активная фракция С3bприсоединяется к комплексу С4bС2b и превращает его в С5-
конвертазу (С4bС2bС3b).
з. С5-конвертаза расщепляет фракцию С5.
и. Появившаяся в результате этого активная фракция С5bприсоединяет фракцию С6.
к. Комплекс С5bС6 присоединяет фракцию С7.
л. Комплекс С5bС6С7 встраивается в фосфолипидный бислой мембраны микробной клетки.
м. К этому комплексу присоединяется белок С8.
н. Будучи вместе со всем комплексом в фосфолипидный бислой мембраны микробной клетки,
белок С8 катализирует полимеризацию 10 – 16 молекул белка С9. Данный полимер фор-
мирует в мембране микробной клетки неспадающую пору диаметром около 10 нм (рис 26.2-2)., что приводит к лизису микроба (так как на его поверхности образуется множество таких пор – «деятельность» одной единицы С3-конвертазы приводит к появлению около 1000 пор). Комплекс С5bС6С7С8С9, образующийся в результате активации комплемента,
называется мемранатакующим комплексом (МАК).

МДФд. Занятие № 10 |
- 17 - |
|
|
|
|
Рис. 26.2-2. Схема образования МАК (слева) и результат активации комплемента – формирование поры в фосфолипидном бислое микробной мембраны, приводящей к осмотическому лизису микробной клетки (справа)
Рис 26.2-3. Схема лектинового пути активации комплемента
Б. Лектиновый путь активации комплемента запускается комплексом нормального белка сыворотки крови – маннансвязывающеголектина (МСЛ) – с углеводами поверхностных структур микробных клеток (с остатками маннозы). Активизирующаяся в результате этого процесса МСЛ-ассоциированная сериновая протеаза действует аналогично С1-эстеразе классического пути, по которому, собственно, и развиваются дальнейшие события, заканчивающиеся формированием МАК (рис. 26.2-3).
В. Альтернативный путь активации комплемента (рис. 26.2-4) начинается с ковалентного связывания активной фракции С3b – которая всегда присутствует в сыворотке крови в результате постоянно протекающего здесь спонтанного расщепления фракции С3 – с поверхностными молекулами не всех, но некоторых микроорганизмов.
Рис. 26.2-4. Схема альтернативного пути активации комплемента
1. Дальнейшие события развиваются следующим образом.
а. С3bсвязывает фактор В (который структурно и функционально гомологичен фактору С2), образуя комплекс С3bВ.
б. В связанном с С3b виде фактор В выступает в качестве сусбтрата для фактора D (сыво-
роточной сериновой протеазы), которая расщепляет его с образованием активного комплекса С3bВb. Этот комплекс обладает ферментативной активностью, структурно и функционально гомологичен С3-конвертазе классического пути (С4bС2b) и называется С3-

МДФд. Занятие № 10 |
- 18 - |
конвертазой альтернативного пути.
в. Сама по себе С3-конвертаза альтернативного пути нестабильна. Чтобы альтернативный путь активации комплемента успешно продолжался этот фермент стабилизируется фактором Р (пропердином).
г. То, что происходит дальше, аналогично классическому пути активации комплемента.
1. Нарабатывается много С3b и образуется комплекс С3bВbС3b, являющийся С5конвертазой.
2. Активация С5 дает начало образованию мембранатакующего комплекса (см. разделы
26.2.А.2.и – 26.2.А.2.н).
2.Основное функциональное отличие альтернативного пути активации комплемента, по сравнению с классическим, заключается в быстроте ответа на патоген: так как не требуется время
для накопления специфических антител и образования иммунных комплексов.
Г. Важно понимать, что и классический и альтернативный пути активации комплемента действуют параллельно, еще и амплифицируя (т.е. усиливая) друг друга. Другими словами комплемент активируется не «или по классическому или по альтернативному», а «и по классическому и по альтернативному» путям активации. Это, еще и с добавлением лектинового пути активации, – единый процесс (см. рис. 26.2-5), разные составляющие которого могут просто проявляться в разной степени.
26.3. Анафилотоксины Активные фракции комплемента С3а и С5а называются анафилотоксинами, так как участвуют,
помимо прочего, в аллергической реакции, называемой анафилаксия (см. ниже). Наиболее сильным анафилотоксином является С5а.
А. Анафилотоксиныдействуют на разные клетки и ткани макроорганизма.
1.Действие их на тучные клетки вызывает дегрануляцию последних.
2.Анафилотоксины действуют также на гладкие мышцы, вызывая их сокращение.
3.Действуют они и на стенку сосуда: вызывают активацию эндотелия и повышение его проницаемости, что создает условия для экстравазации из сосудистого русла жидкости и клеток
крови в ходе развития воспалительной реакции.
Б. Корме того, анафилотоксины являются иммуномодуляторами, т.е. они выступают в роли регуляторов иммунного ответа.
1.С3а выступает в роли иммуносупрессора (т.е. подавляет иммунный ответ).
2.С5а является иммуностимулятором (т.е. усиливает иммунный ответ).
26.2-4. Общая схема активации комплемента

МДФд. Занятие № 10 |
- 19 - |
26.2-5. Схема, иллюстрирующая взаимосвязь путей активации комплемента
26.4. Рецепторы для компонентов комплемента Фракции комплемента могут воздействовать на клетки макроорганизма лишь в том случае, если на последних существуют соответствующие рецепторы.
А. Фагоциты имеют рецептор для С3b. Этот рецептор обуславливает большую активности фагоцитов по отношению к опсонизированным микробами (а именно, к тем из них, на поверхности которых наличествует фракции С3b).
Б. Эритроциты обладают специфическими рецепторами для фракций С3b и С4b. Этими рецепторами эритроциты связывают соответствующие фракции комплемента в составе циркулирующих иммунных комплексов (ЦИК) и транспортируют эти комплексы к макрофагам селезенки и печени, которые, их уничтожают, осуществляя тем самым клиренс (т.е. очищение) крови от ЦИК.
В. На тучных клетках локализованы рецепторы к фракции С5а, через которые этот анафилатоксин активирует эти клетки и вызывает их дегрануляцию.
Г. Таким же рецептором обладают макрофаги, благодаря чему фракция С5а активирует и эти клетки.
26.5. Регуляция системы комплемента В норме, в отсутствие во внутренней среде макроорганизма патогена, уровень спонтанной актив-
ности системы комплемента невысок. Каскадный механизм активации комплемента «запускается» активаторами, а регуляция его работы по типу «обратной связи» – ингибиторами, без которых каждый эпизод активации заканчивался бы полным истощением всей системы.
А. Активаторами системы комплемента являются молекулярные комплексы, располагающиеся на поверхности микроорганизма, и запускающие процесс активации комплемента по тому или иному пути. О них уже упоминалось выше (см. раздел 26.2).
1.Активаторами классического пути активации комплемента выступают два комплекса. а. Иммунный комплекс (комплекс антиген-антитело).
б. Комплекс антигена с С-реактивным белком.
2.Активатором лектинового пути активации комплемента выступает комплекс нормального белка сыворотки крови – маннансвязывающеголектина (МСЛ) – с углеводами поверхностных структур микробных клеток (а именно – с остатками маннозы).
3.Активаторами альтернативногопути активации комплемента выступают два комплекса.
а. Комплекс (в результате ковалентного связывания) активной фракции С3b – которая всегда присутствует в сыворотке крови в результате постоянно протекающего здесь спонтан-
ного расщепления фракции С3 – с поверхностными молекулами не всех, но некоторых
микроорганизмов.
б. Агрегированные на поверхности микроба иммуноглобулины классов А и Е.
Б. Ингибиторы системы комплемента локализуются в сыворотке крови или на мембране клеток.
МДФд. Занятие № 10 |
- 20 - |
1.В сыворотке крови локализуются пять белков – ингибиторов системы комплемента. а. С1-ингибитор (С1inh) инактивирует активную фракцию С1qrs (т.е. С1-эстеразу).
б. С4-связывающий протеин (C4BP)делает фактор С4b доступным для деградации фактором I.
в. Фактор Н – делает фактор С3b доступным для деградации фактором I.
г. Фактор I расщепляет С3b (в комплексе с фактором Н) и С4b (в комплексе с С4ВР).
д. Белок S связывается с комплексом С5bС6С7 и предотвращает дальнейшее образование мембранатакующего комплекса.
2.На клетках млекопитающих (и, соответственно человека) локализуются три белка – ингибитора системы комплемента.
а. DAF (decay-acceleratingfactor = фактор, ускоряющий распад) инактивирует С4bС2b (т.к. вместо С2 связывается с С4b).
б. МСР (мембранный кофакторпротеолиза) делает фактор С3b доступным для деградации фактором I.
в. Протектин (обозначаемый также как молекула CD59) инактивирует белки мембранатакующего комплекса (препятствует С-опосредованному лизису собственных клеток)
26.6. Функции системы комплемента Система комплемента играет очень важную роль в защите макроорганизма от патогенов.
А. Система комплемента участвует в инактивации микроорганизмов, в т.ч. опосредует действие на микробы антител.
Б. Активные фракции системы комплемента активируют фагоцитоз.
В. Активные фракции системы комплемента принимают участие в формировании воспалитель-
ной реакции.
26.7. Определение активности системы комплемента Для определения активности комплемента в современных иммунологических лабораториях ис-
пользуют реакцию гемолиза и иммуноферментный анализ (ИФА), пришедший на смену реакции радиальной иммунодиффузии по Манчини.
А. Реакция гемолиза используется для определения титра комплемента и для измерения общей активности системы комплемента.
1.Титр комплемента определяется как максимальное разведение сыворотки крови, вызывающее лизис эритроцитов барана, нагруженных антиэритроцитарными антителами (так назы-
ваемой гемсистемы).
2.Под общей активностью системы комплемента понимают количество комплемента, обеспечивающее лизис 50% эритроцитов гемсистемы (обозначается как СН50).
Б. Иммуноферментный анализ используется для определения концентрации в сыворотке крови отдельных компонентов системы комплемента (C1q, C1s, C2, C3, C4, C5, C6, C7, C8, C9, пропердина, фактора В, С1-ингибитора). Раньше концентрацию наиболее важных в функциональном отношении фракций системы комплемента (чаще – С3 и С4) определяли с помощью реакции иммунодиффузии по Манчини, но в современных лабораториях, оснащенных ИФАанализаторами, с этой целью используют иммуноферментный анализ, значительно расширивший возможности оценки функционального состояния у пациента его системы комплемента.
27. ФАГОЦИТОЗ
27.1. Общее понятие Под фагоцитозом понимают внутриклеточную цитотоксичность (внутриклеточный киллинг) мик-
роорганизмов и биодеградацию других частиц диаметром более 0,1 мкм. Осуществляют фагоцитоз главным образом нейтрофилы и макрофаги/моноциты, хотя фагоцитирующей способностью обладают и другие клетки.
27.2. Стадии фагоцитоза Выделяют четыре стадии фагоцитоза: хемотаксис, адгезия, эндоцитоз и биодеградация. В русскоя-
зычной передаче эти стадии можно описать как «четыре п»: приближение, прилипание, поглощение и переваривание.
