
Стирол C8H8 (фенилэтилен, винилбензол, этиленбензол) — бесцветная жидкость со специфическим запахом. Практически нерастворима в воде, хорошо растворима в органических растворителях, хороший растворитель полимеров.
Получение
Большую часть стирола (около 85 %) в промышленности получают дегидрированием этилбензола при температуре 600—650°С, атмосферном давлении и разбавлении перегретым водяным паром в 3 — 10 раз. Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия.
Другой промышленный способ, которым получают оставшиеся 15 %, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола. Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздухом.
Разрабатываются альтернативные способы получения стирола. Каталитическая циклодимеризация бутадиена в винилциклогексен, с его последующим дегидрированием. Окислительное сочетание толуола с образованием стильбена; метатезис стильбена с этиленом приводит к стиролу. Взаимодействием толуола с метанолом также может быть получен стирол. Кроме того, активно разрабатывались способы выделения стирола из жидких продуктов пиролиза. На сегодняшний день, ни один из этих процессов не является экономически выгодным и в промышленном масштабе не реализован.
Свойства
Стирол легко окисляется, присоединяет галогены, полимеризуется (образуя твердую стекловидную массу — полистирол) и сополимеризуется с различными мономерами. Полимеризация происходит уже при комнатной температуре (иногда со взрывом), поэтому при хранении стирол стабилизируют антиоксидантами (например, третбутилпирокатехином, гидрохиноном). Галогенирование, например, в реакции с бромом, в отличие от анилина идёт не по бензольному кольцу, а по виниловой группе, образуя 1,2 дибромэтилфенил.
Применение
Стирол применяют почти исключительно для производства полимеров. Многочисленные виды полимеров на основе стирола включают полистирол, модифицированные стиролом полиэфиры, пластики АБС (акрилонитрил-бутадиен-стирол) и САН (стирол-акрилонитрил). Также стирол входит в состав напалма.
Пропиле́н(пропен) СН2=СН-СН3—непредельный (ненасыщенный)углеводородряда этилена, горючий газ. Наркотик с наркотическим действием более сильным, чем уэтилена. Класс опасности - четвертый.[1].
|
|
Физические свойства
Пропилен представляет собой газообразное вещество с низкой температурой кипения tкип= -47,7 °C и температурой плавления tпл= −187,6 °C, оптическая плотность d204=0,5193.
Химические свойства
Обладает значительной реакционной способностью. Его химические свойства определяются двойной углерод-углеродной связью. p-связь, как наименее прочная и более доступная, при действии реагента разрывается, а освободившиеся валентности углеродных атомов затрачиваются на присоединение атомов, из которых состоит молекула реагента. Все реакции присоединения протекают по двойной связи и состоят в расщеплении π-связи алкена и образовании на месте разрыва двух новых σ-связей.
Чаще реакции присоединения идут по гетеролитическому типу, являясь реакциями электрофильного присоединения.
Присоединение галогенов (галогенирование)
Реакцию галогенирования обычно проводят в растворителе при обычной температуре. Галогены легко присоединяются по месту разрыва двойной связи с образованием дигалогенопроизводных. Легче идет присоединение хлора и брома, труднее — йода. Фтор взаимодействует со взрывом.
Присоединение водорода (реакция гидрирования)

Присоединяя водород в присутствии катализаторов (Pt, Pd, Ni), пропен переходит в предельный углеводород — пропан.
Присоединение воды (реакция гидратации)

Пропилен реагирует с водой с образованием одноатомного спирта изопропанола, при этом двойная связь раскрывается.
Присоединение галогеноводородов (HHal)
Происходит по правилу Марковникова. Водород кислоты HHal присоединяется к наиболее гидрированному атому углерода при двойной связи. Соответственно остаток Hal связывается с атомом углерода, при котором находится меньшее число атомов водорода.


Пример гидрогалогенирования — получение бромпроизводного пропана при реакции бромоводородаи пропилена.
] Горение на воздухе
При поджигании горит на воздухе: 2СН2=СНСН3+ 9О2→ 6СО2+ 6Н2О.
С кислородом воздуха газообразный пропилен образует взрывчатые смеси.
В слабощелочной или нейтральной водной среде пропилен окисляется перманганатом калия, что сопровождается обесцвечиванием раствора KMnO4и образованием гликолей (соединений с двумя гидроксильными группами при соседних атомах углерода). Эта реакция получила название реакции Вагнера.
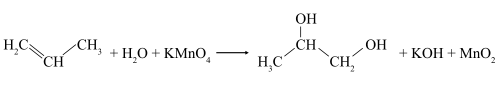
Полимеризация
Условия реакции: нагревание, присутствие катализаторов. Соединение молекул происходит путем расщепления внутримолекулярных π-cвязей и образования новых межмолекулярных σ-cвязей.

Окисление кислородом воздуха в пропиленоксид
При нагревании в присутствии серебряных катализаторов:

Получение
В лаборатории
1. Отщепление галогеноводорода от галогеналкилов при действии на них спиртового раствора щелочи:
H2C—CH – CH3 → H2C=CH–CH3 + KCl + H2O
| | Cl H K — ОH
2. Гидрирование пропина в присутствии катализатора (Pd):
H—C≡C—CH3 + H2 → H2C=CH—CH3
3. Дегидратация изопропилового спирта (отщепление воды). В качестве катализатора используют кислоты (серную или фосфорную) или Аl2O3:
Н2С—СН2 — CH3 → Н2С=СН — CH3 + Н2О
| |
H -OH
4. Отщепление двух атомов галогена от дигалогеноалканов, содержащих галогены при соседних атомах С. Реакция протекает под действием металлов (Zn и др.):
H2C-CH-CH3+Zn → H2C=CH-CH3+ZnBr2 | | Br Br
