
21
Биохимический механизм эффекта Пастера заключается в конкуренции между
пируватдегидрогеназой, превращающей пируват в ацетил-S-КоА, и лактатдегид-
рогеназой, превращающей пируват в лактат. При отсутствии кислорода внутримитохондриальные процессы дыхания не идут, цикл трикарбоновых кислот тормозится
и накапливающийся ацетил-S-КоА ингибирует ПВК-дегидрогеназу. В этой ситуации
пировиноградной кислоте не остается ничего иного как превращаться в молочную. При наличии кислорода ингибирование ПВК-дегидрогеназы прекращается и она, об-
ладая большим сродством к пирувату, выигрывает конкуренцию.
Важно то, что пировиноградная кислота является для клетки токсичным
веществом, и клетке необходимо избавиться от нее каким угодно образом. Так как через мембраны она не проходит, то обезвреживание достигается
превращением пирувата 1) в лактат; 2) в ацетил-S-КоА; 3) в аланин (см "Аланинаминотрансфераза"), 4) в оксалоацетат.
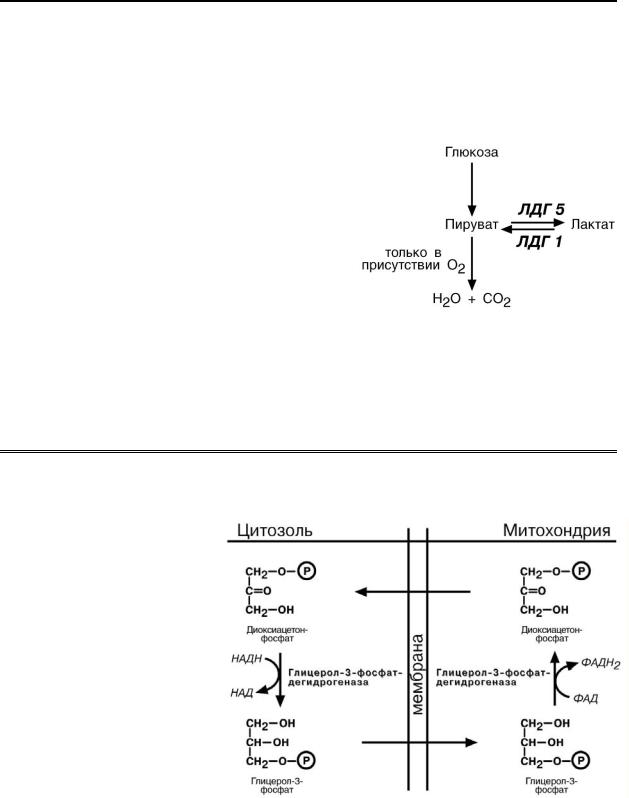
Иллюстрацией к сказанному служит отличие изоферментов лактатдегидрогеназ (ЛДГ) друг от друга. Сердечный
изофермент ЛДГ-1 обладает высоким сродством к молочной кислоте и "стре-
мится" поднять концентрацию пирувата с целью его включения в ЦТК и получения энергии для деятельности мио-
карда. Большое количество митохонд-
рий и поступление сюда лактата из других органов обеспечивает работу сердца при аэробных условиях. При нехватке кислорода свойства ЛДГ-1 не из-
менятся, он по-прежнему будет сдвигать реакцию в сторону продукции пиро-
виноградной кислоты. Изофермент скелетной мышцы ЛДГ-5 обладает высоким сродством к пирувату, при отсутствии кислорода в клетке быстро и эффективно превращает его в лактат, легко проникающий сквозь мембраны. Таким образом, в анаэробных условиях сильнее будет страдать сердечная мышца, что, собственно говоря, и наблюдается в медицинской практике.
ЧЕЛНОЧНЫЕ СИСТЕМЫ
Челночные системы –
механизм доставки обра-
зованных в гликолизе ио-
нов Н+ (в составе НАДН)
из цитозоля в митохондрию.
Так как сама молекула
НАДН через мембрану не проходит, природа поза-
ботилась о том, чтобы
создать системы, прини-
мающие этот водород в цитоплазме и отдающие его в матриксе митохондрий.
22
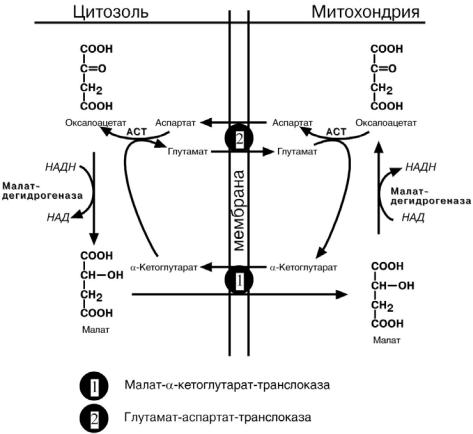
Определены две основные челночные системы – глицеролфосфатная и малат-
аспартатная.
Глицеролфосфатный челнок активен в печени и в быстрых мышечных волокнах. Его ключевыми ферментами являются изоферменты глицерол-3-фосфат-
дегидрогеназы, цитоплазматический и митохондриальный. Они отличаются своими
коферментами: у цитоплазматической формы – НАД, у митохондриальной – ФАД. Метаболиты гликолиза – диоксиацетонфосфат и НАДН образуют глицерол-3-
фосфат, поступающий в матрикс митохондрий, где он окисляется с образованием
ФАДН2. Далее ФАДН2 направляется в дыхательную цепь и используется для получения энергии.
Малат-аспартатный челнок более сложен: постоянно идущие в цитоплазме ре-
акции трансаминирования аспартата поставляют оксалоацетат, который под действием цитозольного пула малатдегидрогеназы восстанавливается до яблочной ки-
слоты. Последняя антипортом с α-кетоглутаратом проникает в митохондрии и, явля-
ясь метаболитом ЦТК, окисляется в оксалоацетат с образованием НАДН. Так как
мембрана митохондрий непроницаема для оксалоацетата, то он аминируется до ас-
парагиновой кислоты, которая в обмен на глутамат выходит в цитозоль.
ГЛЮКОНЕОГЕНЕЗ
Глюконеогенез – это синтез глюкозы из неуглеводных компонентов: лактата, пирувата. глицерола, метаболитов цикла Кребса, аминокислот. Все аминокислоты,
кроме кетогенных лейцина и лизина, способны участвовать в синтезе глюкозы. Неко-
торые из них – глюкогенные – полностью включаются в молекулу глюкозы, некоторые – смешанные – частично.

23
Ворганизме всегда существует потребность в глюкозе:
•для эритроцитов глюкоза является единственным источником энергии,
•нервная ткань потребляет 120 г глюкозы в сутки, притом эта величина не зависит от интенсивности ее работы. Только в экстремальных ситуациях (дли-
тельное голодание) она способна получать энергию из неуглеводных источ-
ников,
•глюкоза играет весомую роль для поддержания необходимых концентраций
метаболитов цикла трикарбоновых кислот (в первую очередь оксалоацета-
та).
Таким образом, при определенных ситуациях – при низком содержании углево-
дов в пище, голодании, длительной физической работе – организм должен иметь
возможность получить глюкозу. Это достигается процессом глюконеогенеза. Кроме получения глюкозы, глюконеогенез обеспечивает и уборку "шлаков" – лак-
тата, образованного при мышечной работе и в эритроцитах, и глицерола, являюще-
гося продуктом липолиза в жировой ткани.
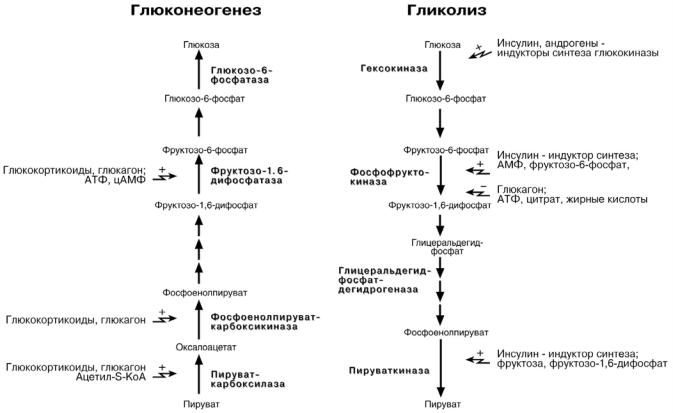
Глюконеогенез лишь отчасти повторяет реакции окисления глюкозы. Как указы-
валось ранее, в гликолизе существуют три необратимые стадии: пируваткиназная
(десятая), фосфофруктокиназная (третья) и гексокиназная (первая). На этих стадиях существуют энергетические барьеры, которые обходятся с помощью специальных реакций.
Обход десятой реакции гликолиза
На этом этапе глюконеогенеза работают два основных фермента – в митохонд-
риях пируваткарбоксилаза и в цитозоле фосфоенолпируват-карбоксикиназа.
Пируваткарбоксилаза превращает пировиноградную кислоту в оксалоацетат. Необ-
ходимо отметить, что эта реакция идет в клетке постоянно, являясь анаплеротиче-
ской (пополняюшей) реакцией ЦТК. Далее оксалоацетат должен попасть в цитозоль
и превратиться в фосфоенолпируват. Однако дело осложняется непроницаемостью мембраны для оксалоацетата. Зато через мембрану может пройти малат, предшественник оксалоацетата по ЦТК. Так как в условиях недостаточности глюкозы в клетке активируется липолиз и окисление жирных кислот, то повышается количество НАДН в митохондриях. Этот избыток позволяет повернуть малатдегидрогеназную реакцию ЦТК вспять. Малат накапливается, выходит в цитозоль и здесь превращается в оксалоацетат.

24
В цитоплазме фосфоенолпируват-карбоксикиназа
осуществляет превращение оксалоацетата в фосфоенол-
пируват, для реакции требуется энергия ГТФ. От молекулы отщепляется тот же углерод, что и присоединяется.
Обход третьей реакции гликолиза
Второе препятствие на пути синтеза глюкозы – фос-
фофруктокиназная реакция – преодолевается с помощью
фермента фруктозо-1,6-дифосфатазы. Этот фермент есть в почках, печени, поперечно-полосатых мышцах. Таким
образом, эти ткани способны синтезировать фруктозо-6-
фосфат и глюкозо-6-фосфат.
Обход первой реакции гликолиза
Последняя реакция катализируется глюкозо-6-
фосфатазой. Она имеется только в печени и почках, следовательно, только эти ткани могут продуцировать сво-
бодную глюкозу.
ГЛЮКОЗО- ЛАКТАТНЫЙ И ГЛЮКОЗО- АЛАНИНОВЫЙ ЦИКЛЫ
Глюкозо-лактатный цикл (цикл Кори) – это связь глюконеогенеза в печени и об-
разования лактата эритроцитах или мышцах из глюкозы. В эритроцитах молочная
кислота образуется
непрерывно, так как для них анаэробный
гликолиз является
единственным способом образования энер-
гии. В скелетных мышцах накопление лактата является следствием гликолиза при очень интенсивной, максимальной мощно-

25
сти, работе, и чем более такая работа интенсивна, тем менее продолжительна По-
сле нагрузки (во время восстановления) лактат удаляется из мышцы довольно бы-
стро – всего за 0,5-1,5 часа.
Дополнение
Следует отметить, что если продолжи-
тельность нагрузки мала (до 10 секунд),
то количество АТФ пополняется преимущественно в
креатинфосфокиназной реакции. В
таком режиме к примеру работают мышцы у ттанги-
стов, прыгунов как в длину, так и в высо-
ту, метателей молота, копья и т.п..
Если нагрузка не более 90 секунд – АТФ синтезируется в основном в реакциях анаэробного глико-
лиза. В спорте это бегуны-спринтеры на 100-500 м, спортсмены силовых видов (борцы, тяжелоатлеты, бодибилдеры). Если напряжение мышцы длится
более двух минут – развивается аэробное окисление глюкозы в реакциях ЦТК
и дыхательной цепи.
Но, хотя мы и говорим об аэробном окислении глюкозы, необходимо знать и помнить, что лактат образуется в мышце всегда: и при анаэробной, и при аэробной работе, однако в разных количествах.
Образовавшийся лактат может утилизоваться только одним способом – превра-
титься в пировиноградную кислоту. Но, как уже указывалось, пируват токсичен для
клеток и должен быть как можно быстрее утилизован. Сама мышца ни при работе, ни во время отдыха не занимается превращением лактата в пируват из-за наличия
специфического изофермента ЛДГ-5.
Если молочная кислота поступила в миокардиоциты, она быстро превращается в пируват, далее в ацетил-S-КоА и вовлекается в полное окисление до
СОB2B и НB2BО.
Большая часть лактата захватывается гепатоцитами, окисляется в пировино-
градную кислоту и вступает на путь глюконеогенеза.
Целью глюкозо-аланинового цикла также является уборка пирувата, но, кроме
этого решается еще одна немаловажная задача – уборка лишнего азота из мышцы.
При мышечной работе и в покое в миоците распадаются белки и образуемые аминокислоты рансаминируются с α-кетоглутаратом. Полученный глутамат взаимодейст-
вует с пируватом. Образующийся аланин является транспортной формой и пирувата
и азота из мышцы в печень. В гепатоците идет обратная реакция трансаминирования, аминогруппа передается на синтез мочевины, пируват используется для синтеза глюкозы
Глюкоза, образованная в печени из лактата или аланина, возвращается обратно в мышцы, восстанавливая во время отдыха запасы гликогена.
26
Кроме мышечной работы, глюкозо-аланиновый цикл активируется во время го-
лодания, когда мышечные белки распадаются и многие аминокислоты используются
вкачестве источника энергии, а их азот необходимо доставить в печень.
РЕГУЛЯЦИЯ ГЛИКОЛИЗА И ГЛЮКОНЕОГЕНЕЗА
27
МЕТАБОЛИЗМ ЭТАНОЛА
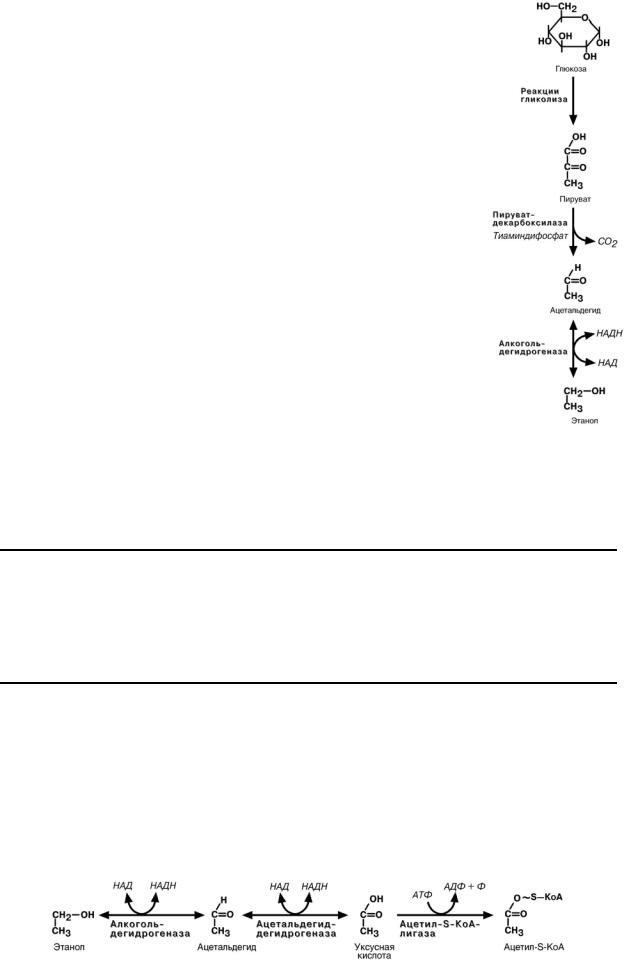
СПИРТОВОЕ БРОЖЕНИЕ
Образование этилового спирта из глюкозы происходит в дрожжах и некоторых видах плесневых грибков. Суммарное
уравнение реакции:
C6H5О10 → 2 CО2 + 2 С2Н5ОН
До стадии образования пирувата реакции спиртового броже-
ния совпадают с реакциями гликолиза, отличия заключаются
только в дальнейшем превращении пировиноградной кислоты. Цель этих превращений – удалить пируват из клетки и окислить
НАДН, который образовался в 6-й реакции.
ОБЕЗВРЕЖИВАНИЕ ЭТАНОЛА
Метаболизм поступающего этанола в организме происходит
в печени двумя путями. Первый путь заключается в окислении
спирта до уксусной кислоты, которая в виде ацетил-S-КоА посту-
пает в ЦТК. Через этот путь проходит от 70% до 90% всего этанола. Оставшаяся часть окисляется в микросомах алкогольоксидазой. При регулярном поступлении этанола доля микросомального окисления возрастает, количество молекул алкогольоксидазы увеличивается.
Так как при обезвреживании этанола образуется большое количество НАДН, в клетках печени активируется реакция превращения пирувата в лактат. Это приводит к гипогликемии, так как пировиноградная кислота является субстратом глюконеогенеза. Свободное проникновение молочной кислоты в кровь обуславливает лакта-
цидемию.
Если запасы гликогена в печени изначально невелики (голодание, недоедание, астеническое телосложение) или израсходованы (после физической работы), то при приеме алкоголя натощак гипогликемия наступает быстрее и может
быть причиной потери сознания. К этому стоит добавить сильный диурети-
ческий эффект этанола, ведущий к быстрому обезвоживанию организма и снижению кровоснабжения головного мозга со всеми вытекающими последствиями.
Этанол является энергетически ценным соединением: при метаболизме 125 г этанола количество образующегося НАДН такое же, как при окислении 500 г глюко-
зы. При полноценном питании и частом потреблении этилового спирта, например, в виде пива, "этанольный" ацетил-S-КоА не столько сгорает в ЦТК, сколько использу-
ется для синтеза холестерина и нейтральных жиров, то есть происходит переход
энергии этанола в запасную форму, что приводит к пивному ожирению и повышает риск атеросклероза.

28
ПЕНТОЗОФОСФАТНЫЙ ШУНТ
Пентозофосфатный путь окисления глюкозы не связан с образованием энергии.
Значение ПФП:
1.Образование НАДФН
•для синтеза жирных кислот,
•холестерина и других стероидов,
•для синтеза глутаминовой кислоты из α-кетоглутаровой кислоты (реак-
ция восстановительного аминирования).
•для систем защиты клетки от свободно-радикального окисления (антиоксидантная защита).

29
2. Образование рибозо-5-фосфата, необходимого для синтеза нуклеиновых ки-
слот.
Наиболее активно реакции ПФП идут в цитозоле клеток печени, жировой ткани, эритроцитах, коре надпочечников, молочной железе при лактации, менее интенсив-
но в скелетных мышцах.
Пентозофосфатный путь включает два этапа – окислительный и неокислительный.
На первом, окислительном, этапе глюкозо-6-фосфат в трех реакциях превра-
щается в рибулозо-5-фосфат, реакции сопровождаются восстановлением двух молекул НАДФ до НАДФН.
Второй этап – этап структурных перестроек, благодаря которым пентозы воз-
вращаются в фонд гексоз. В этих реакциях рибулозо-5-фосфат может изомеризоваться до рибозо-5-фосфата и ксилулозо-5-фосфата. Далее под влиянием фермен-
тов транскетолазы и трансальдолазы происходят структурные перестройки с обра-
зованием иных моносахаридов. При реализации всех реакций второго этапа пентозы превращаются во фруктозо-6-фосфат и глицеральдегидфосфат. Из глицеральдегид-
3-фосфата при необходиости могут образоваться гексозы.
Связь пентозофосфатного пути и гликолиза
Судьба полученных фруктозо-6-фосфата и глицеральдегидфосфата различна
в зависимости от ситуации и потребностей клетки. Поэтому метаболизм глюкозо-6-фосфата может идти по 4 различным механизмам.
Механизм 1. Потребность в НАДФН и рибозо-5-фосфате сбалансирована
(например, при синтезе дезоксирибонуклеотидов). При таких условиях реак-

30
ции идут обычным порядком – образуется две молекулы NADPH и одна моле-
кула рибозо-5-фосфата из одной молекулы глюкозо-6-фосфата по окислительной ветви пентозофосфатного пути.
Механизм 2. Потребность в рибозо-5-фосфате значительно превышает потребность в НАДФН (например, синтез РНК) Большая часть глюкозо-6- фосфата превращается во фруктозо-6-фосфат и глицеральдегид-3-фосфат
по гликолитическому пути. Затем две молекулы фруктозо-6-фосфата и одна молекула глицеральдегид-3-фосфата под действием трансальдолазы и
транскетолазы рекомбинируют в три молекулы рибозо-5-фосфата путем обращения реакции 2 этапа пентозофосфатного пути.
Механизм 3. Потребность в НАДФН значительно превышает потреб-
ность в рибозо-5-фосфате (например, биосинтез холестерола, жирных кислот). В этой ситуации по окислительным реакциям пентозофосфатного
пути образуются НАДФН и рибулозо-5-фосфат. Далее, под действием транскетолазы и трансальдолазы, рибулозо-5-фосфат превращается в пентозо-5- фосфаты, во фруктозо-6-фосфат и глицеральдегид-3-фосфат. В заключение
происходит ресинтез глюкозо-6-фосфата из фруктозо-6-фосфата и глицеральдегидфосфата по пути глюконеогенеза. Подключение новых молекул
глюкозо-6-фосфата позволяет поддерживать стехиометрию процесса.
Механизм 4. Потребность в НАДФН значительно превышает потребность в рибозо-5-фосфате и необходима энергия (например. антиокси-
дантная защита в эритроците). Глюкозо-6-фосфат превращается в рибозо- 5-фосфат и далее во фруктозо-6-фосфат и глицеральдегид-3-фосфат, которые (в отличие от механизма 3) вступают на гликолитический путь обмена, а не подвергаются обратному превращению в глюкозо-6-фосфат. Образованный пируват вступает в ЦТК. В результате происходит одновременное генерирование НАДФН и АТФ.
Недостаточность глюкозо-6-фосфат-дегидрогеназы
Генетическая недостаточность глюкозо-6-фосфат-дегидрогеназы отмечается примерно с частотой 1:60, то есть на Земле имеется около 100 млн человек с этим заболеванием, которое, к счастью, не всегда проявляется. Следствием ферментного дефекта является снижение синтеза НАДФН в клетке. Особенно существенно это влияет на эритроциты, в которых окислительный этап пентозофосфатного цикла является единственным источником НАДФН.
Из разнообразных функций НАДФН для эритроцитов имеет значение одна – уча-
стие в работе антиоксидантной системы, а именно кооперация с глутатион-
пероксидазой, ферментом, восстанавли-
вающим пероксид водорода до воды. Пероксид водорода в клетке образуется из
свободных кислородных радикалов (актив-
ных форм кислорода), последние являются обычным продуктом деятельности ряда
ферментов, например, цитохромоксидазы.
При употреблении некоторых лекарственных препаратов (сульфаниламиды, (стрептоцид, сульфацил-Na), норсульфазол, парацетамол, аспирин, примахин, метиленовый синий, нафталин) в клетках ак-
