
Физиология возбудимых тканей I
.pdf
Лицензия ИД №00597 от 15.12.99 г. Подписано в печать 15.12.01. Усл. печ. л. 2,25.
Формат 60 84 1/16. Печать офсетная. Тираж 350 экз. Заказ № 552/01. 197089, Санкт-Петербург, улица Льва Толстого, 6/8.
Издательство СПбГМУ
Министерство здравоохранения Российской Федерации Санкт-Петербургский государственный медицинский университет имени академика И.П.Павлова
Кафедра нормальной физиологии
А.М.Коробкова, А.Ю.Юров
ФИЗИОЛОГИЯ ВОЗБУДИМЫХ ТКАНЕЙ
Часть I
Пособие для студентов лечебного, стоматологического факультетов
и факультета спортивной медицины
Санкт-Петербург
2001

А в т о р ы : к.б.н. А.М.Коробкова, к.б.н. А.Ю.Юров.
Р е ц е н з е н т ы : проф. Р.В.Бабаханян,
проф. А.К.Косоуров.
Утверждено на заседании ЦМК химико-физиологических дисциплин 01 декабря 2001 г.
В пособии рассматриваются строение и работа ионных мембранных каналов, условия возникновения и поддержания мембранного потенциала покоя, локальные потенциалы и потенциалы действия в возбудимых тканях. Пособие содержит проверенные фундаментальные знания в объеме, соответствующем учебным планам СПбГМУ и медицинскому стандарту USMLE. Предназначено для студентов II курса лечебного, стоматологического факультетов и факультета спортивной медицины.
Издательство СПбГМУ, 2001
МЕМБРАННЫЙ ПОТЕНЦИАЛ
Мембранный потенциал – это разность электрических потенциалов между внутренней и внешней сторонами клеточной мембраны. Для измерения мембранного потенциала используется методика внутриклеточного отведения. Внутрь клетки вводится микроэлектрод, который представляет собой стеклянный капилляр, заполненный электропроводящим раствором
(рис. 1).
Рис.1. Внутриклеточное измерение мембранного потенциала стеклянным микроэлектродом [Vander et al., 1985].
Величина мембранного потенциала задается различиями в плотности электрических зарядов по разные стороны мембраны. Плотность электрического заряда в свою очередь обусловливается концентрацией заряженных частиц, то есть ионов. Поэтому мембранный потенциал определяется различиями в концентрации ионов по разные стороны мембраны.
Известно, что на ион, находящийся в растворе и в электрическом поле, действует сила электрохимического градиента, в которую входят две противоположно направленные составляющие:
механическая, определяемая градиентом концентрации данного иона (сила химического градиента, задаваемая разностью – в нашем случае разницей – концентраций иона по разные стороны мембраны). Эта сила стремится передвинуть ион туда, где его меньше и распределить его равномерно во всем растворе.
-4 -
электрическая, зависящая от собственного заряда иона и градиента внешнего электрического поля. В нашем случае эта сила определяется величиной мембранного потенциала и направлена против механической.
Если эти две силы полностью уравновесят друг друга, то ионы данного типа будут неподвижны. Их поток будет равен нулю. Если одна из компонент перевесит другую, то возникнет ионный ток через мембрану. Значение тока будет определяться, с одной стороны, силой электрохимического градиента, и, с другой, – проницаемостью мембраны для данного типа ионов.
Величина мембранного потенциала, при которой ион будет неподвижен, может быть рассчитана количественно из уравнения Нернста. Данное уравнение выведено из условия равновесия двух сил, действующих на ион
впротивоположном направлении. Как уже говорилось, с одной стороны это сила электростатического поля, взаимодействующая с электрическим зарядом иона, а с другой – механическая сила, обусловленная неравномерностью ионной концентрации. Уравнение Нернста определяет равновесный мембранный потенциал – то значение мембранного потенциала, которое уравновесит силу, стремящуюся переместить ион в область с меньшей концентрацией:
|
|
E |
RT |
ln |
[C]out |
, |
(1) |
|
|
|
|
||||
|
|
|
zF |
[C]in |
|
||
где E |
– |
равновесный электрический потенциал; |
|
||||
R |
– |
универсальная газовая постоянная; |
|
||||
T |
– |
абсолютная температура; |
|
|
|
||
z |
– |
валентность иона; |
|
|
|
||
F |
– |
число Фарадея (константа); |
|
|
|
||
C |
– |
концентрация иона; |
|
|
|
||
out |
– |
вне клетки; |
|
|
|
||
in |
– |
внутри клетки. |
|
|
|
||
Другими словами, равновесный мембранный потенциал соответствует нулевому значению электрохимического градиента для данного иона.
Результирующая сила, проталкивающая ион через мембрану, будет тем больше, чем значительней разница между равновесным и мембранным потенциалами. Если мембрана проницаема для данного типа ионов, то возникнет ионный ток через мембрану. Его величина будет тем больше, чем сильнее отличаются эти потенциалы.
- 5 -
Концентрации некоторых наиболее важных ионов и соответствующие значения равновесных потенциалов приведены в таблице 1.
|
|
|
Та б ли ц а 1 |
|
|
|
|
Ионы, молекулы |
Равновесный |
Концентрация |
Концентрация |
|
потенциал, мВ |
в клетке, мМ/л |
в среде, мМ/л |
|
|
|
|
К+ |
-90 |
145 |
4-5,5 |
Na+ |
+60 |
10 |
145-150 |
Ca++ |
+130 |
0,001 |
2,4 |
Cl- |
-80 |
4-10 |
100-120 |
Фосфаты |
|
75 |
4 |
Аминокислоты |
|
200 мг/дцл |
30 мг/дцл |
Фосфолипиды |
|
2-95 |
0,5 |
Белки |
|
16-40 |
2-5 |
Мембранный потенциал покоя (МПП) – значение мембранного потенциала клетки, находящейся в покое. Прямые измерения показывают, что эта величина лежит в пределах от –10 до –90 мВ.
Из таблицы видно, что значения равновесного потенциала конкретных ионов могут значительно отличаться от МПП. Следовательно, в покоящейся клетке на эти ионы будет действовать сила, стремящаяся протолкнуть их сквозь мембрану. Если мембрана проницаема для данного иона, то в покоящейся клетке постоянно будет существовать поток ионов данного типа. Величина тока будет тем выше, чем больше разница между равновесным потенциалом иона и МПП и чем выше проницаемость мембраны для иона.
В клетке, находящейся в состоянии покоя, суммарный заряд не меняется. Следовательно, несмотря на то, что ионы в состоянии покоя постоянно проталкиваются через мембрану, суммарный мембранный ионный ток в условиях покоя должен быть равен нулю. Это возможно благодаря постоянной работе многочисленных ионных насосов, активно – с затратой энергии – перемещающих ионы через мембрану в обратном направлении, противоположном силе электрохимического градиента.
- 6 -
ОСОБЕННОСТИ ТРАНСПОРТА ИОНОВ ЧЕРЕЗ КЛЕТОЧНУЮ МЕМБРАНУ
Билипидный слой мембраны не является проницаемым ни для ионов, ни для крупных органических молекул (белки, аминокислоты, фосфолипиды, фосфаты), имеющих обычно отрицательный заряд. Эти вещества, однако, способны проходить в клетку и из нее благодаря специальным белковым структурам, встроенным в мембрану.
Ионы постоянно движутся через мембрану в двух противоположных направлениях: под действием суммарной силы, задаваемой направлением электрохимического градиента (внешней силы), и в обратом – противоположном действию внешней силы.
Движение ионов против направления действия внешней силы требует дополнительных затрат энергии и осуществляется при помощи транспортеров.
Транспортеры – белки, которые соединившись с веществом, находящимся по одну строну мембраны, меняют свою третичную и четвертичную структуру (конформацию) и за счет этого процесса активно, с затратой энергии, перемещают вещество сквозь мембрану. Пройдя через мембрану вещество отсоединяется от переносчика. Обычно на перенос затрачивается энергия распада АТФ. Таким образом транспортер способен перемещать вещество в направлении, противоположном действию суммарной внешней силы, с затратой энергии. Более подробно работа одного из важнейших транспортеров – К+/Na+-АТФазы – будет рассмотрена ниже.
Движение ионов в направлении действия внешней силы происходит в основном по механизму облегченной диффузии, т.е. пассивно. В этой связи выделяют специальные структуры – каналы.
Каналы – белковые мембранные комплексы, иногда с водным слоем внутри. Движение частиц через мембрану по каналу происходит под действием внешней силы без дополнительных затрат энергии.
Специально выделяют ионоселективные каналы, избирательно проницаемые только для ионов какого-либо конкретного вещества.
Свойства ионоселективные каналов
1. Избирательность (ионная селективность) канала. Не все ионы способны проходить через один и тот же канал. Свойства канала должны соответствовать размерам, электрическому заряду, параметрам гидратной оболочки и другим специфическим свойствам иона. Например, исключительно важны Na+ каналы, избирательно проницаемые только для ионов
- 7 -
Na+, но непроницаемые, скажем, для ионов К+. Аналогично большое значение имеют К+ каналы, проницаемые лишь для К+, не пропускающие Na+.
2. Способность канала к изменению своей проницаемости. Про-
ницаемость канала может различаться в зависимости от изменений конформации канального белка.
Принято рассматривать следующие состояния канала:
инактивированное (канал не способен к открытию);
активированное (канал способен к открытию):
–открытое;
–закрытое.
Состояние канала зависит от внешней среды. Наиболее часто рассматривают два типа зависимости проницаемости канала: от величины мембранного потенциала (потенциалзависимые каналы) и от химического воздействия (хемозависимые каналы).
Потенциалзависимый канал в зависимости от значения разности потенциалов вне и внутри клетки (величины электрической поляризации клеточной мембраны) может принимать открытое либо закрытое состояние.
Принято считать, что потенциалзависимые каналы не имеют промежуточных состояний, а переход между их устойчивыми конформациями осуществляется скачком. При этом переключение между открытым и закрытым состояниями может происходить со скоростью до 300 раз в секунду. Вероятность и частота перехода канала из открытого в закрытое состояние и наоборот зависят от степени поляризации мембраны. Чем менее поляризована мембрана, тем менее изменена конформация белка-канала внешним полем и тем больше вероятность его перехода в открытое состояние.
Большое значение имеют Na+- и K+-потенциалзависимые каналы (рис.2). Механизм действия этих каналов объясняют с помощью модели так называемых "ворот".
Полагают, что Na+-каналы имеют активационные ворота с внешней стороны клеточной мембраны и инактивационные ворота с внутренней. Если инактивационные ворота закрыты, то канал вообще теряет способность переходить в открытое состояние. Открытие инактивационных ворот делает возможной работу активационных ворот и позволяет им открывать либо закрывать канал в зависимости от значения мембранного потенциала. При напряжении поляризации -90 мВ Na+ каналы закрыты, но активированы (способны к открытию). В пределах между -70 и -50 мВ каналы на-

- 8 -
чинают скачкообразно открываться. Чем меньше разность потенциалов внутри и снаружи клетки, тем больше вероятность перехода канала в открытое состояние и тем большее число каналов открыто. Открытие большинства Na+-каналов увеличивает проницаемость для Na+ в 500-5000 раз. Na+ по градиенту электрохимического потенциала лавинообразно устремляется в клетку через открытые каналы. Мембранный потенциал внутри клетки меняет знак и из отрицательного превращается в положительный (явление "overshoot"). Изменение потенциала до положительных величин приводит к закрытию инактивационных ворот, "выключению" каналов и прекращению дальнейшего перемещения Na+ внутрь клетки. Это происходит примерно через 1/10000 с после открытия активационных ворот. Следовательно, Na+-каналы остаются открытыми не более 1/10000 с, а затем инактивируются (переходят в состояние, в котором они вообще не способны открыться). Для того, чтобы вновь привести эти каналы в активированное состояние (вернуть им способность открываться), требуется возвращение потенциала внутри клетки к отрицательным величинам порядка -70 мВ.
Рис.2. Схематическое изображение потенциалзависимых каналов для Na+ и К+. При негативном потенциале покоя m- и n-ворота закрыты, h-ворота открыты
[Bullock et al., 1995].
- 9 -
Поведение К+-каналов удовлетворительно объясняет более простая модель с одними воротами, всегда находящимися в активированном состоянии. Чем более отрицателен потенциал внутри клетки, определяющий степень поляризации клеточной мембраны, тем больше вероятность нахождения К+-канала в закрытом состоянии. Считается, что ворота полностью закрыты при мембранном потенциале -90 мВ. Они открываются при уменьшении мембранного потенциала до 0 мВ и дальнейшей перезарядке мембраны примерно до +35 мВ.
Хемозависимый канал способен изменять свою проницаемость при взаимодействии с биологически активными химическими веществами (медиаторами, гормонами и др.), взаимодействующими со специфическими рецепторами канала. Специально выделяют чувствительность каналов к специфическим токсинам. Токсин способен связаться с каналом и перевести его в определенное устойчивое состояние – открытое или закрытое. Далее нормальная работа канала становится невозможной. Если токсин закрывает канал, его называют блокатором, если открывает – ионофором. Связывание токсина с каналом может быть обратимым и необратимым. Необратимое связывание может привести к гибели организма (например, токсическое действие ядов некоторых змей). Обратимое связывание может разрушиться при определенных условиях, либо со временем. Например, для имеющего важное значение потенциалзависимого Na+-ка- нала необратимым блокатором является природный яд рыбы Tetronodon – тетродотоксин, обратимым – новокаин. Блокаторы и ионофоры позволяют выявить наличие или отсутствие определенного канала в мембране, установить его биохимические свойства. Они нашли чрезвычайно широкое применение как в научных исследованиях, так и в практической фармакологии.
УСЛОВИЯ, ОПРЕДЕЛЯЮЩИЕ ВЕЛИЧИНУ МЕМБРАННОГО ПОТЕНЦИАЛА ПОКОЯ
Важнейшими условиями, определяющими величину потенциала покоя, являются:
–различия в проницаемости мембраны для разных ионов;
–градиенты концентраций ионов по разные стороны мембраны;
–поддержание ионных градиентов работой К+/Na+-АТФазы, совершающей активный перенос ионов через мембрану.
- 10 - |
|
- 11 - |
|
Различия в проницаемости мембраны для разных ионов. Гради- |
Мембрана проницаема и для других ионов, например для Cl–, кото- |
||
енты концентраций ионов по разные стороны мембраны. |
|
рый в большом количестве находится по другую сторону мембраны клет- |
|
Мембрана клетки наиболее проницаема для ионов К+. В пределах от |
- |
ки, чем К+, т.е. снаружи. Наиболее проницаема для Cl– мембрана мышеч- |
|
70 до -90 мВ суммарная проницаемость калиевых каналов большинства кле- |
ных клеток, в меньшей степени – мембрана нейронов. |
|
|
ток достаточно велика и превосходит натриевую более, чем в 20 раз. |
В |
Полагают, что перераспределение ионов вследствие изменения состо- |
|
этих условиях К+ способен легко выходить из клетки по градиенту концен- |
яния каналов происходит только в пределах двойного электрического слоя |
||
трации. Крупные отрицательные ионы (органические молекулы, синтезиро- |
в непосредственной близости от мембраны клетки. В целом же в цитоплаз- |
||
ванные в клетке и не способные из-за больших размеров выходить наружу) |
ме как положительные, так и отрицательные ионы остаются свободно рас- |
||
перемещаются к мембране вслед за ионами К+, но остаются в клетке и под- |
пределенными. Поэтому требуется сравнительно небольшое количество |
||
держивают отрицательный заряд на внутренней стороне мембраны. |
|
перемещенных ионов одного знака, чтобы быстро (за 1/10000 с) изменить |
|
Слой анионов вдоль внутренней стороны мембраны удерживает |
заряд мембраны от -90 до +35 мВ: от 0,2 10-7 до 10-9 общего заряда, нахо- |
||
К+ вдоль наружной стороны мембраны, образуя положительно заряжен- |
дящегося внутри клетки. Химический градиент иона при этом практически |
||
ный слой. Возникает двойной электрический слой зарядов вдоль мембра- |
не меняется, так как в изменении мембранного потенциала участвуют от- |
||
ны (рис.3). Удельная электрическая емкость мембраны составляет около |
носительно малые количества ионов. |
|
|
1 мкф/см2. |
|
Поддержание ионных градиентов через мембрану работой |
|
|
|
К+/Na+-АТФазы. По электрохимическому градиенту ионы Na+ движутся в |
|
|
|
клетку, деполяризуют мембрану и вызывают выход ионов K+, равный вхо- |
|
|
|
ду Na+. Следовательно, через какое-то время концентрация ионов K+ и Na+ |
|
|
|
внутри и снаружи клетки сравняются, а МП исчезнет. Стремление в клетку |
|
|
|
Na+ нарушает осмотический баланс, потому что внутри клетки частиц и |
|
|
|
без того намного больше (анионы и K+), чем снаружи. Поддержание гради- |
|
|
|
ентов K+ и Na+ и уменьшение Na+ в клетке для сохранения осмотическо- |
|
|
|
го баланса осуществляется транспортером, который называют K+/Na+- |
|
|
|
АТФаза. Его работа требует затрат энергии, так как он транспортирует |
|
|
|
ионы против градиента их концентрации. K+/Na+-АТФаза непрерывно пе- |
|
|
|
ремещает 2K+ в клетку в обмен на 3Na+, которые она одновременно выво- |
|
|
|
дит из клетки через мембрану. |
|
|
|
К+/Na+-АТФаза представляет собой белковый комплекс из двух субъ- |
|
|
|
единиц с тремя участками связывания Na+ внутри, двумя участками связы- |
|
|
|
вания К+ снаружи и внутриклеточным центром связывания с молекулой |
|
|
|
АТФ. Только при одновременном связывании с ионами натрия, калия |
и |
Рис. 3. Образование двойного электрического слоя на наружной и внутрен- |
АТФ К+/Na+-АТФаза изменяет свою конформацию и переносит ионы, ис- |
||
пользуя энергию расщепленной макроэргической связи в молекуле АТФ. |
|
||
ней сторонах клеточной мембраны [Vander et al., 1985]. |
|
|
|
|
|
Неэквивалентным обменом ионов К+/Na+-АТФаза создает дополни- |
|
Поскольку мембрана клетки наиболее проницаема для ионов К+, ве- |
тельный отрицательный заряд в клетке от 5 до 20 мВ в зависимости от со- |
||
личина мембранного потенциала покоя наиболее близка к равновесному |
противления мембраны. Главнейший вклад этого транспортера в работу |
||
потенциалу именно этого иона. Для ионов Na+ в условиях покоя прони- |
клетки заключается также в поддержании осмотического равновесия: вы- |
||
цаемость в 20-100 раз меньше, чем для К+. |
|
водя Na+, К+/Na+-АТФаза способствует выходу из клетки избыточной воды, |
|
- 12 -
проникающей в нее вслед за Na+ и Cl–. Повышение количества Nа+ в цитоплазме является основным, если не единственным, механизмом активации К+/Na+-АТФазы.
Ослабление работы К+/Na+-АТФазы, например недостаточное образование АТФ в митохондриях нейронов головного мозга при ишемии (недостатке кислорода), приводит к уменьшению ионных градиентов. Na+ перестает активно выводиться из клетки и накапливается в ней, приводя тем самым к гипертоничности внутриклеточной жидкости. Возникающая разность осмотических давлений во внутри- и внеклеточной среде вызывает вход воды в клетку вплоть до ее гибели.
Выводы:
1.К+, Nа+, CL–, а также белковые и фосфатные внутриклеточные анионы являются важнейшими ионами, формирующими величину МПП.
2.Вклад каждого из этих ионов в образование МПП определяется
проницаемостью мембраны для иона. Наиболее проницаема мембрана для К+, поэтому МПП наиболее близок к равновесному потенциалу для К+ (примерно -90 мВ).
3.В результате выхода ионов из клетки на мембране создается двойной электрический слой. Анионы на внутренней стороне мембраны клетки образуют отрицательный потенциал и электростатически удерживают катионы снаружи мембраны.
4.Пассивное движение ионов продолжается до тех пор, пока электростатическая сила, действующая на них, не уравновесит силу химического градиента. Величина равновесного потенциала, который предотвращает дальнейшую диффузию, может быть оценена из уравнения Нернста
(1)и определяется различием концентраций ионов по разные стороны мембраны: чем больше разнятся концентрации, тем больше величина потенциала.
5.Пассивные токи утечки К+ и Nа+ через мембрану, когда Na+ входит в клетку, а К+ выходит из клетки по электрохимическому градиенту, компенсируются работой K+/Na+-АТФазы с затратой энергии АТФ, переносящей эти ионы в обратном направлении.
6.Суммарный ионный ток через мембрану клетки, находящейся в состоянии покоя, равен нулю. Это обусловлено равновесием: а) входящего
тока утечки натрия; б) выходящего тока утечки калия; в) компенсирующих токов натрия и калия, создаваемых K+/Na+-АТФазой. Токи утечки для каждого типа ионов осуществляются по собственным ионоселективным каналам.
- 13 -
ИЗМЕНЕНИЕ ВЕЛИЧИНЫ МЕМБРАННОГО ПОТЕНЦИАЛА
Если мембранный потенциал отличен от нуля, то говорят, что мембрана поляризована. Состояние, при котором разность потенциалов по разные стороны мембраны увеличивается, называют гиперполяризацией. Уменьшение разности потенциалов соответственно называют деполяризацией.
Любые воздействия, которые влияют на поток ионов через мембрану, изменяют отрицательный заряд внутри клетки и, следовательно, ее мембранный потенциал.
Рассмотрим некоторые практически важные случаи изменения величины мембранного потенциала.
Увеличение внеклеточной концентрации ионов К+ приводит к снижению концентрационного градиента этого иона. Выходящий ток К+ при этом уменьшается и возникает деполяризация.
Необходимо отметить, что значительное увеличение внеклеточной концентрации К+ приводит к обратному эффекту – падению возбудимости. Так двукратное увеличение количества К+ (например при внутривенном введении больших доз КСl) приводит к незначительной деполяризации и
повышению возбудимости клеток сердца. Четырехкратное превышение количества К+ уменьшает возбудимость до полной остановки сердца в фазе расслабления. Этот эффект находит клиническое применение при создании кардиоплегических растворов, используемых для временной остановки сердца при хирургическом вмешательстве.
Уменьшение внеклеточной концентрации К+ приводит к гиперполяризации и снижению возбудимости. Однако активность клеток-водите-
лей ритма сердца повышается. Действие мочегонных препаратов, вызывающих избыточную потерю К+, может привести к аритмиям сердца.
Снижение проницаемости мембраны для ионов К+ (например, при блокаде К+-каналов тетраэтиламмонием или при снижении рН крови) уменьшает К+-ток и приводит к деполяризации. Повышение К+-проницае- мости (например, при действии ацетилхолина на пейсмекерные клетки сердца)вызывает гиперполяризацию.
Повышение проницаемости для ионов Na+ приводит к усилению входящего натриевого тока и к деполяризации, снижение вызывает гипер-
поляризацию и приближение величины мембранного потенциала к равновесному потенциалу для К+, так как уменьшается деполяризующий ток утечки натрия.
-14 -
Сl– в большинстве клеток (кроме нервных)свободно перемещается
через мембрану и распределяется в соответствии с величиной мембранного потенциала. Равновесный потенциал для ионов Сl– -80 мВ. При деполяризации мембраны ионы Сl– начинают входить в клетку, при гиперполяризации усиливается выход Сl–. Таким образом, ток ионов Сl– стабилизирует
мембранный потенциал, пытаясь поддержать его близким к своему равновесному -80 мВ, т.е. ионы Сl– вместе с ионами К+ определяют и поддерживают величину мембранного потенциала покоя.
Угнетение активности К+/Na+-АТФазы приводит к деполяризации,
во-первых, за счет снижения концентрационного градиента калия и замедления пассивного выхода этого иона, а во-вторых, вследствие уменьшения активного выведения ионов Na и накопления их в цитоплазме. Торможение работы К+/Na+-АТФазы возникает при действии специфических блокаторов (например, препаратов наперстянки), а также при отравлении ядами, снижающими образование АТФ (например, цианидами, которые угнетают процессы биологического окисления).
ВОЗБУДИМОСТЬ
Все живые клетки обладают раздражимостью – способностью активно отвечать на внешнее воздействие той или иной формой деятельности: изменением метаболизма, роста, ускорением деления, секрецией, движением, сокращением, изменением потенциала и т.д. Раздражимость живых систем отличается от пассивной реактивности неживых тел тем, что:
1)для реакции живые системы используют не энергию внешнего воздействия, а энергию собственных метаболических процессов;
2)затраты собственной энергии для ответа живой системы далеко не всегда пропорциональны силе внешнего воздействия.
Реакция конкретной живой клетки на действие раздражителя обладает специфическими свойствами. Клетки, обладающие свойством генерировать в ответ на раздражение электрический импульс (так называемый нервный импульс, или потенциал действия, см. дальше), называются возбудимыми, а процесс генерации потенциала действия – возбуждением. Ткань, состоящая из возбудимых клеток, также называется возбудимой.
Не следует называть возбуждением любую особо отчетливо выраженную внешнюю деятельность, например, сокращение или движение. В общебиологической литературе, однако, можно встретить такое понятие возбуждения. Выделяют нервную, мышечную и железистую возбудимые ткани.
-15 -
ЛОКАЛЬНЫЙ ОТВЕТ И ЭЛЕКТРОТОН
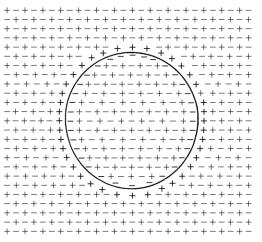
При пропускании через ткань постоянного электрического тока от внешнего источника величина МП будет сдвигаться. В том случае, когда сила тока настолько мала, что не вызывает заметного изменения состояния потенциалзависимых каналов, величина реакции прямо пропорциональна величине стимула (линейная зависимость). Такое изменение МП называют электротоном. Электротон рассматривают исключительно как пассивное явление (проявление пассивной реактивности, которая не отличается по своей природе для случаев живых и неживых систем). При увеличении силы тока ответ клетки начинает возрастать в большей степени, чем сила приложенного стимула (нелинейная зависимость). Увеличение активности клетки объясняется тем, что часть потенциалзависимых Na+-каналов начинает открываться. В этом случае даже незначительные сдвиги силы стимула вызывают гораздо большее изменение амплитуды реакции, чем в случае электротона. Изменение мембранного потенциала, которое еще не вызывает возбуждения, но заметно сдвигает состояние потенциалзависимых каналов, называется локальный ответ (локальный потенциал) (рис.4).
Рис.4. Электротонические потенциалы и локальные ответы. 1, 2, 3, 4, 5 – относительная амплитуда стимула [Шмидт, Тевс, 1985].
- 16 -
Свойства локального ответа и электротона. |
Способность к суммированию. В процессе развития локального |
|
Зависимость от силы приложенного раздражения. Чем больше |
ответа мембрана сохраняет способность реагировать на другие раздражи- |
|
приложенный ток, тем больше деполяризация или гиперполяризация |
тели. При повторном действии раздражителя в условиях последействия |
|
(рис.5). Скорость изменения величины мембранного потенциала неодина- |
предыдущего суммарная амплитуда ответа увеличивается. Этот процесс из- |
|
кова во времени. Наиболее быстрой она является непосредственно в мо- |
вестен под названием временной суммации локальных ответов. Про одно- |
|
мент нанесения раздражения, но затем начинает уменьшаться из-за увели- |
временном действии нескольких раздражителей их локальные ответы так- |
|
чения выхода из клетки ионов К+ через деполяризованную мембрану. В |
же суммируются. Это явление называется пространственной суммацией |
|
итоге деполяризация достигает конечного уровня, при котором ионный |
локальных ответов. В обоих случаях суммации итоговое действие на МП |
|
ток через мембрану полностью уравновешивает внешний ток приложенно- |
оказывается в соответствии со сдвигом суммарного электрического заряда |
|
го электрода. |
ионов (см. рис.5). |
|
|
Распространение по мембране (в том числе и возбудимой) |
с |
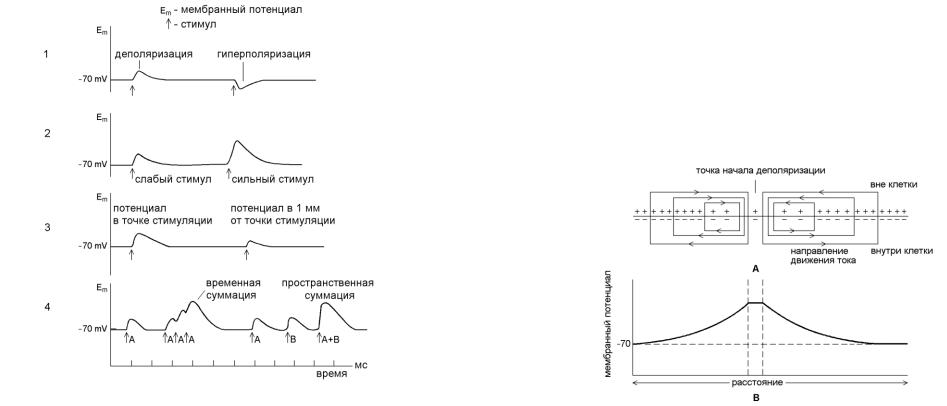
затуханием (уменьшением амплитуды и на незначительное расстояние). Электрический ток, распространяющийся вдоль мембраны, по мере удаления от точки нанесения раздражения уменьшается по величине, так как "расходуется" на преодоление электрических сопротивления и емкости среды. Соответственно сдвиги МП будут уменьшаться по мере удаления от места раздражения. Чем больше сопротивление мембраны, диаметр аксона и чем меньше сопротивление аксоплазмы, тем больше будет расстояние, на которое распространится ток. Значимый локальный ответ как правило распространяется на расстояние не более 2-5 мм (см. рис.5; рис.6).
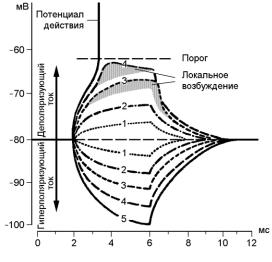
Рис.5. Свойства электротона и локального ответа: 1) деполяризация и гиперполяризация; 2) зависимость от силы стимула; 3) распространение с затуханием; 4) способность к пространственной и временной суммации [Vander et al., 1985].
- 17 -
Рис.6. Деполяризация соседних участков мембраны электротоном, распространяющимся от точки стимуляции и деполяризации [Vander et al., 1985].
- 18 -
Для процесса возбуждения локальный ответ имеет определяющее значение:
–в мембранах рецепторов – окончаниях дендритов чувствительных нейронов – при действии на них раздражителей, изменяющих проницаемость этих мембран к ионам;
–в мембранах синапсов (мест контактов нервной клетки с другими клетками) в момент передачи информации от нейрона к другой клетке;
–в мембранах возбудимых клеток, если сила раздражения недоста-
точно велика, чтобы вызвать характерное только для этих типов клеток изменение МП, которое называется возбуждение или потенциал действия.
ПОТЕНЦИАЛ ДЕЙСТВИЯ
Потенциал действия (ПД) – это быстрое изменение величины МП до положительного значения, а затем возвращение примерно с такой же скоростью до начального отрицательного значения (рис.7). Возбудимые клетки обладают способностью генерировать ПД в ответ на действие раздражителей, деполяризующих мембрану. Необходимыми условиями возможности возникновения ПД являются различие концентраций ионов по разные стороны клеточной мембраны и существование в ней соответствующих потенциалзависимых ионоселективных каналов.
Фазы потенциала действия.
Фаза деполяризации. Деполяризация возбудимой клеточной мембраны начинает развиваться из-за возникновения в ней локального деполяризующего электрического тока, приводящего к изменению МП в положительную сторону. В результате усиливается выходящий из клетки ток утечки К+ (мембранный потенциал в большей степени отличается от равновесного для К+). Однако гораздо в большей степени усиливается и начинает превалировать входящий ток Na+ (все большая часть потенциалзависимых Na-каналов начинает переходить из активированного состояния в открытое и суммарная проводимость Na+ каналов многократно возрастает).
Увеличение входа Na+ дополнительно деполяризует мембрану. Эта деполяризация в свою очередь вызывает дополнительное открытие Na+ каналов и ток утечки Na+ возрастает еще больше. Возникает самоусиливаю-
щийся процесс с положительной обратной связью: деполяризация открыва-
ет Na+-каналы, проницаемость мембраны для Na+ возрастает, Na+ входит в клетку и еще больше увеличивает степень деполяризации, сдвигая МП в положительную сторону. Открываются дополнительные Na+-каналы,
- 19 -
проницаемость для Na+ увеличивается еще больше. Процесс становится лавинообразным. Максимальная скорость деполяризации в ряде случаев достигает 1000 В/с. В результате внутренняя поверхность клетки меняет знак и становится положительной (явление "overshoot"). Максимальное значение положительного потенциала в среднем составляет от +5мВ до
+30 мВ.
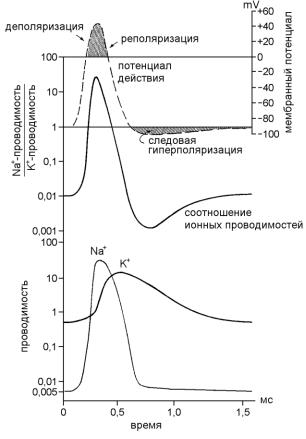
Рис.7. Потенциал действия (верхняя кривая), изменение отношения проводимостей мембраны для Na+ и К+ (средняя кривая), проводимости мембраны для Na+ и К+ (нижняя кривая) во время развития потенциала действия [Guyton, Hall, 1996].
- 20 -
