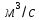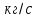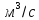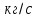Исходные данные
-
Состав обжигового газа после обжига серосодержащего сырья в атмосфере воздуха:
|
Состав |
Объемные % |
|
SO2 |
12,8 |
|
SO3 |
0,07 |
|
Н2О |
5,7 |
|
О2 |
2,6 |
|
N2 |
78,83 |
-
Перед подачей в реактор газ подвергается осушке и очистки от SO3, (объемные %):
Концентрация в объемн. % SO2 10,2
-
Окисление SO2 осуществляется в несколько стадий контактирования в каталитическом реакторе:
Каталитический реактор промежуточными теплообменниками между 5-ю слоями катализатора. В системе ДК-ДА. С промежуточной очисткой от продуктов реакции и возвратом в колонну на последние слои катализатора.
-
Заданная производительность установки (в тоннах 100%-ной серной кислоты в сутки):
П (H2SO4) 600
Расчет адиабатического разогрева
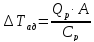
где Qр – тепловой эффект реакции 94,400[кДж/моль SO2]
А – концентрация SO2 = 0,095
Cр – теплоемкость смеси 0,252 [кал/л*газа*град]
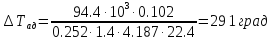
Расчет концентраций на слоях катализатора:
Из
формулы
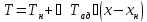 выражая x
,мы получим
выражая x
,мы получим
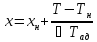
|
1 |
2 |
3 |
|
|
598 |
567 |
488 |
TH |
|
422 |
520 |
460 |
TK |
|
0 |
0.51 |
0.79 |
xн |
|
0.6 |
0.67 |
0.88 |
xp |
Материальный баланс:
SO2 + 0.5 O2 = SO3
x1 =0,88
После первой ступени газ идет на очистку от SO3, а это значит, что должен меняться объем потока и объемные доли газов, входящих в него.
Предположим,
что
 ,
тогда
,
тогда
![]()

![]()

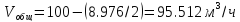
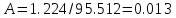
Рассчитаем
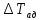
![]() для второй ступени:
для второй ступени:
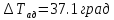
|
|
4 |
5 |
|
TH |
444 |
422 |
|
TK |
420 |
421 |
|
xн |
0 |
0,61 |
|
xp |
0,65 |
0,64 |
x2 =0,64
Материальный баланс

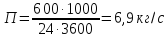
Реакции процесса:
![]()
![]()
Суммарная реакция:
![]()

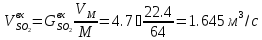
После сжигания SO2 было 12.8% отсюда общий объём смеси газа после сжигания составит:
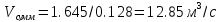
Остальные компоненты:
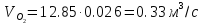
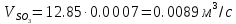
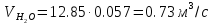

Составление материального баланса первой ступени
![]()
На
первую ступень поступило 9.5% SO2,
что составило 1.645⋅0.128=0.211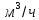
![]() .
Объёмы остальных газов не изменились.
.
Объёмы остальных газов не изменились.
x1=0.88
После Ι ступени получим:

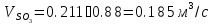

Для пересчета используем формулу
![]()
|
Приход |
|
|
Расход |
|
|
|
SO2 |
|
|
SO2 |
|
|
|
O2 |
|
|
O2 |
|
|
|
SO3 |
0 |
0 |
SO3 |
|
|
|
N2 |
10.13 |
|
N2 |
10.13 |
|
|
Σ |
|
|
|
|
|