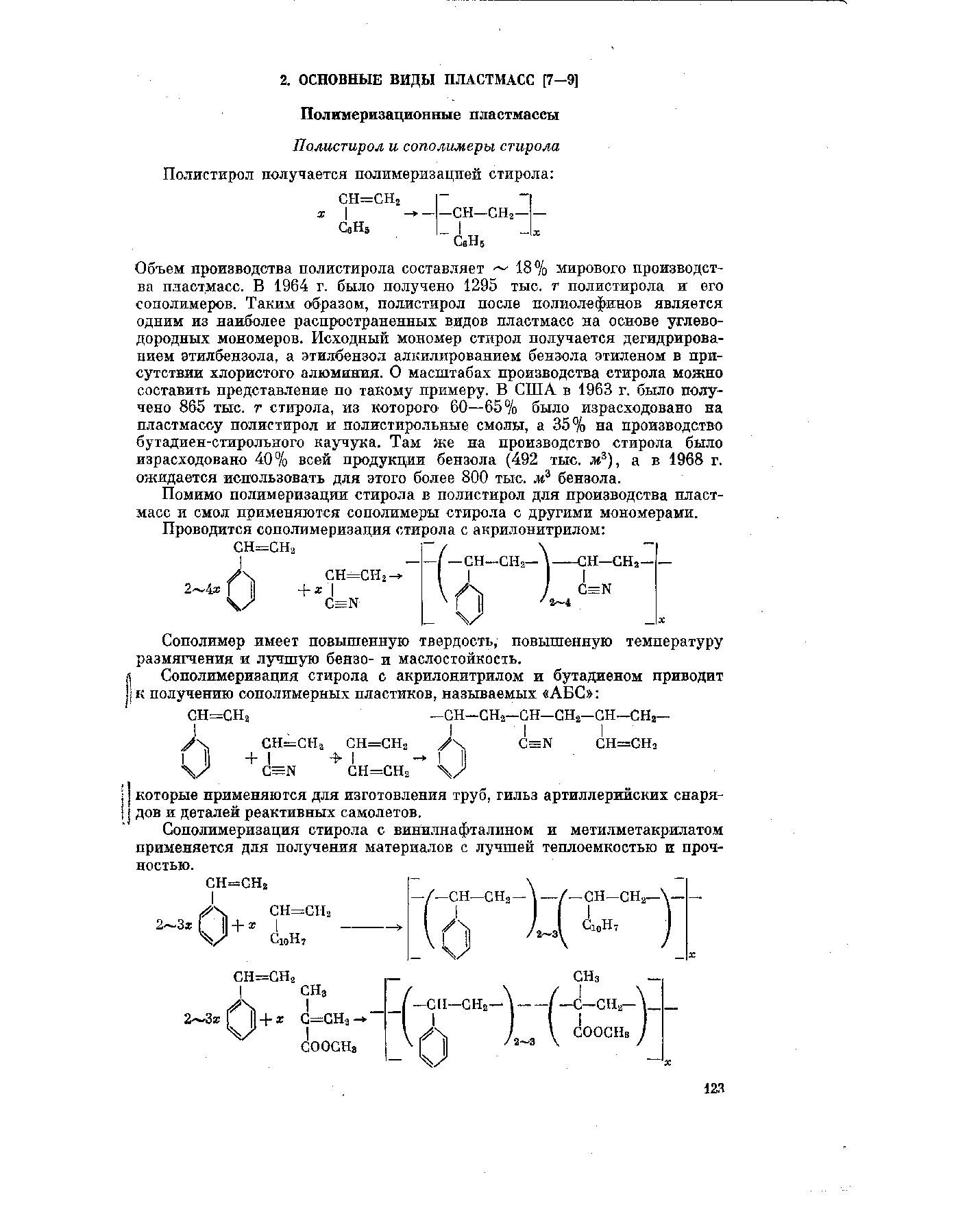
- •1.(22) В 3,72 г оксида металла содержится 2,75 г металла. Вычислить эквивалентные массы металла и оксида.
- •47. Сколько пар валентных электронов в электронной оболочке атома титана в нормальном состоянии?
- •197. Водный раствор замерзает при 271,5 к. Определите температуру кипения этого раствора, если криоскопическая и эбуллиоскопическая постоянные для воды равны 1,86 и 0,513, соответственно.
- •222. Напишите молекулярные и ионные уравнения реакций между растворами: а) хлорида аммония и гидроксида кальция; б) сульфата алюминия и сульфида натрия; в) нитрата кальция и силиката натрия.
- •272. Уравняйте окислительно-восстановительные реакции методом электронного баланса, укажите окислитель и восстановитель:
- •297. Алюминий склепан с медью. Какой из металлов будет коррозировать в кислоте, содержащей растворенный кислород? Напишите уравнения анодного и катодного процессов.
- •347. Хлороводород, полученный при действии серной кислоты на NaCl массой 58,5 г, растворили в воде массой 146 г. Вычислите массовую долю (%) нСl в растворе.
297. Алюминий склепан с медью. Какой из металлов будет коррозировать в кислоте, содержащей растворенный кислород? Напишите уравнения анодного и катодного процессов.
Cu(2+) +2e=Cu | E=0,34B Al - 3e=Al(3+) | E=-1,66B 3Cu(2+)+2Al=3Cu+2Al(3+)
Изделие из алюминия склёпано медью. Какой из металлов будет подвергаться коррозии с водородной деполяризацией, если эти металлы попадут в кислую среду (HCl)? Составьте уравнения проходящих при этом процессов, приведите схему образующегося гальванического элемента. Определите продукты коррозии
В реакциях с кислотами атомы алюминия окисляются ионами водорода в ионы алюминия, которые переходят в раствор: 2Al+6H+→2Al3+ +3H2h
Медь в электрохимическом ряду напряжения металлов находится за водородом, (т.е. её стандартный потенциал положительный) и с разбавленными кислотами не реагирует (положительно заряженные ионы меди не переходят в раствор).
В кристаллической решетке меди (в отличие от алюминия) свободные электроны не накапливаются. При соприкосновении этих двух металлов свободные электроны алюминия переходят к меди и восстанавливают на её поверхность ионы водорода: 2H+ +2e→H2h
Продуктами коррозии будет являться результат взаимодействия алюминия с соляной кислотой: 2Al+6HCl→2AlCl3+3H2h
Образуется гальванический элемент: (–) Al |AlCl3|Cu(+)
322. Напишите формулу комплексного соединения, полученного из следующих веществ: Co(NO2)3 + KNO2→. Определите заряд комплексообразователя, координационное число, заряд комплексного иона и назовите комплексное соединение.
347. Хлороводород, полученный при действии серной кислоты на NaCl массой 58,5 г, растворили в воде массой 146 г. Вычислите массовую долю (%) нСl в растворе.
2NaCl+H2SO4=2HCl+Na2SO4 n(HCl)=n(NaCl)=58,5\58,5=1 моль. масса HCl равна 36,5 г. масса раствора равна 146+36,5=182,5 массовая доля HCl=36,5\182,5=0,2 или 20% Ответ: 20%
372. Напишите электронные и молекулярные уравнения: а) Ве+NаОН, б) Мg+Н2SO4 (конц.) учитывая, что кислота восстанавливается максимально.
Реакция бериллия с водными растворами щелочей сопровождается выделением водорода и образованием гидроксобериллатов: Be + 2NaOH(р) + 2H2O = Na2[Be(OH)4] + H2 При проведении реакции с расплавом щелочи при 400—500 °C образуются диоксобериллаты: Be + 2NaOH(ж) = Na2BeO2 + H2 Mg+H2SO4(р-р) = MgSO4+H2 С концентрированной азотной и серной кислотами магний не реагирует – он пассивируется, однако при повышении температуры реакция с данными кислотами пойдет.
4Mg+5 H2SO4(конц.) = 4MgSO4+H2S+4H2O
437. Напишите схему сополимера стирола и акрилонитрила, считая, что образуется полимер с регулярным чередованием иономерных звеньев в соотношении 1:1. Помимо полимеризации стирола в полистирол , для производства пластмасс и смол применяются сополимеры стирола с акрилонитрилом.
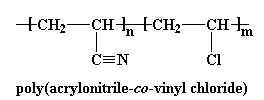
.