
- •Цвет меди и её соединений
- •Электропроводимость
- •Кристаллическая решетка меди
- •Окончание табл. 1
- •Химические свойства меди
- •Отношение к кислороду
- •Взаимодействие с водой
- •Получение меди
- •1. Метод электролиза
- •2. Металлотермический метод получения
- •3. Пирометаллургический способ получения меди
- •Опыт 1 Получение меди электролизом раствора. Определение электрохимического и химического эквивалентов меди
- •Теоретическая часть Никель Физические и химические свойства
- •Получение никеля
- •Опыт 2 Получение никелевого покрытия методом электроосаждения
- •Экспериментальная часть
- •Домашнее задание к лабораторной работе
- •Лабораторная работа № 2 физико-химические свойства полимерных материалов
- •Теоретическая часть Высокомолекулярные соединения
- •Продолжение табл. 1
- •Окончание табл. 1
- •Специальные добавки в пластмассы
- •Отношение волокон к реагентам
- •Окончание табл. 3
- •Полимеры классифицируют по следующим признакам.
- •Экспериментальная часть Опыт 1 Свойства полиэтилена (пэ) и полистирола (пс)
- •Опыт 2 Свойства поливинилхлорида (пвх)
- •Опыт 3 Свойства полиметилметакрилата (пмма)
- •Опыт 4 Свойства капрона
- •Физико-химические свойства полимерных материалов
- •Лабораторная работа № 3 получение стекол
- •Теоретическая часть Неорганические диэлектрики
- •Керамика
- •Установочная керамика
- •Основные свойства установочной радиокерамики
- •Основные свойства конденсаторной керамики
- •Сегнетокерамика
- •Вакуумная керамика
- •Жаростойкая керамика
- •Свойства нагревостойкой керамики
- •Основные физические, механические, электрические и химические свойства стекол
- •Химический состав некоторых промышленных стекол в весовых %
- •Опыт 1 Получение легкоплавких силикатных стекол
- •Окончание таблицы
- •Домашнее задание к лабораторной работе
- •Шкала коррозионной стойкости металлов по гост 5272-50
- •Экспериментальная часть
- •Определение скорости коррозии
- •Примечание
- •Диапазон сопротивлений
- •Опыт 1 Влияние pH среды на скорость коррозии железа. Измерение скорости коррозии
- •Гальванические покрытия
- •Подготовка поверхности
- •Экспериментальная часть
- •Определение никеля
- •Защита от коррозии Опыт 2 Скорость коррозии луженого железа в кислой среде
- •Опыт 3 Анодное и катодное покрытие для железа
- •Опыт 4 Влияние ингибиторов
- •Контрольные вопросы
- •Домашнее задание к лабораторной работе
- •Приложение 1
- •Приложение 2 Химия радиоматериалов Вариант 1
- •Химия радиоматериалов Вариант 2
- •Химия радиоматериалов Вариант 3
- •Химия радиоматериалов Вариант 4
- •Приложение 3 План ргр
- •Варианты
- •Приложение 4
- •Список литературы
- •Химия радиоматериалов сборник лабораторных работ и домашних заданий
- •6 30092, Г. Новосибирск, пр. К. Маркса, 20
Определение никеля
На поверхность пластинки нанесите стеклянной палочкой каплю разбавленной азотной кислоты (d = 1,2). Через несколько секунд снимите каплю фильтровальной бумагой и на то место, где была капля кислоты, нанесите сперва несколько капель NH4OH, а затем каплю раствора диметилглиоксима. Появление розового пятна указывает на присутствие никеля. Реакция между диметилглиоксимом и солями никеля, открытая известным советским химиком Л.А. Чугаевым, основана на образовании сложного комплексного соединения никельдиметилглиоксима
С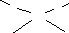 Н3-С=N-ОН
СН3-С=N-ОН
ОН-N=С-СН3
Н3-С=N-ОН
СН3-С=N-ОН
ОН-N=С-СН3
2 + Ni2+ 2Н+ + Ni
СН3-С=N-ОН СН3-С=N-О О-N=С-СН3
Защита от коррозии Опыт 2 Скорость коррозии луженого железа в кислой среде
А. Покрытие цельное. Коррозионный датчик с электродами из луженого железа погрузить в 0,001 М раствор HCl. Измерение скорости коррозии производить при множителе поддиапазона «10». Сопоставьте результаты опытов I и IIА. Какой металл корродирует?
Б. Покрытие нарушено. Коррозионный датчик с электродами с повреждённым покрытием погрузить в электролит того же состава и произвести аналогичные измерения, что и в пункте «А».
Данные опыта внести в табл. 12.
Таблица 12
|
№ п/п |
Материал образца |
Электролит HCl |
Поддиапа-зон изме-рений |
Rp |
Примечание |
|
|
Концент-рация |
pH |
|||||
|
1 |
Луженое железо (цельное покрытие) |
0,001 M |
3 |
10 |
|
Различие в величинах Rp опытов I и IIБ объясняется тем, что площадь нарушения покрытия меньше 2 см2 |
|
2 |
Луженое железо (нарушено покрытие) |
0,001 M |
3 |
10 |
|
|
В каком случае скорость коррозии больше (учтите, что величина скорости коррозии обратно пропорциональна значению Rp)?
В отчёте показать макрогальванопару Fe-Sn c направлением движения электронов и ионов. Записать электрохимическую схему данной гальванопары и электродные процессы.
Чем можно объяснить различия в величинах скорости коррозии образцов с цельным и нарушенным покрытием?
Сделайте вывод о том, какое это покрытие (анодное или катодное)? Надежно ли оно?
Опыт 3 Анодное и катодное покрытие для железа
А. Обнаружение ионов Fe2+ в растворе элекролита. При коррозии железа в растворе появляются ионы Fe2+, которые обнаруживаются раствором железосинеродистого калия (красной кровяной соли K3[Fe(CN)6]).
Качественная реакция на ион Fe2+: растворить в небольшом количестве воды кристаллы FeSO4, прибавить несколько капель раствора красной кровяной соли. Идёт реакция с образованием осадка темно-синего цвета (турнбулевой кислоты):
3FeSO4 + 2K3[Fe(CN)6] = Fe3[Fe(CN)6]2↓ + 3K2SO4
3Fe2+ + 2 [Fe(CN)6]3- = Fe3[Fe(CN)6]2↓.
турнбулева синь
Б. Коррозия оцинкованного и луженого железа в кислой и нейтральных средах. В две пробирки с 1 М раствором NaCl добавить несколько капель раствора K3[Fe(CN)6] и фенолфталеина. В одну пробирку поместить образец оцинкованного железа, а в другую – луженого с предварительно сделанными на их поверхности глубокими царапинами. В две другие пробирки налить 1 М раствор HCl, добавив в него несколько капель раствора K3[Fe(CN)6] и поместить в них образцы луженого и оцинкованного железа с нарушенным покрытием.
Дать постоять 5–10 минут. Что наблюдается? В отчёте объяснить причину качественных изменений и на рисунках показать макрогальванопары Fe-Sn и Zn-Fe c направлением движения электронов и ионов.
Записать электрохимичиеские схемы гальванопар и электродные процессы. Указать вид деполяризации в нейтральной (NaCl) и кислой (HCl) средах. В каком случае корродирует железо? Какое покрытие является более эффективным?
