
- •Семейство пировиноградной кислоты включает Ала, Сер, Гли, Цис и Тре
- •Цистеин образуется из метионина
- •Пролин синтезируется из глутаминовой кислоты
- •Основной член семейства -кетоглутаровой кислоты – глутаминовая кислота
- •У аргинина и пролина на пути к глутаминовой кислоте общий метаболит –глутаминоый полуальдегид
- •Глутамат, аспартат и аланин самые заменимые из заменимых.
- •Метионин, изолейцин и валин члены семейства сукцинил-КоА.
- •Н ачальные реакции катаболизма изолейцина и валина подобны катаболизму лейцина.
- •У валина четыре шага до сукцинил-КоА
- •Н арушение декарбоксилирования аминокислот с разветвленной цепью приводит к болезни «кленового сиропа»
- •У семейств фумаровой кислоты и ацетил-КоА есть общие аминокислоты.
- •Фенилаланин – предшественник тирозина. Основной и, по-видимому, единственной функцией фенилаланина, не считая участия в синтезе белков и пептидов, является использование его в качестве источника
- •Тирозин принадлежит трем семействам: фумарата, ацетоацетата и ацетил-КоА
- •Тирозинемия, тирозинурия и фенолацидурия –формы проявления нарушения катаболизма тирозина.
- •В механизме синтеза треонина и лизина есть общие реакции
- •Аминогруппы лизина не участвуют в переаминировании
- •Аминокислоты можно синтезировать из простых предшественников
- •Пути синтеза аминокислот можно сгруппировать в несколько логических модулей.
- •1.Мультимедийная презентация
Цистеин образуется из метионина
Хотя цистеин и относится к группе заменимых аминокислот он образуется в клетке из метионина – незаменимой аминокислоты. У микроорганизмов синтез цистеина – двухступенчатая реакция .и происходит с участие серина и ацетил-КoA, которые соединяясь, образуют O-ацетилсерин, и после присоединения серы образуется цистеина.
Метионин незаменимая аминокислота для человека, у микроорганизмов синтезируется из оксалоацетата. В процессе участвует сукцинил-КоА и цистеин в качестве донора серы. Оксалоацетат сначала преобразуется в гомосерин (см синтез треонина). Гомосерин затем присоединяет серу в два этапа и метилирование завершает образование метионина.
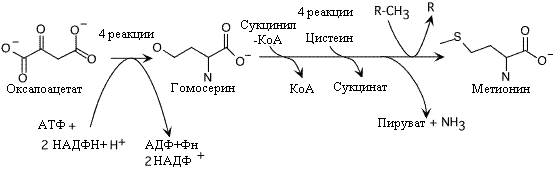
Синтез метионина. Донор метильной группы (R), N5,N10-метилен тетрагидроптероил.
Основной член семейства -кетоглутаровой кислоты – глутаминовая кислота
Глутаминовая кислота занимает важное место в промежуточном обмене нескольких аминокислот. К ним относятся глутамин, пролин, аргинин и гистидин.

Реакция превращения глутамина в глутаминовую кислоту напоминает превращение аспарагина в аспарагиновую и катализируется глутаминазой. Учитывая, что глутамин - главная транспортная форма аммиака глутаминаза
и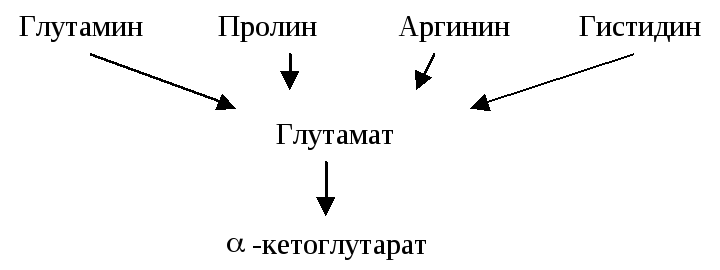 грает
важную роль в органах, активно использующих
аммиа и прежде всего в печени и почках.
грает
важную роль в органах, активно использующих
аммиа и прежде всего в печени и почках.
Пролин синтезируется из глутаминовой кислоты
Синтез пролина включает четырехэтапный процесс, начинающийся с глютамата и представляет реакции обратные его распаду. Одна молекула АТФ и два НАДФH + Н+ используются на моль пролина.

Синтез пролина.
Гистидин – «полузаменимая» аминокислота.
Взрослый человек может поддерживать азотистое равновесие на диете, лишенной гистидина. Но растущие организмы и длительное пребывание на безгистидиновой диете вызывают нарушения роста. Ничего не известно о механизме синтеза гистидина у людей и животных, но у микроорганизмов этот путь изучен подробно. Путь синтеза гистидина переплетается с биосинтезом нуклеотидов (в частности пурина), довольно сложен и, по-видимому, универсален для всех организмов, способных синтезировать гистидин. Первые пять этапов пути используют рибозу от фосфорибозилпирофосфата (ФРПФ) и превращают ее в имидазолилглицеролфосфат. После формирования имидазольного кольца, глутамат поставляет аминогруппу и образовавшийся амин окисляется в гистидин на последнем этапе пути. Энергия используется в форме АТФ (в этом случае элементы молекулы АТФ, фактически становится частью аминокислоты) и пирофосфата, который отщепляется от ФРПФ, и помогает АТФ проводить реакцию.
Самое маленькое семейство у оксалацета
В оксалоацетат
превращаются 2 аминокислоты аспарагин
и аспарагиновая кислота. Два фермента
катализируют это превращение. Аспарагиназа
катализирует гидролитическое
дезаминирование амидной группы аспарагина
и образование аспарагиновой кислоты,
а последняя под влиянием
аспартатаминотрансферазы (АСТ) теряет
аминогруппу и становится оксалоацетатом.
Эта реакция обеспечивает цикл трикарбоновых
кислот оксалоацет атом
(анаплеротическая реакция.)
атом
(анаплеротическая реакция.)
АСТ активна в сердечной мышце, что послужило основанием для применения препаратов, содержащих аспарагиновую кислоту в кардиологической клинике. Аспарагиназа используется при лечении некоторых форм аспарагина и образование аспарагиновой кислоты, а последняя под влиянием аспартатаминотрансферазы (АСТ) теряет аминогруппу и становится оксалоацетатом. Эта реакция обеспечивает цикл трикарбоновых кислот оксалоацетатом (анаплеротическая реакция). АСТ активна в сердечной мышце, что послужило основанием для применения препаратов, содержащих аспарагиновую кислоту в кардиологической клинике. Аспарагиназа используется при лечении некоторых форм лейкозов для разрушения аспарагина, который является незаменимой аминокислотой для отдельных форм предшественников лейкоцитов.
