
- •Основы химической термодинамики, кинетики, равновесия и электрохимии
- •1. Основные закономерности протекания химических реакций
- •1.1. Энергетика химических реакций
- •1.2. Направленность химических процессов
- •2. Основы химической кинетики
- •2.1. Скорость химической реакции
- •2.2. Химическое равновесие
- •2.3. Смещение химического равновесия
- •3. Основы электрохимии
- •3.1. Гальванический элемент
- •3.2. Коррозия металлов и методы защиты от коррозии
- •3.3. Электролиз
- •Список литературы
- •Содержание
- •1. Основные закономерности протекания химических реакций 1
- •Энергетика химических реакций 1
- •Основы химической термодинамики, кинетики, равновесия и электрохимии
3.1. Гальванический элемент
Гальванический элемент - это устройство, в котором, в результате протекания окислительно-восстановительной реакции, возникает электрический ток. Любой гальванический элемент состоит из двух электродов - проводников электрического тока (обычно металлов), погруженных в растворы электролитов и соединенных между собой. Электрод, на котором проходит процесс окисления (отдача электронов), называется анодом; электрод, на котором осуществляется восстановление (присоединение электронов) - катодом. В электрохимии широко используется понятие электродный потенциал. Электродный потенциал возникает на поверхности раздела - электрод - раствор при погружении металла (Me) в воду или раствор, содержащий ионы данного металла (Mez+). На границе металл - раствор устанавливается равновесие
Me
↔Mez++
Z
![]() ,
,
которое обусловливает образование двойного электрического слоя. Наличие двойного электрического слоя приводит к возникновению разности потенциалов между металлом и раствором, которую принято называть электродным потенциалом металла и обозначать φМе z+/Mе. Измеряется потенциал в вольтах (В). Электрод принято изображать в виде схемы:
Me|Mez+,
где вертикальная черта обозначает поверхность раздела металл -раствор.
Если металл опущен в раствор собственной соли с концен- трацией катионов металла, равной 1 моль/л при температуре 298 К (25 °С), то возникающий потенциал называют стандарт- ным и обозначают φМеz+/Mе. Непосредственно определить потенции- ал отдельного электрода нельзя, его измеряют путем сравнения с потенциалом эталонного электрода. Чаще всего для этой цели используют стандартный водородный электрод, который схематически изображается так: Pt, H2 | 2H+. Платина не участвует в окислительно-восстановительной реакции и выполняет роль проводника электронов. На границе раздела фаз в водородном электроде устанавливается равновесие:
Н22Н+ + 2e.
19
Величину потенциала такого электрода принимают за ноль (при всех температурах) и называют стандартным потенциалом водородного электрода φ0H+/H2 = 0.
Располагая металлы в порядке возрастания значений их стандартных электродных потенциалов, получают электрохимический ряд напряжений металлов: Li, К, Ва, Sr, Са, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H2, Sb, Bi, Cu, Hg, Ag, Pt, Au.
Числовые значения стандартных потенциалов металлов приведены в таблицах, имеющихся в учебник?" по общей химии. Ряд напряжений характеризует химические свойства металлов: чем меньше алгебраическое значение φ0Меz+/Mе, тем сильнее выражены восстановительные свойства металлов, т.е. легче окисляются (отдают электроны) и труднее восстанавливаются из своих ионов.
Величина электродного потенциала металла φМеz+/Mе зависит от величины φ0Меz+/Mе концентрации его ионов в растворе, СMе z+, температуры Т и выражается уравнением Нернста:
![]()
где R - газовая постоянная равная 8,3 Дж/(моль*К); F - число Фа-радея.
Уравнение Нернста при Т = 298 К принимает вид:
![]()
Если два электрода из разных металлов(МеI и МeII; MеIZ+/MеI, < <MеIIZ+/MеII) соединить между собой, образуется гальванический элемент, который принято изображать следующим-образом:
MeI|MeIz+||MeIIz+|MeII.
Двойная вертикальная черта обозначает границу между растворами солей (растворы разделены пористой перегородкой или электролитическим ключом для предупреждения их смешивания). Причиной возникновения и протекания электрического тока в гальваническом элементе является разность электродных потенциалов взятых металлов (MеIZ+/Mе MеIIZ+/Mе). Электрод, изготовленный из металла, потенциал которого имеет меньшее значение (МеI), является анодом, на нем протекает процесс окисления атомов металла I (растворение металла):
20
MeI-Ze=Mez+ (1)
Образующиеся ионы MeIZ+ переходят в раствор, а электроны по проводнику, соединяющему металлические пластины, перемещаются к электроду с большим значением электродного потенциала, выполняющему роль катода (МeII), всегда φкатода > φанода. На поверхности катода происходит восстановление ионов металла МеIIZ+ из раствора:
MeIIZ+ + Ze = MeII. (2)
Атомы металла II осаждаются на электроде. Суммарное уравнение реакции, протекающей при работе гальванического элемента, получающееся при сложении уравнений (1) и (2), называется токообразующей реакцией.
Анодный процесс MeI - Ze =MeIZ+ Катодный процесс MeII+ + Z e = МеII
Токообразующая реакция MeI, + МеIIZ+ = MeIZ+ + МеII.
В схеме гальванического элемента анод (МеI) принято записывать слева, а катод (МeII) - справа.
Максимальное значение напряжения гальванического элемента называется электродвижущей силой (ЭДС). Для любого работающего элемента ЭДС - величина положительная и может быть вычислена по формуле:
ЭДС = φкатода > φанода.
Гальванический элемент можно составить, используя электроды из одного металла, опущенные в растворы соли этого металла разной концентрации. В этом случае гальванический элемент называют концентрационным. Примером может служить цинковый концентрационный элемент
IZn -|ZnCl2 (СI) || ZnCl2 (С2) | Zn2,
где CI и С2 - концентрации ионов цинка (Zn2+) в растворах. Если
CI < С2 - то, согласно уравнению Нернста IZn2+/Zn<2Zn2+/Zn, левый электрод (1) будет анодом, а правый (2) - катодом. При работе этого гальванического элемента протекают процессы:
Анодный процесс Zn - 2 e = Zn2+
Катодный процесс Zn2+ + 2 e = Zn0,
21
Электроны в концентрационном гальваническом элементе перемещаются от электрода с меньшей концентрацией катионов металла в растворе (анода) к электроду с большей концентрацией соли в растворе (катоду).
Пример 1. Составьте схему гальванического элемента, в котором роль катода выполняет никелевая пластина, опущенная в раствор сульфата никеля, концентрация раствора равна 0,001 моль/л. Напишите уравнения процессов, протекающих на электродах при работе этого элемента, и вычислите ЭДС.
Решение. По таблице находим значение стандартного электродного потенциала никеля: (0Ni 2+/Ni = - 0,23 В. По уравнению Нернста рассчитываем потенциал никелевого электрода при концентрации ионов никеля 0,001 моль/л
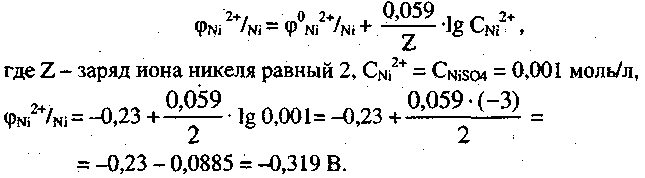
Итак, потенциал никелевого электрода равен -0,319 В и этот электрод выполняет роль катода. Анодом может служить любой металл, имеющий меньшее алгебраическое значение потенциала, например марганец 0мn2+/мn = - 1,18 В. В качестве электролита выберем раствор MnSO4 с концентрацией ионов Мn2+ 1 моль/л (можно выбрать и другое значение концентрации). Запишем схему гальванического элемента, располагая анод слева, катод справа и указывая в скобках концентрации электролита:
(А) Мn | MnSO4 (1м) || NiSO4 (0.001 м) | Ni (К).
При работе этого элемента протекают реакции:
Анод Мn - 2 e - Мп2+ (окисление)
Катод Ni2+ + 2 е = Ni0 (восстановление)
Мn + Ni2+ = Mn2+ + Ni (токообразующая реакция)
или в молекулярном виде:
Мn + NiSO4 = MnSO4 + Ni.
22
ЭДС гальванического элемента рассчитываем из формулы:
ЭДС = катода -анода = ЭДС = Ni2++/Ni - Mn2+/Mn.
Электродные потенциалы Ni2++/Ni = -0,319 В ≈ -0,32 В; Mn2+/Mn =
0 Mn2+/Mn = - 1,18 В, так как при концентрации соли 1 моль/л = 0, ЭДС = -0,32 - (-1,18) = 0,86 В.
