
- •Биосинтез рнк: строение промоторов, взаимодействие рнк-полимеразы с промоторами.
- •Характеристика рнк-полимераз у про- и эукариот.
- •Этапы биосинтеза рнк: инициация, элонгация, терминация.
- •Инициация
- •Элонгация.
- •Терминация.
- •Компоненты белоксинтезирующей системы у прокариот: мРнк, рРнк, тРнк; белковые факторы инициации, элонгации и терминации; 70s рибосомы.
- •Компоненты белоксинтезирующей системы эукариот (мРнк, рРнк, тРнк; мяРнк, белковые факторы инициации, элонгации и терминации; 80s рибосомы).
- •Строение рибосом, характеристика функциональных центров.
- •Биосинтез белка: активация аминокислот. Характеристика аминоацил-тРнк-синтетаз.
- •Инициация трансляции в прокариотических клетках.
- •46. Элонгация и терминация трансляции прокариот.
- •47. Генетический код. Основные характеристики.
- •Характеристика этапов трансляции в эукариотических клетках.
- •Сворачивание (фолдинг) полипептидной цепи. Роль ферментов и шаперонов в этом процессе.
- •Посттрансляционные модификации белков (из интернета).
- •1.Динамическая биохимия. Характеристика метаболических путей
- •1.1 Характеристика метаболических путей
- •2. Распад углеводов в желудочно-кишечном тракте. Роль амилолитических ферментов.
- •2.1 Расщепление углеводов в пищеварительном тракте
- •5. Трегалаза (не давала в лекции)
- •В последующей реакции, катализируемой ферментом фосфоенолпируваткарбоксикиназой, из оксалоацетата образуется фосфоенолпируват. Реакция Mg2-зависимая и донором фосфата служит gtp.
- •5. Окислительное декарбоксилирование пирувата. Строение пируватдегидрогеназного комплекса, регуляция активности.
- •6.Цикл лимонной кислоты. Регуляция цикла.
- •7.Дыхательная цепь: организация компонентов в виде 4-х белковых комплексов. Характеристика дыхательных переносчиков (fmn, железосерные белки, убихиноны, цитохромы).
5. Трегалаза (не давала в лекции)
Трегалаза – гликозидазный комплекс, гидролизующий связи между мономерами в трегалозе (дисахариде, содержащемся в грибах).
Строение трегалозы:
Совместное действие всех перечисленных ферментов завершает переваривание пищевых олиго- и полисахаридов с образованием моносахаридов, основной из которых – глюкоза, а также фруктоза и галактоза, манноза, ксилоза, арабиноза.
. Гликолиз. Регуляция гликолиза. Гликогенолиз. Регуляция процесса на уровне гликогенфосфорилазы.
Гликолиз– последовательность ферментативных реакций, приводящих к превращению глюкозы в пируват с одновременным образованием ATP.
Анаэробный гликолиз – сложный ферментативный процесс распада глюкозы, протекающий без потребления О2. Конечным продукт - молочная кислота, также образуется ATP. Суммарное уравнение гликолиза:
![]()
В анаэробных условиях гликолиз – единственный процесс в животном организме, поставляющий энергию. Внутриклеточно гликолиз локализуется в цитоплазме.
1. Фосфорилирование, т.е. перенос остатка ортофосфата на глюкозу за счет ATP. Фермент - гексокиназа:

Освобождение большого кол-ва Е делает эту реакцию практически необратимой.
2. превращение глюкозо-6-фосфата во фруктозо-6-фосфат. Фермент -глюкозо-6-фосфат-изомераза:

3. Фосфорилирование фруктозо-6-фосфат за счет второй молекулы ATP ферментом фосфофруктокиназа:

эта реакция определяет скорость гликолиза в целом.
Фосфофруктокиназа - аллостерический фермент, ингибируется ATP и стимулируется АMP.
4. фруктозо-1,6-бисфосфат расщепляется на две фосфотриозы. фермент - альдолаза.
![]()
5. изомеризация триозофосфатов. Фермент - триозофосфатизомераза:
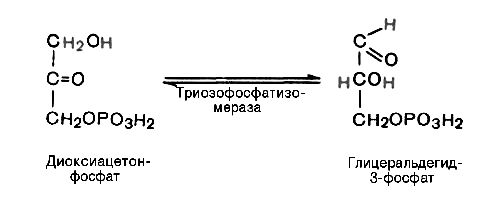
В последующие реакции включается только глицеральдегид-3-фосфат.
6. глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента NAD+ и неорганического фосфата подвергается своеобразному окислению с образованием 1,3-бисфосфоглицериновой кислоты и восстановленной формы NAD (NADH).
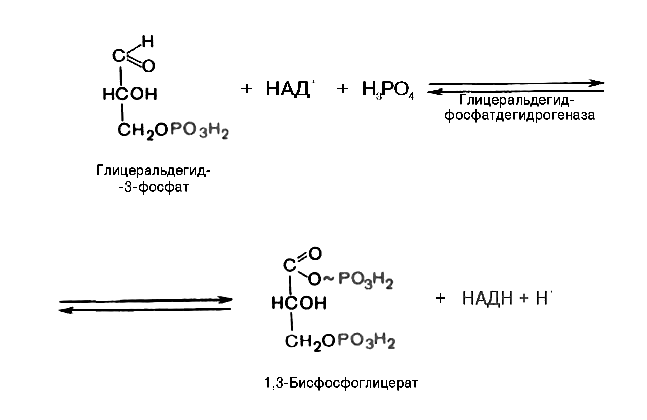
1,3-Бисфосфоглицерат - высокоэнергетическое соединение.
7. Фермент - фосфоглицераткиназа; при этом происходит передача богатого энергией фосфатного остатка (фосфатной группы в положении 1) на ADP с образованием ATP и 3-фосфоглицериновой кислоты (3-фосфоглицерат):
![]()
8. Происходит внутримолекулярный перенос оставшейся фосфатной группы, 3-фосфоглицериновая кислота превращается в 2-фосфоглицериновую кислоту (2-фосфоглицерат). Легкообратима, протекает в присутствии Mg2+. Кофактор фермента - 2,3-бисфосфоглицериновая кислота аналогично тому, как в фосфоглюкомутазной реакции роль кофактора выполняет глюкозо-1,6-бисфосфат:

9. фермент - енолаза, при этом 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится высокоэргической:
![]()
10. разрыв высокоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на ADP (субстратное фосфорилирование). Фермент - пируваткиназа:
![]() Для
действия пируваткиназы необходимы ионы
Mg2+,
а также одновалентные катионы щелочных
металлов (К+
или др.) Реакция практически необратима.
Для
действия пируваткиназы необходимы ионы
Mg2+,
а также одновалентные катионы щелочных
металлов (К+
или др.) Реакция практически необратима.
11. восстановление ПВК, образование малата. Фермент – лактатдегидрогеназа, кофермента NADН (образовавшегося в 6й реакции):

Биологическое значение гликолиза - образование богатых энергией фосфорных соединений. На первых стадиях гликолиза затрачивается две молекулы ATP (гексокиназная и фосфофруктокиназная реакции). На последующих образуются четыре молекулы ATP (фосфоглицераткиназная и пируваткиназная реакции). Таким образом, энергетическая эффективность гликолиза в анаэробных условиях составляет две молекулы ATP на одну молекулу глюкозы.
Осн. реакция лимитирующая скорость гликолиза - фосфофруктокиназная. Вторая реакция, лимитирующая скорость и регулирующая гликолиз, – гексокиназная реакция. Кроме того, контроль гликолиза осуществляется также лактатдегидрогеназы и ее изоферментами.
4. Спиртовое брожение. Глюконеогенез.
Спиртовое и молочнокислое брожение – основные источники энергии некоторых микроорганизмов в анаэробных условиях.
Спиртовое
брожение осуществляется так называемыми
дрожжеподобными организмами, а также
некоторыми плесневыми грибками. Суммарная
реакция спиртового брожения:
![]()
Механизм процесса очень близок к гликолизу. Расхождение начинается лишь после этапа образования пирувата. При гликолизе пируват при участии фермента ЛДГ и кофермента NADH восстанавливается в лактат. При спиртовом брожении этот конечный этап заменен двумя другими ферментативными реакциями: пируватдекарбоксилазной и алкогольдегидрогеназной.
В дрожжевых клетках (спиртовое брожение) пируват вначале подвергается декарбоксилированию - образуется ацетальдегид. Данная реакция необратима, катализируется ферментом пируватдекарбоксилазой, который требует наличия ионов Mg2+ и кофермента (TРP):
![]() Образовавшийся
ацетальдегид присоединяет к себе
водород, отщепляемый от NADH,
восстанавливаясь при этом в этанол.
Реакция катализируется ферментом
алкогольдегидрогеназой:
Образовавшийся
ацетальдегид присоединяет к себе
водород, отщепляемый от NADH,
восстанавливаясь при этом в этанол.
Реакция катализируется ферментом
алкогольдегидрогеназой:
![]()
Конечные продукты - этанол и СО2, а не молочная кислота, как при гликолизе.
Существуют и другие виды брожения, конечными продуктами которых могут являться пропионовая, масляная и янтарная кислоты, а также другие соединения.
Глюконеогенез – процесс синтеза глюкозы de novo из неуглеродных предшественников. Главная функция - поддержание уровня глюкозы в крови во время голодания и интенсивной физической работы. Наиболее активно процесс протекает в печени, менее интенсивно в корковом слое почек и слизистом эпителии кишечника. От недостатка глюкозы в крови, прежде всего страдает головной мозг.
Большинство реакций глюконеогенеза протекает за счет обратимых реакций гликолиза и катализируется теми же ферментами. Однако образование фосфоенолпирувата, гидролиз фруктозо-1,6-бисфосфата и глюкозо-6-фосфата термодинамически необратимы и протекают другими путями.
Фосфоенолпируват образуется из пирувата в ходе двух реакций: пируват из цитозоля переносится в митохондрии и там карбоксилируется с образованием оксалоацетата.
Митохондриальный фермент пируваткарбоксилаза, катализирующий данное превращение пирувата, в качестве кофермента содержит биотин. Реакция протекает с затратой молекулы АТР.
![]()
Для оксалоацетата внутренняя мембрана митохондрий непроницаема, транспорт оксалоацетата в цитоплазму клетки происходит с помощью малатного челночного механизма, смысл которого заключается в восстановлении оксалоацетата до малата под действием митохондриального фермента малатдегидрогеназы.
Малат выходит в цитоплазму, где цитоплазматическая малатдегидрогеназа окисляет малат до оксалоацетата. Митохондриальная малатдегидрогеназа NADH-зависимая, а цитозольная в качестве кофермента содержит NAD+
![]()
