
PDF-лекции с картинками / 11 ревматические
.pdf151
РЕВМАТИЧЕСКИЕ БОЛЕЗНИ
Составил профессор Ю.В.Крылов, 2002.
Мы с Вами уже говорили, что основной тенденцией развития медицины, и, причем во многом благодаря клинико-анатомическому направлению, является выделение новых нозологических единиц из групп родственных заболеваний. В то же время есть примеры, когда отдельные заболевания по общим признакам объединяют на основании их клинических и морфологических особенностей в группы. Таким примером являются коллагеновые болезни. В 1941-42 немец Клемперер выделил группу заболеваний, объединяющим признаком которых явилось наличие фибриноидных превращений коллагеновых волокон, и он назвал эти болезни коллагенозами.
Сейчас системные заболевания соединительной ткани называют ревматическими болезнями, поскольку показано, что страдают не только коллагеновые волокна, но и основная субстанция и клетки соединительной ткани, при этом в основе повреждения соединительной ткани лежат нарушения иммунного гомеостаза.
К коллагеновым или ревматическим болезням относятся: 1)ревматизм, 2)ревматоидный артрит, 3)системная красная волчанка, 4)склеродермия, 5)узелковый периартериит и 6)дерматомиозит. Ранее считавшееся разновидностью ревматоидного артрита поражение связочного аппарата позвоночника, выделено также в качестве нозологической единицы (Болезнь Бехтерева).
Основными критериями коллагеновых заболеваний являются: 1) системная дезорганизация соединительной ткани; 2) повреждение сосудов микроциркуляторного русла; 3) нарушение иммунного гомеостаза; 4) прогрессирующее течение патологического процесса; 5) благоприятное влияние кортикостероидной терапии.
1) Дезорганизация соединительной ткани при коллагеновых болезнях протекает с развитием фазовых изменений: мукоидного набухания, фибриноидного набухания, фибриноидного некроза с ответной клеточной пролиферацией и исходом в склероз. При этом в склерозированных участках вновь могут возникать явления фибриноидного некроза. Такие изменения характерны для всех коллагеновых болезней. Однако каждая нозологическая форма имеет свои особенности. При ревматизме преобладает обратимая фаза мукоидного набухания, а клеточная реакция носит характер типичной для ревматизма гранулемы. При ревматоидном артрите и системной красной волчанке преобладают необратимые изменения - фибриноидный некроз, при склеродермии - склероз. Далее, несмотря на системное поражение соединительной ткани при коллагеновых болезнях, для каждого заболевания характерна преимущественная локализация процесса: при ревматизме - соединительная ткань сердца, при ревматоидном артрите - суставов, при
152
склеродермии - кожи, при системной красной волчанке - строма и сосуды многих внутренних органов, при узелковом периартериите сосуды.
2) Повреждение сосудов микроциркуляторного русла (артериолы, прекапилляры, капилляры, венулы) ведет к нарушению обменных процессов в строме органов. Повреждение микроциркуляторного русла (васкулиты) являются следствием иммунопатологических процессов - реакций гиперчувствительности немедленного и замедленного типов. При реакции гиперчувствительности немедленного типа в крови циркулирует большое количество иммунных комплексов, которые, фиксируясь на стенке сосудов, повреждают ее. Эти комплексы обнаруживают методом иммунофлюоресценции. Именно они вызывают фибриноидные изменения сосудов с некрозом стенки, иногда присоединяется тромбоз с последующим склерозом. При реакции замедленного типа возникают клоны сенсибилизированных лимфоцитов через бласттрансформацию тимус зависимых лимфоцитов. Они реагируют с антигеном, оказывая на стенку сосудов цитотоксическое действие. Морфологическим выражением гиперчувствительности замедленного типа является появление лимфоидно-макрофагальных инфильтратов по ходу сосудов. При этом повышается проницаемость сосудов и пропотевание плазменных белков, которые всегда присутствуют в очагах дезорганизации соединительной ткани.
3.Нарушение иммунного гомеостаза выражается в том, что при коллагеновых болезнях в период обострения со стороны органов иммуногеза /костный мозг, лимфоузлы, селезенка, тимус/ отмечается реакция бласттрансформации и плазматизации/. Последняя связана с продукцией аутоантител. Поэтому в крови больных регистрируется гипергаммаглобулинэмия и противотканевые аутоантитела. Однако ведущее место в повреждении принадлежит не аутоантителам, а циркулирующим в крови иммунным комплексам (антиген-антитело- комплимент). Последний обладает непосредственно лизирующим эффектом. Это общие механизмы нарушения иммунного гомеостаза, однако, при каждом коллагеновом заболевании они имеют свои особенности.
4.Прогрессирующее течение с ремиссиями и обострениями характерно для всех коллагеновых болезней, поэтому прогноз, как в отношении инвалидности, так и продолжительности жизни не благоприятный.
5.Основным методом лечения этих заболеваний является кортикостероидная терапия благодаря воздействию на систему гиалуроновая кислота-гиалуроиноза. В ряде случаев даже при неясном диагнозе коллагеноза, проводят пробную терапию этими препаратами, и улучшение состояния больного свидетельствует в пользу такого диагноза.
Ревматизм - от греческого глагола "rey"-теку или болезнь Сокольского-Буйо - это инфекционно-аллергическое заболевание с
153
преимущественным поражением сердца и сосудов, волнообразным течением, периодами обострения (атаки) и затихания (ремиссии). Ревматизм самая частая и распространенная коллагеновая болезнь. Среди сердечно-сосудистых заболеваний причиной смерти в возрасте до 20 лет в 98% является ревматизм. Чаще всего ревматизмом страдают дети в возрасте от 7 до 12 лет. У девочек болезнь встречается чаще. За исключением болезни Бехтерева женщины вообще чаще болеют коллагеновыми болезнями.
В этиологии ревматизма многочисленными исследованиями подтверждена роль бета гемолитического стрептококка типа А. Установлено, что гемолитический стрептококк типа А обладает активными энзимными системами и токсинами, антигенная структура которых близка к тканевым антигенам сердца. В сыворотке больных ревматизмом обнаружены повышенные титры антител к энзимам и токсинам стрептококка, а также кардиальные аутоантитела.
Патогенез. Клинически ревматизму, как правило, предшествует тонзиллярная стрептококковая инфекция, ведущая к сенсибилизации организма. Антигенная общность стрептококка и тканей сердца приводит к возникновению перекрестной иммунной реакции, при которой образуются антикардиальные аутоантитела. Циркулирующие в крови антистрептококковые антитела и иммунные комплексы (в их состав входит стрептококковый антиген, антитело и комплимент) повреждают основное вещество соединительной ткани сосудов микроциркуляторного русла, что приводит к проникновению аутоантител в ткани внутренних органов. Осаждение иммунных комплексов в ткани вызывает развитие гиперергического воспаления как гиперергической реакции немедленного типа. Сенсибилизированные лимфоциты фиксируют на себе аутоантигены соединительной ткани миокарда и оказывают на сердечную ткань цитотоксический эффект. Развивается гиперергическая реакция замедленного типа в сердце развиваются типичные для ревматизма АшофТалалаевские гранулемы. С помощью электронно-микроскопического исследования показано, что основными клетками этих гранулем являются макрофаги. Они трансформируются из моноцитов крови и осуществляют процессы фагоцитоза в области повреждений соединительной ткани. На высоте активной фазы процесса отмечается плазматизация т.е. увеличение количества плазматических клеток, которые как Вы знаете, продуцируют иммуноглобулины.
Клинически обострение процесса характеризуется повышением температуры, болями в суставах, сердце, а также развернутой лабораторной картиной в виде ускорения СОЭ, повышения титра анттистрептококковых антител и т.д.
Патологическая анатомия. Морфологические изменения при ревматизме складываются из четырех основных процессов, тесно связанных друг с другом: 1. Дезорганизация основного вещества и
154
волокон соединительной ткани; 2. Образования специфических для ревматизма гранулем; 3. Возникновения неспецифического экссудативнопролиферативного воспаления; 4. Развития в исходе этих процессов склероза и гиалиноза.
1.Процессы дезорганизации соединительной ткани подробно изучены А.И.Струковым и Беглоряном. Для ревматизма как мы уже говорили характерно преобладание мукоидного набухания, когда происходит перераспределение кислых мукополисахаридов и накопление преимущественно гиалуроновой кислоты в коллагеновых волокнах и межуточном веществе стромы миокарда, клапанов сердца и стенок коронарных сосудов. Гидрофильность кислых мукополисахаридов вызывает набухание, а их присутствие в свободном виде феномен метахромазии. Углубление процесса приводит к фибриноидному набуханию и фибриноидному некрозу, при которых в очагах дезорганизации всегда присутствуют плазменные белки (альбумины, глобулины, фибрин), которые выходят из сосудистого русла вследствие повышения проницаемости сосудистой стенки. Фибриноидное набухание
инекроз необратимы и вызывают ответную реакцию со стороны клеток соединительной ткани с исходом в склероз.
2.Образуются гранулемы, описанные в 1904 немецким патологом Ашофом и более подробно систематизированные по динамике Талалаевым в 1929 году. Эти гранулемы возникают как ответная реакция на фибриноидный некроз. Типичные гранулемы образуются только в сердце (чаще в ушке левого предсердия). Похожие, без крупных базофильных макрофагов, встречаются в суставных сумках, сухожилиях, апоневрозах, перитонзиллярной соединительной ткани, в строме других органов. В сердце гранулемы располагаются в периваскулярной соединительной ткани миокарда, в пристеночном и клапанном эндокарде. Они состоят из крупных макрофагальных клеток моноцитарного генеза с большими ядрами и базальной цитоплазмой за счет большого количества в них РНК. Между ними и по периферии гранулемы всегда присутствуют лимфоциты. Выделяют гранулемы "цветущие" в центре которых видны глыбки фибриноидного некроза; "увядающие" когда клетки гранулемы начинают вытягиваться, среди них появляются фибробласты и "рубцующиеся", когда фибриноид полностью рассасывается появляются аргирофильные, а затем и коллагеновые волокна. Цикл развития гранулемы составляет от 3 до 4 месяцев.
3.Экссудативно-пролиферативное воспаление при ревматизме неспецифического характера и наблюдается в интерстиции миокарда, особенно интенсивно вокруг гранулем. Интерстиций пропитывается серозным экссудатом с примесью разнообразных клеточных элементов (лимфоцитов, гистиоцитов, эозинофилов и нейтрофильных лейкоцитов). Экссудативный процесс наблюдается также и в серозных листках (в
эпикарде и перикарде с выпотом в сердечную сорочку, реже в
155
плевральных листках, еще реже в брюшине /но об этом важно знать, это тот перитонит, при котором хирургу нечего делать в брюшной полости/. Выпот в полости имеет серозно-фибринозный характер, что впоследствии приводит к организации фибрина и образованию спаек.
4. Склероз и гиалиноз развиваются в исходе фибриноидных изменений и клеточных реакций. В очагах склероза при повторных атаках вновь могут образовываться очаги фибриноида.
Различают четыре клинико-морфологические формы ревматизма:
1.Полиартритическая, при которой в клинике ведущим является припухание, краснота и боли в суставах. В суставах возникает серозное воспаление. В синовиальных оболочках обнаруживаются атипичные гранулемы.
По образному выражению Лагеса "ревматизм лижет суставы и кусает сердце", поэтому наиболее частой формой ревматизма является
2.Кардиоваскулярная форма. При ней поражаются эндокард, миокард
иперикард, т.е. ревматический панкардит. Ревматический эндокардит. При нем поражаются пристеночный эндокард, хорды и створки клапанов. По характеру поражения различают четыре формы ревматического эндокардита:
1)Вальвулит, при котором происходит мукоидное набухание и фибриноидные изменения створок клапана. Эндотелий не повреждается и поэтому отложений тромботических масс на клапане нет.
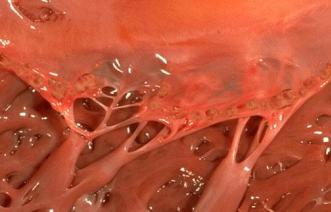
2)Острый бородавчатый эндокардит сопровождается повреждением эндотелия и образованием по замыкающему краю створок тромботических наложений в виде бородавок (рис.1, 2).
Рис.1 Острый бородавчатый эндокардит при ревматизме: мелкие уплощенные бородавчатые наложения на створке митрального клапана.
3)Фибропластический развивается как следствие двух предыдущих, тромбы подвергаются организации, фибриноид и гранулемы склерозируются.
4)Возвратно-бородавчатый характеризуется повторной дезорганизацией соединительной ткани клапанов с изменением их эндотелия, тромботическими наложениями на фоне склероза и гиалиноза митральных клапанов. В исходе эндокардита развивается склероз и
156
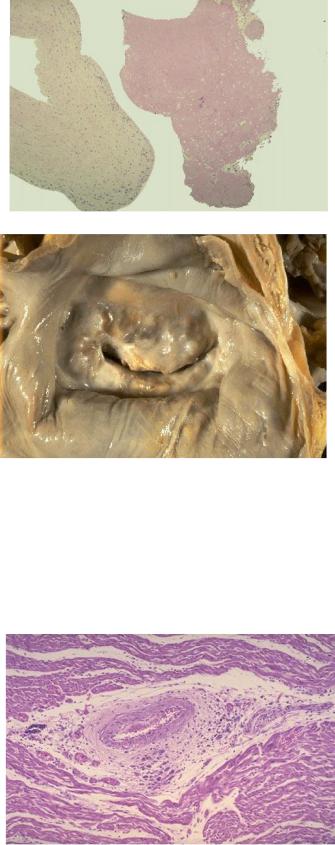
гиалиноз митрального клапана, что ведет к развитию порока сердца, чаще митрального (рис.3).
Рис. 2 острый бородавчатый эндокардит при ревматизме: слева створка митрального клапана с воспалительной инфильтрацией, справа – бесструктурные тромботические массы, которые могут стать источником тромбоэмболии.
Рис.3 Ревматический митральный порок: склероз, гиалиноз и кальциноз створок митрального клапана. Картина «рыбьей пасти».
Миокардит постоянно наблюдается при ревматизме. Выделяют три формы:
1) Узелковый продуктивный (гранулематозный). Характеризуется образованием периваскулярной ткани миокарда гранулем (рис.4). В исходе развивается периваскулярный склероз, который впоследствии может привести к кардиосклерозу.
Рис.4 Узелковый продуктивный миокардит при ревматизме: в периваскулярной ткани миокарда Ашофф-Талалаевские гранулемы – скопление крупных макрофагов вокруг очагов фибриноидного некроза.
157
2)Диффузный межуточный экссудативный чаще встречается в детском возрасте и описан Скворцовым. При нем имеется выраженный отек и полнокровие межуточной ткани миокарда с инфильтрацией лимфоцитами, гистиоцитами, нейтрофилами и эозинофилами. Развиваются дистрофические изменения миокардиоцитов. Сердце становится очень дряблым, полости его расширяются, больные умирают от сердечной недостаточности. При выздоравливании остается диффузный кардиосклероз.
3)Очаговый межуточный миокардит наблюдается при латентном течении ревматизма. При нем развивается незначительная очаговая инфильтрация стромы миокарда лимфоцитами, гистиоцитами и нейтрофилами.
Перикардит при ревматизме бывает серозным, серозно-фибринозным
ифибринозным (рис.5). Последний может закончиться образованием спаек и даже облитерацией полости сердечной сорочки.
Церебральная форма ревматизма или малая хорея клинически проявляется гиперкинезами, чаще болеют девочки школьного возраста.
Она связана с ревматическими васкулитами сосудов головного мозга, которые обнаруживаются в полосатом теле, мозжечке, субталамических ядрах.
Нодозная форма встречается редко, характеризуется появлением ревматических узелков в коже, периартикулярной ткани, в области апоневрозов. Диаметр их от 1-2 мм до 1 см, это крупные очаги фибриноидного некроза.
Осложнения ревматизма связаны с поражением сердца. В исходе эндокардита как правило развивается порок сердца, чаще митральный и в дальнейшем рано или поздно, в зависимости от характера проводимого лечения, образа жизни, наступает декомпенсация этого порока. Во время ревматической атаки за счет возвратно-бородавчатого эндокардита возможны тромбоэмболические осложнения в виде инфарктов в сосудах большого круга кровообращения (рис.6).
Представим себе типичного больного ревматизмом. Чаще это будет молодая женщина в возрасте 20-30 лет, в анамнезе ревматизм в виде суставных болей с 12 лет. При внешнем осмотре акроцианоз, отеки нижних конечностей, асцит, печень увеличена выступает из-под края реберной дуги, грубый систолический шум на верхушке, в анализах крови при поступлении ускоренное СОЭ, гиперглобулинэмия, в анализах мочи эпизодически эритроциты, на ЭКГ нарушения ритма. Поступила по поводу болей в суставах, в сердце, субфебрильная температура. Во время пребывания в клинике внезапно появились резкие головные боли, развилась левосторонняя гемиплегия, т.е. потеря чувствительности и движений одной половины тела. Напишем клинический диагноз, представим патологоанатомические изменения.

158
Рис. 6
Рис.5 Фибринозный перикардит: отрубевидные наложения фибрина на эпикарде.
Рис.6 Инфаркт почки: желтоватый треугольного вида участок, окруженный кровоизлиянием направленный основанием к капсуле.
Рис. 5
Ревматоидный артрит - хроническое ревматическое заболевание, основу которого составляет прогрессирующая дезорганизация соединительной ткани оболочек и хряща суставов, ведущая к их деформации.
Этиология и патогенез. Этиология пока невыяснена. Чаще болеют женщины, носители антигена гистосовместимости Н L А/В27 и Д/ДR4. Основное значение в тканевых повреждениях при ревматоидном артрите имеют гуморальные иммунные реакции. В сыворотке крови и в синовиальной жидкости обнаруживаются высокомолекулярные иммунные комплексы, состоящие из иммуноглобулинов и так называемых ревматоидных факторов. Ревматоидным фактором называют аутоантитела против собственных иммуноглобулинов. Этим иммунным комплексам, фиксирующим на себе комплимент принадлежит основная роль в тканевых повреждениях при ревматоидном артрите. Иммунные комплексы фагоцитируются лейкоцитами и макрофагами, что сопровождается выделением лизосомальных ферментов /кислой фосфатазы и других гидролаз в т.ч. и коллагеназы. Эти энзимы также воздействуют на мезенхимальные ткани, преимущественно суставов. Кроме гуморальных реакций при ревматоидном артрите имеет значение и реакция гиперчувствительности замедленного типа, которая развивается в синовиальной оболочке.
Патологическая анатомия. Процессы дезорганизации соединительной ткани при ревматоидном артрите развиваются в околосуставной ткани и капсуле мелких суставов кистей рук и стоп обычно симметрично.
159
Деформация наступает сначала в мелких, а затем крупных суставах (обычно коленных).
В околосуставной соединительной ткани процесс развивается классически начинает с мукоидного набухания переходя в фибриноидный некроз. Поражаются и мелкие сосуды. В ответ на некроз развиваются клеточные реакции со скоплением макрофагов и даже гигантских клеток, что приводит к развитию склероза, который опять может подвергнуться аналогичным изменениям. Эти очаги некроза возникают обычно вокруг крупных суставов размером до лесного ореха. Цикл развития близок к ревматической гранулеме (3-5 месяцев).
Дезорганизация соединительной ткани в синовиальных оболочках приводит к развитию синовита, который протекает в три стадии:
1.В этой стадии синовиальная оболочка набухает, полнокровна, хрящ
восновном сохранен. В строме ворсин мукоидные и фибриноидные изменения вплоть до некроза отдельных, которые выпадают в полость сустава, образуя т.н. рисовые тельца. В синовиальной жидкости много нейтрофилов, которые содержат ревматоидный фактор и как мы уже говорили, вызывают дополнительные повреждения ферментами активизированных лизосом. Такие нейтрофилы называют рагоцитами от слова "рагос" гроздь винограда. Эта стадия тянется несколько лет в зависимости от лечения и др. факторов.
2.Особенностью второй стадии является разрастание ворсин и разрушение хряща грануляционной тканью. Она в виде пануса /лоскута/ нарастает с краев на хрящ. Гиалиновый хрящ постепенно истончается под влиянием грануляций, расплавляется костная поверхность эпифиза обнажается.
3.В третьей стадии, которая развивается через 20-30 лет, если больной доживет, развивается фиброзно-костный анкилоз, обуславливающий неподвижность сустава.
Являясь, прежде всего болезнью суставов ревматоидный артрит может поражать и другие органы. Давно известны поражения соединительной ткани и сосудов микроциркуляторного русла, серозных оболочек, сердца, легких, почек. Однако наиболее типичным осложнением ревматоидного артрита является вторичный амилоидоз с преимущественным поражением почек. Его развитие укладывается в мутационную теорию, поскольку развивается выраженная плазматизация ряда органов, сдвиги, количественные и качественные, в составе иммуноглобулинов. В редких случаях васкулит при ревматоидном артрите протекает злокачественно, поражая сосуды мелкого и среднего калибра (артерии). Для наиболее тяжелой форма ревматоидного артериита характерны полинейропатия, некроз и изъязвления кожи, гангрена пальцев и инфаркты внутренних органов. Развитие этой болезни подобно взрыву и через несколько недель или месяцев ведет к смерти. Ревматоидный артрит у детей носит название синдрома Стилла, описан в 1897 году, и

160
характеризуется хроническим полиартритом, генерализованным увеличением л/узлов, селезенки и перикардитом, течет намного острее, чем у взрослых. У мужчин развивается болезнь Бехтерева, ревматоидный спондилит, который также сопровождается вторичным амилоидозом и заканчивается костными анкитозами суставов позвоночника.
Системная красная волчанка /болезнь Либмана Сакса/ хроническое системное заболевание соединительной ткани с выраженной аутоиммунизацией и преимущественным поражением кожи, сосудов и почек. В 90% случаев СКВ страдают молодые женщины, реже дети и пожилые женщины. Этиология системной красной волчанки неустановленна, хотя на подозрении находятся РНК - содержащие вирусы из группы парамиксовирусов.
Развитие болезни связывают с нарушением регуляции гуморального и клеточного иммунитета, снижением Т - клеточного контроля за счет поражения Т лимфоцитов предположительно вирусной природы. Установлено, что при СКВ имеет место сенсибилизация организма компонентами клеточных ядер. Гуморальные реакции связаны с наличием в плазме крови аутоантител к различным компонентам ядра и цитоплазмы к ДНК, РНК, нуклеопротеидам, к эритроцитам, лимфоцитам, тромбоцитам
(рис.7).
Рис.7 Антиядерные антитела в сыворотке крови при системной красной
волчанке, выявляемые методом иммунной флюористенции.
Появляется большое количество иммунных комплексов, которые по типу реакции гиперчувствительности немедленного типа вызывают фибриноидный некроз. Лимфомакрофагальные инфильтраты разрушающие тканевые элементы и встречающиеся во многих органах говорят о наличии клеточных реакций по типу гиперчувствительности замедленного типа. Влияние кортикостероидной терапии существенно замедляет течение этого заболевания.
Особенностью фибриноидного некроза при СКВ является присутствие в нем ядерного распада в виде обломков ядер, (гематоксилиновые тельца) поскольку, ядра красятся гематоксилином. Особенно характерным для СКВ является фагоцитоз ядерного распада и даже целых ядер лейкоцитами костного мозга. В костном мозге и крови
