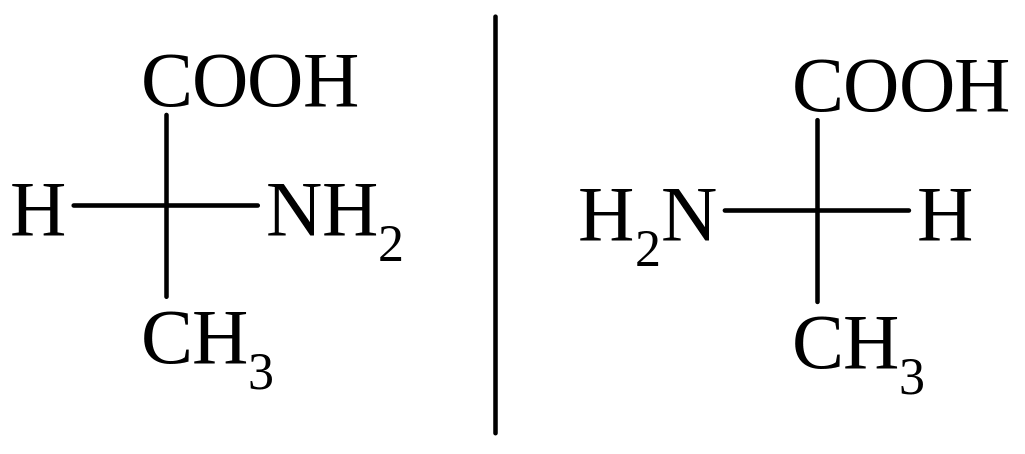- •Модуль III
- •Номенклатура Обычно ак имеют тривиальное название.
- •Изомерия
- •Классификация
- •Химические свойства
- •I. Кислотно-оснóвные
- •Отношение ак к нагреванию
- •Качественная р-ция на -ак
- •Коричневый Белки
- •Функции белков:
- •Лабораторная работа
- •Тесты для самостоятельной работы студентов Вариант 1.
- •Вариант 2.
- •Вариант 3.
- •Вариант 4.
- •Вариант 5.
Модуль III
Тема занятия: “Биологически важные аминокислоты. Белки”
Цель занятия: изучить строение и химические свойства биологически важных аминокислот, белков и их роль в организме.
Студент должен знать:
- строение, прототропную таутомерию, классификацию α-аминокислот;
- строение, структуру и свойства пептидов;
- строение, свойства, структуру белков и их водных растворов.
Студент должен уметь:
- классифицировать аминокислоты,
- объяснить амфотерность аминокислот, их химическое поведение.
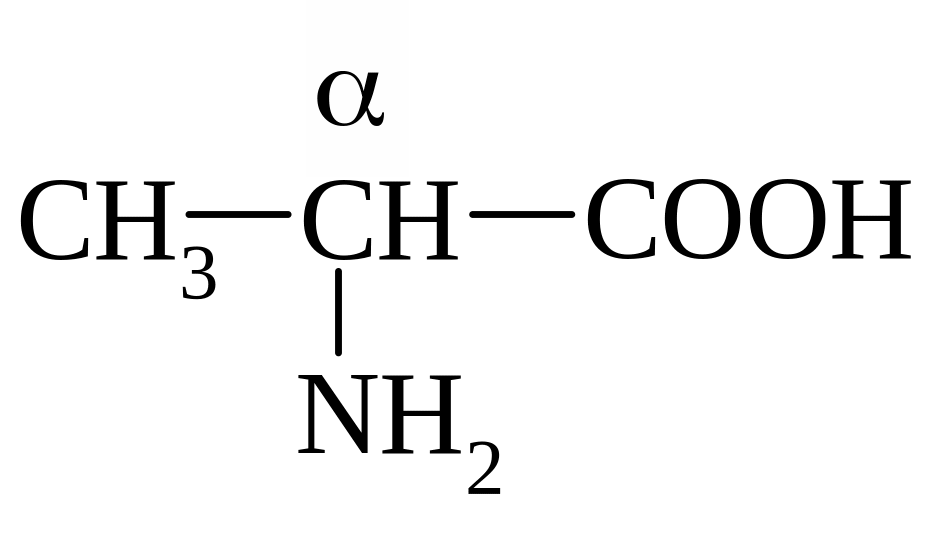
Аминокислоты (АК) - это гетерофункциональные соединения, содержащие амино- и карбоксильную группы:
![]()
Номенклатура Обычно ак имеют тривиальное название.
По рациональной номенклатуре их названия составляются путем прибавления к тривиальному названию приставки амино- и буквы греческого алфавита, указывающей положения – NH2 группы по отношению к – СООН.
МН в названии АК используется редко.
Изомерия
Изомерия цепи:
Лейцин, a-аминоизокапроновая к-та, a-амино-g-метилвалериановая к-та |
Изолейцин, a-амино-b-метил- валериановая к-та |
2. Изомерия положения гр. – NH2:
a-Аланин |
b-Аланин |
3. Оптическая изометрия (обладают все АК, кроме глицина). Отнесение к D- и L-ряду проводят по аналогии с глицериновым альдегидом по расположению Н и –NH2 гр.
Во всех случаях, когда a-АК содержит два и более асимметрических атомов углерода, конфигурацию ее определяют, исходя из a-углеродного атома.
D- L- Аланин |
D-Треонин Алло-L-треонин |
В организме обычно имеются L-, a- и алло-формы. В составе белков АК находятся только в L-форме. D-АК встречаются в антибиотиках (грамицидин).
Классификация
По числу –NH2, –COOH групп, а также в зависимости от R- АК подразделяют на: моноаминокарбоновые, моноаминодикарбоновые, диаминокарбоновые, ароматические и гетероциклические.
Аланин |
Лизин, a,e-диаминокапроновая к-та |
a-Аминоглутаровая к-та, Глутаминовая к-та |
Тирозин, n-оксифенилаланин |
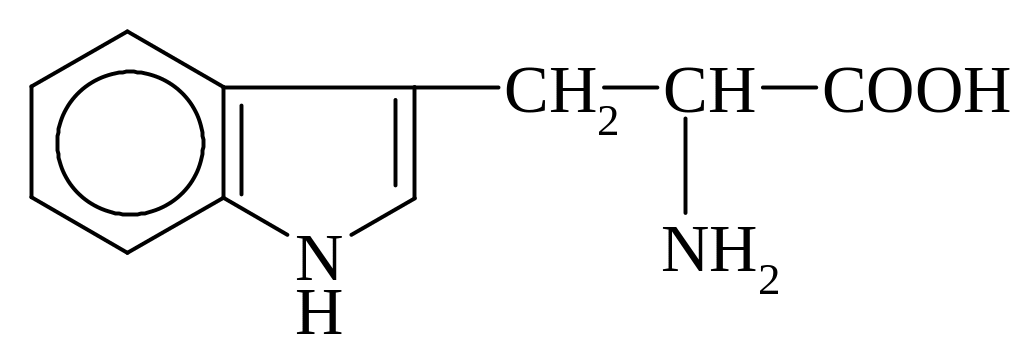
Триптофан,
b-индолилаланин,
3-индолил-2-аминопропановая к-та
Кроме вышесказанного выделяют также окси- и серусодержащие АК:
-

Серин
a-амино-b-оксипропионовая к-та

Цистеин,
a-амино-b-тиопропионовая к-та
Живые организмы различаются по своей способности синтезировать АК. АК, не синтезируемые в организме, наз-ся незаменимыми. Это гетероциклические и разветвленные АК.
Химические свойства
I. Кислотно-оснóвные
АК за счет –I группы –NH2 являются более сильными к-тами, чем соответствующие им карбоновые к-ты и более слабыми основаниями, чем амины.
a-АК являются амфотерными соединениями, т.к. содержат в одной молекуле –NH2 гр., обусловливающую оснóвные св-ва и –СOOH – кислотные. Поэтому в зависимости от среды АК могут существовать в р-ре в виде катионов, анионов или диполярных ионов:

Значение рН р-ра, при котором АК имеет равное количество положительных и отрицательных зарядов, наз-ся изоэлектрической точкой (ИЭТ). Заряд белковой молекулы определяется суммой ионогенных групп –NH3+ и –COO–.
АК, как амфотерные соединения, образуют соли как с к-тами, так и с основаниями:

Р-ции по –СООН группе
АК могут диссоциировать, образовывать соли, сложные эфиры, ангидриды, амиды, хлорангидриды.

Эта р-ция используется как “защитная” в синтезе белков и пептидов.
Р-ции по –NH2 группе
а) Р-ция солеобразования (см.выше)
б) Р-ция с HNO2
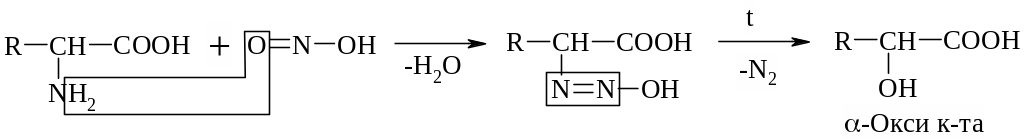
Эта р-ция дезаминирования in vitro. По количеству выделившегося азота определяют кол-во АК (метод Ван-Слайка).
в) Хлорангидриды и ангидриды к-т образуют с АК ацилпроизводные (подобно аминам и мочевине):

Эта р-ция используется для “защиты” –NH2 гр. в синтезе белков и пептидов.
г) Р-ция с формальдегидом
При взаимодействии с альдегидами a-АК, подобно первичным аминам, образуют основания Шиффа. Для аналитических целей применяется р-ция a-АК с формальдегидом, останавливающаяся на стадии N-гидроксиметильного производного АК (гидроксиметильной наз-ся гр. –СН2ОН):


Последняя р-ция лежит в основе метода формольного титрования. Сами АК вследствие амфотерности не могут быть оттированы щелочью. N-гидросиметильные производные АК содержат свободную –СООН гр. и могут быть определены количественно титрованием щелочью.