
Методические руководства кафедры / Гастроэнтерология / Послеоперационные заболевания желудка (Бельтюков)
.pdfБоязнь приема пищи и резкие нарушения в процессе пищеварения и усвоения пищи приводят больных к истощению.
Изнуряющий понос.
Трудоспособность значительно снижена, больные имеют инвалидность 2 группы.
Дефицит веса до 13-15 кг.
Гипергликемический коэффициент 2,0-2,5.
Во время приступа заболевания пульс учащается на 15-20 ударов,
систолическое давление снижается на 10-15 мм рт ст.
Эвакуация бария из культи желудка совершается в течение 5-7 минут, пищевого завтрака - за 12-15 минут. Время нахождения бария в тонком кишечнике не более 2-2,5 часов.
Демпинг-синдром 4 степени также относится к тяжелой форме заболевания.
к вышеописанным проявлениям присоединяются еще дистрофические изменения внутренних органов,
значительное истощение, доходящее до кахексии,
гипопротеинемия,
безбелковые отеки,
анемия.
Больные совершенно нетрудоспособны, нередко нуждаются в постороннем уходе.
ГИПОГЛИКЕМИЧЕСКИЙ СИНДРОМ (ПОЗДНИЙ ДЕМПИНГ-СИНДРОМ)
Демпинг-синдром поздний или гипогликемический развивается через 2-3 ч после приема пищи, является продолжением раннего демпинг-синдрома. Встречается у 0,5 -30% оперированных на желудке больных.
ПАТОГЕНЕЗ: в результате ускоренного опорожнения культи желудка в тощую кишку большого количества готовых к всасыванию углеводов происходит гипергликемия, в ответ на это возникает гуморальная реакция - избыточное выделение инсулина во время ранней демпинг-реакции. Далее происходит снижение уровня сахара крови до субнормальных показателей (до 3,33-3,89 ммоль/л) с клиникой гипогликемии при одновременном повышении концентрации иммунореактивного инсулина.
КЛИНИКА
Через 1,5-3 часа после приёма пищи или физической нагрузки возникают приступы, которые сопровождаются следующими симптомами
слабость,
Усиленное потоотделение, дрожь в теле,
резкое чувство голода,
спастическая, сосущая боль в эпигастральной области,
головокружение, потемнение в глазах,
сердцебиение, снижение артериального давления, иногда брадикардия,
бледность кожных покровов, пот.
Симптомы быстро проходят после приема небольшого количества пищи, особенно углеводистой. Чтобы предотвратить выраженные проявления гипогликемического
синдрома, больные стараются чаще питаться, носят с собой сахар, печенье или хлеб и принимают их при возникновении первых признаков.
СТЕПЕНИ ТЯЖЕСТИ ГИПОГЛИКЕМИЧЕСКОГО СИНДРОМА:
1 степень: симптомы появляются через 2-2,5 часа 2-3 раза в неделю, больные могут их не замечать.
2. степень: симптомы появляются 2-3 раза в неделю, больные знают их и стараются питаться чаще. Нередко гипогликемический синдром сочетается с другими более тяжёлыми синдромами.
3 степень: признаки болезни проявляются ежедневно. Из-за приступов, заставляющих прекращать работу и лечь, больные вынуждены питаться очень часто, постоянно носить с собой сахар и хлеб.
ДИАГНОСТИКА
Диагностика основана на характерных жалобах больного, на данных наблюдения за больным в момент приступа, низком Выраженность симптомов гипогликемического синдрома различна: от эпизодически возникающей слабости, быстро проходящей, до тяжелых проявлении, наблюдающихся ежедневно. Постоянное сочетание гипогликемического синдрома с демпинг-синдромом обусловлено их патогенетической общностью, при этом ведущим страданием является демпинг-синдром, на который должны быть направлены лечебные мероприятия.
У больных с демпинг-синдромом наблюдаются нервно-психические расстройства, основными из них являются астено-невротический синдром, истероформный синдром, депрессивный синдром, ипохондрический синдром.
Гликемическая кривая после нагрузки глюкозой характеризуется быстрым крутым подъемом и таким же быстрым падением концентрации сахара в крови ниже исходного уровня.
Рентгенологическое исследование
При демпинг-синдроме отмечаются ускоренное опорожнение культи желудка и быстрое продвижение контрастного вещества по тонкой кишке, петли которой расширены, в них заметны скопления газа и жидкости. Однако сходные явления иногда наблюдаются и в случае отсутствия клинических симптомов демпинг-синдрома. Для доказательства его наличия полезна проба А. Я. Фильштинского: у больного проводят исследование желудка дважды — до подкожной инъекции 2 мл 0,2 % раствора ацеклидина и спустя 15 мин после нее. При демпинг-синдроме начальная скорость эвакуации сульфата бария возрастает в 2,3 раза, в то время как у лиц без синдрома уменьшается в 2,1 раза
ЛЕЧЕНИЕ
Консервативное лечение применяется при лёгкой и средней степени тяжести, при тяжёлой используется для подготовки к операции.
1.Диетотерапия
Начинать прием пищи с плотных (вторых) блюд, богатых белками, витаминами, минеральными солями, с нормальным содержанием жиров,
исключить легкоусвояемые углеводы( разрешен сорбит по 3-5 г 3 раза в день)
энергетическая ценность-14654 кДж;
для снижения осмолярности содержимого желудка и замедления опорожнения желудка включат пищевые волокна,
прием жидкости до или после еды,
питание дробное, малыми порциями (5-6 раз в сутки),
прием пищи лёжа или в положении на левом боку, полулежа в кресле в течение
30 мин;
2.Нормализация моторно-эвакуаторной функции верхних отделов ЖКТ:
При гастро- и дуоденостазе: сульпирид 2 мл в/м 2 раза или по 50 мг 2-3 раза во время еды, метоклопрамид 5-10 мг 3 раза и др. прокинетики;
При спастической дискинезии: дебридат 1-2 таблетки 3 раза, селективные миотропные спазмолитики (дюспаталин 200 мг 2 раза, метеоспазмил и др.), бускопан,
Имодиум по 1-2 капс. 1-2 разапрепарат замедляет пропульсивные движения, повышает тонус сфинктеров,
В резистентных случаяхсоматостатин 50-100 мкг 2 раза кожно,
3.Заместительная терапия полиферментными препаратами: креон 25 000-50 000 ЕД с едой,
4.Комплексные поливитаминные препараты.
5.Коррекция дисбиоза кишечника по общепринятым методикам,
6.При нейровегетативных нарушениях: седативные, транквилизирующие препараты: фенобарбитал 0,02-0,03 г 3 раза, бензодиазепины, настои валерианы или пустырника и т.п.,
7.Перитол 4 мг 3 раза за 30 мин до еды.
8.Анаболические стероиды: ретаболил 1 мл в/м в 7 дней или силаболин 1 мл в/м в 7 дней при отсутствии противопоказаний,
9.При тяжелом демпинге -переливания плазмозаменителей, аминокислотных смесей.
10.Терапия анемического синдрома по общепринятым методикам.
11.Лечение психопатологических синдромов по согласованию с психиатром.
12.При гипогликемии: внутривенное введение 40% раствора глюкозы, сладкий чай и т.п.
Принципы хирургического лечения следующие.
Хирургическое лечение демпинг-синдрома тяжелой и средней степени показано при неэффективности лечебного питания и комплексного медикаментозного лечения. Цель операции - устранение анатомических условий, способствовавших развитию демпинг-синдрома.
При демпинг-синдроме, возникшем после резекции желудка с гастроеюнальным анастомозом, для устранения быстрой эвакуации пищи из культи желудка в тощую кишку и улучшения переваривания пищи применяют гастроеюнодуоденопластику, обеспечивающую прохождение пищи через двенадцатиперстную кишку. При демпингсиндроме, развившемся после резекции желудка с гастродуоденальным анастомозом, также может быть выполнена гастроеюнодуоденопластика.
У больных, которым ранее была выполнена резекция желудка по поводу пептической язвы двенадцатиперстной кишки, реконструктивная гастроеюнодуоденопластика может способствовать восстановлению кислотообразующей функции слизистой оболочки культи желудка. В связи с этим для профилактики возникновения пептической язвы в тонкокишечном трансплантате реконструктивную гастроеюнодуоденопластику надо дополнить ваготомией.
Тонкокишечный трансплантат обеспечивает порционную эвакуацию содержимого желудка в двенадцатиперстную кишку. В результате гастроеюнодуоденопластики поступающая из желудка в двенадцатиперстную кишку пища смешивается с панкреатическим соком и желчью, происходит выравнивание осмолярности содержимого двенадцатиперстной кишки с осмолярностью плазмы, осуществляется гидролиз всех ингредиентов пищи в нижележащих отделах тощей кишки. Благодаря этому в тощей кишке улучшаются процессы пищеварения и всасывания продуктов гидролиза пищи, витаминов, электролитов. У больных, перенесших реконструктивную гастроеюнодуоденопластику, демпинг-реакция на прием пищи становится менее выраженной или не возникает, масса тела увеличивается.
Профилактика демпинг-синдрома заключается в тщательном анализе предоперационного состояния пациента, готовящегося к резекции желудка или ваготомии с выбором наиболее оптимального для данного пациента вида вмешательства. При этом больному проводится математический анализ кардиоритма в сочетании с пробой Фишера при помощи тетраполярной реографии; определение содержания в крови биологически активных (серотонина, гистамина, 11-оксикетостероидов) веществ на фоне пробы Фишера; с помощью интестиноскопа - биопсия слизистой тощей кишки (на протяжении 40 см от связки Трейца) с определением в ней концентрации Ес-клеток, индекса их насыщения и грануляционного индекса. Эти исследования позволяют выявить врождённую демпинг-предрасположенность, прогнозировать тяжесть ДС в после операционном периоде. Оптимальный способ операции у лиц с высокой опасностью развития ДС - резекция желудка по Бильрот-I или резекция желудка и 40 см гормональноактивной части тощей кишки с формированием гастроэнтероанастомоза по Ру и созданием условий для замедления пассажа пищи по то щей кишке (спиралевидный клапан-инвагинат, реверсионная вставка тощей кишки и др.).
Важным этапом профилактики является грамотная реабилитация больных.
Этапы реабилитации больных, перенесших операции на желудке
1 этап. В период предоперационной подготовки больным ЯБ проводят адекватную противоязвенную терапию, в том числе эрадикационную.
2 этап. В раннем послеоперационном периоде на 2 дня назначают голод, проводят аспирацию желудочного содержимого через зонд с последующим введением через зонд смесей для энтерального питания.
С 2-4-го дня при отсутвтии признаков гастро- и дуоденостаза больному назначают специальную диету, содержащую белковый энпит.
Если к концу 1-й недели сохраняется повышенная кислотообразующая функция культи желудка, то назначают антисекреторные препараты (ИПП, Н2-блокаторы или антациды).
3 этап. Начинается со 2-й недели после операции и продолжается 2-4 мес. Проводится комплексная терапия, цель которой - способствовать уменьшению воспалительных реакций, активизировать репаративные процессы, предупредить формирование демпинговых реакций и т.п.
Назначается диета с высоким содержанием белка (140г), нормальным содержанием жиров (110-115 г) и углеводов (380г), ограничением механических и химических раздражителей слизистой оболочки и рецепторного аппарата ЖКТ.
Исключаются: тугоплавкие жиры, легкоусвояемые углеводы, молоко.
Режим питания дробный.
Для нормализации моторики назначают: прокинетики, имодиум при диарее, дюспаталин.
Если признаки болезни оперированного желудка отсутствуют, данные профилактические мероприятия рекомендуют соблюдать в течение 2-5 лет после операции. Прежде всего это касается правил диетотеапии.
СИНДРОМ ПРИВОДЯЩЕЙ ПЕТЛИ
Хронический синдром приводящей петли развивается после резекции желудка с наложением гастроеюнального анастомоза в случае стеноза приводящей или отводящей петли.
Синдром приводящей петли (СПП) встречается в 3,5-42% после резекции желудка по Бильрот-II или ваготомии с формированием гастроэнтероанастомоза. Частота синдрома приводящей петли достигает в среднем 13%.
Патогенез. Возникают нарушения эвакуации дуоденального содержимого и попадания части пищевого химуса не в приводящую, а отводящую петлю тощей кишки. Причинами ее могут быть как механические, так и функциональные нарушения проходимости кишечника.
К механическим факторам относятся:
1)слишком длинная приводящая петля без брауновского соустья;
2)слишком короткая приводящая петля, которая в результате дополнительного фиксирования к малой кривизне может создать перегиб кишки;
3)горизонтальное расположение линий желудочно-кишечного анастомоза, благодаря чему часть пищи поступает в приводящую петлю, а далее в 12-перстную кишку, вызывая в ней дуоденостаз; так как сила сокращений культи желудка больше, чем 12-перстной кишки, то поступившая пища может задержаться там более или менее длительно;
4)выпадение слизистой приводящей петли в желудок или в отводящую петлю;
5)ротация приводящей петли вокруг своей продольной оси;
6)рубцы, спайки, опухоли или язвенный стеноз приводящей или отводящей петель;
7)антиперистальтическое расположение кишки для анастомоза;
Функциональный синдром приводящей петли может быть вызван:
1)дискинезией приводящей и отводящей петель или сфинктеров 12-перстной кишки, сфинктера Одди и желчного пузыря;
2)нарушением нервной регуляции 12-перстной и тощей кишки в результате перерезки нервных ветвей во время операции;
3)имевшимся дооперационным дуоденостазом;
Поступление из культи желудка необработанной пищи в верхний отдел тощей кишки является основой для развития демпинг-синдрома.
Потери дуоденального содержимого в результате рвоты, асинхронизм между поступлением в отводящую петлю пищи и пищеварительных соков из двенадцатиперстной кишки, сочетание синдрома приводящей петли с демпинг-синдромом и панкреатической недостаточностью способствуют развитию синдромов расстройств питания, нарушению водно-электролитного обмена и кислотно-щелочного состояния.
КЛИНИКА
По тяжести клинической картины можно выделить 4 степени заболевания.
К 1-й степени синдрома относят больных, у которых есть легкие расстройства типа срыгиваний, рвоты желчью 1-2 раза в месяц, чаще связанные с приемом молока. Диспептические нарушения и болевые ощущения почти не беспокоят больных, общее состояние удовлетворительное, трудоспособность не нарушена.
2-я степень синдрома характеризуется средней тяжестью проявления заболевания. Рвота с желчью возникает 2-3 раза в неделю, количество рвотных масс достигает 200-300 мл. Возникновению рвоты предшествует появление чувства полноты в правом подреберье и эпигастрии после еды, особенно после жидкой пищи и молока. Рвота приносит облегчение. У этой категории больных имеет место снижение трудоспособности, потеря в весе.
К 3-й степени синдрома относятся случаи, когда рвота возникает почти ежедневно, объем рвотных масс достигает 400-500 мл и более. После еды возникают распирающие боли в правом подреберье и подложечной области. Для облегчения состояния больные самостоятельно вызывают рвоту. Характерно истощение, значительное снижение трудоспособности.
4-я степень заболевания характеризуется, кроме вышеуказанных признаков, резкими расстройствами питания и обмена веществ (безбелковые отеки, резкое истощение, гипопротеинемия, малокровие), а также значительными дистрофическими изменения со стороны паренхиматозных органов.

Диагностика
Рентгенологическое исследование
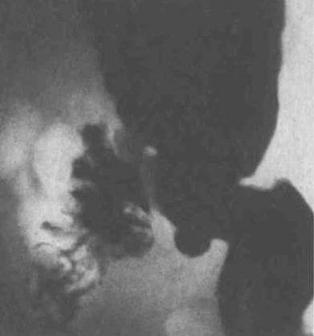
Поступление контрастного вещества в приводящую петлю само по себе не является патологией. Признаками синдрома приводящей петли служат ее расширение, отечность слизистой оболочки, задержка в петле содержимого, болезненность при пальпации (рис.2). Эти признаки могут быть связаны с избыточной длиной петли и неправильным расположением анастомоза, но могут возникнуть и в результате рубцового сужения кишки у анастомоза. В этом случае иногда для заполнения приводящей петли после фармакологической релаксации необходимо ввести зонд с баллоном в петлю для ее блокады. Из-за частичной непроходимости идентификация приводящей петли при приеме бария затруднена. В этих случаях бариевую взвесь вводят через канал эндоскопа при ЭГДС.
Рис.2. Рентгенограммы оперированного желудка: синдром приводящей петли - петля расширена, содержит газ и жидкость.
ЛЕЧЕНИЕ
Консервативное – малоэффективно. Для уменьшения симптомов используют следующие мероприятия:
После еды лежать на правом боку,
Повторные промывания желудка и дренирование приводящей петли через эндоскоп
Санация слепой петли от развивающегося дисбиоза_ использование «кишечных» антибиотиков и антиспетиков: интетрикс 1 др. 3 раза,сульфаниламиды (бактрим 1 т. 2-4 раза), антибиотики широкого спектра действия. Курс лечения- 7- 14 дней.
Операции делятся на три группы:
1.Устраняющие перегибы приводящей петли или укорочение:
подшивание приводящей петли к малому сальнику и заднему листку брюшины (Capper-Butler, 1951);
подшивание приводящей петли к малой кривизне желудка;
устранение перегибов петли с фиксацией швами;
укорочение при водящей петли (Hoffmann-Spiro, 1961).
2.Дренирующие операции:
энтероэнтероанастомоз по Брауну;
энтероэнтероанастомоз по Ру;
дуоденоеностомия (бок в бок или по Витебскому или Bergeret);
реимплантация двенадцатиперстной кишки и приводящей пет ли в отводящую (по Tanner-Roux);
«панталонная» пластика гастроэнтероанастомоза по Hoag-Saunders- Steinberg.
3.Реконструктивные:
дегастроэнтеростомия после ваготомии и гастро-энтеростомии, и пилоропластика;
реконструкция гастроэнтероанастомоза по Райхелю-Полиа в анастомоз по Гофмейстеру-Финстереру;
реконструкция Бильрот-I в Бильрот-П;
гастроеюнопластика.
Острый синдром приводящей петли - угрожающее жизни острое заболевание. .
Патогенез. Острая непроходимость вызвана - спайками, заворотом, внутренними грыжами, инвагинацией, ущемлением в «окне» поперечно-ободочной кишки, стенозом анастомоза, атонией двенадцатиперстной кишки после ваготомии.. Повышение давления в приводящей петле приводит к расстройству кровообращения в ее стенках, к развитию гангрены и перитониту. Вследствие застоя содержимого в приводящей петле повышается давление в желчных протоках, в протоке поджелудочной железы, и развивается острый панкреатит.
КЛИНИКА острой непроходимости приводящей петли:
Боль в эпигастрии, правом подреберье, тошнота, рвота.
Нарастает интоксикация, воспалительный синдром.
При пальпации живота в эпигастрии и правом подреберье определяется болезненность, выявляется напряжение мышц брюшной стенки.
При некрозе двенадцатиперстной кишки и перфорации возникает клиника распространённого перитонита.
При вовлечении в процесс желчного пузыря и поджелудочной железы возникают опоясывающие боли, появляются признаки желтухи и холангита.
На обзорной рентгенограмме брюшной полости выявляются затемнение, пневматоз кишечной петли.
Отмечается длительная задержка контраста при выполнении холеграфии.
Лечение: экстренная операция. Для устранения гипертензии в приводящей петле применяют еюнодуоденостомию, реконструкцию терминолатерального гастроеюнального анастомоза в У-образный анастомоз. Летальность составляет до 26%.
ПЕПТИЧЕСКАЯ ЯЗВА АНАСТОМОЗА
Возникает после формирования гастроэнтероанастомоза в 5-10% случаев, после резекции желудка - в 0,5-2% наблюдений. Подавляющее большинство язв анастомоза и тощей кишки возникают через 6-12 месяцев после операции. Пептические язвы чаще склонны к пенетрации, кровотечению, чем первичные язвы желудка и 12-перстной кишки.
ПАТОГЕНЕЗ
Сроки появления пептических язв гастроэнтероанастомоза после резекции желудка, с наложением гастродуоденального анастомоза или гастроэнтероанастомоза на короткой петле, почти одинаковые. Клинические проявления, свидетельствующие о пептических язвах гастроэнтероанастомоза, возможны уже в первые месяцы после резекции желудка м, через 1,5 мес, часто – в первые 6–18 мес после операции и значительно позже(через 1-8 лет). Причиной появления пептической язвы после резекции желудка является наличие свободной соляной кислоты в желудочном соке, которая становится патогенетическим фактором в развитии язвы на соустье или анастомозированной петле. Источником соляной кислоты могут быть:
оставленные в результате экономной резекции желудочные железы тела и дна, продуцирующие соляную кислоту и пепсин,
технически неправильно выполненная операция, когда оставляется пилорический отдел желудка вместе со слизистой оболочкой, которая выделяет гормон гастрин, являющийся сильным возбудителем кислотопродуцирующих желудочных желез,
синдром Золлингера-Эллисона, для которого характерна триада: пептическая язва после резекции желудка (даже субтотальной), высокая желудочная секреция, наличие опухоли поджелудочной железы из островковой ткани. Гастрэктомия является на сегодняшний день операцией выбора при синдроме ЗоллингераЭллисона, т.к. оставление даже небольшого участка желудка приводит к рецидиву пептической язвы,
резекция желудка, при которой накладывается брауновское соустье или анастомоз по Ру. При обеих этих модификациях щелочное содержимое 12-перстной кишки не орошает желудочно-кишечное соустье, а переходит по межкишечному соустью в отводящую петлю.
КЛИНИКА
Ведущий симптомболь в эпигастральной области, чаще – левее срединной линии, реже – в области послеоперационного рубца или в пупочной области. Иррадиация болей возможна в левые подреберье и лопатку верхней половине живота. Боль постоянная, усиливается вскоре после приема пищи, не облегчается при приеме антацидов или молока,
тошнота, рвота, изжога.
понос или запор.
похудание.
В связи с пенетрацией язвы боль по интенсивности значительно превосходит боль, возникавшую у больного до операции при пенетрации (71% больных), возникает симптоматика со стороны других органов.
При гастродуоденальном кровотечении (2/3 больных): гематемезис, мелена, анемия.
Возможно развитие других осложнений: перитонит в результате перфорации, желудочно-ободочный свищ.
При исследовании желудочной секреции находят сохранение кислотопродуцирующей функции оперированного желудка.
Рентгенологический симптом рецидива язвы - ниша, которую, однако, бывает трудно выявить из-за рубцовой деформации оперированных органов.
Наиболее информативным методом диагностики рецидива язвы является эндоскопическое исследование.
ДИАГНОСТИКА
Эндоскопическое исследование
Размеры пептических язв гастроэнтероанастомоза достигают 3–5 см и более (нередко с неоднократными кровотечениями в анамнезе)
Рентгенологическое исследование
Нарушение функции анастомоза отмечается при пептической язве. Она чаще всего образуется через 1 — 2 года после оперативного вмешательства и располагается в самом анастомозе либо прилежащем отделе отводящей или приводящей кишки. Язва выявляется в виде контурной или рельефной ниши, окруженной воспалительным валом (рис.3), болезненна при пальпации, нередко сопровождается сужением просвета кишки и спазмом анастомоза с расстройством эвакуаторной функции культи. Прободение такой язвы может привести к образованию внутреннего свища (чаще желудочно-ободочного), который обнаруживают по затеканию в него контрастного вещества
Рис.3. Рентгенограммы оперированного желудка: пептическая язва анастомоза после резекции желудка по Бильрот 2.
При хирургическом лечении постгастрорезекционных синдромов широко применяют реконструктивную гастроеюнодуодено-пластику, или редуоденизацию. Создаваемый при этой операции тонкокишечный трансплантат играет роль резервуара и выполняет функцию привратника. При рентгенологическом исследовании
