

Общая схема реакции азосочетания и ее механизм (SEAr)
N≡N + H |
Y |
H |
Y |
||
X |
N |
N |
|
|
|
диазокомпонента (E+) |
азокомпонента |
|
X=акцептор (-SO3H, |
Y= -NH2,-NHR,-NRR, |
|
-NO2,-COOH) |
-OH (R=алкил) |
|
- H+ |
N N |
Y |
|
X |
|
|
азосоединение |
|
Реакция протекает с образованием только продукта пара-замещения из-за большого объема электрофила.
В зависимости от природы заместителя (Y) в азокомпоненте азосочетание проводят в слабощелочной (Y=-OH) или слабокислой среде (Y= -NH2,-NHR,- NRR).
Азосочетание с фенолами (нафтолами) проводят при рН 9-10, при этом фенолы и нафтолы превращаются в алкоголяты и азосочетание проходит более эффективно.
Получение нафтолоранжа
SO |
NH |
NaOH |
NaNO2 |
Na O S |
NH |
||
3 |
3 |
3 |
2 |
сульфаниловая кислота |
- H2O |
HCl |
|
|
0 - 5°C |
||
|
(цвиттер-ион) |
|
O Na |
|
|
|
|
|
SO3H |
N≡N Cl |
|
|
|
pH 9 - 10 |
|
250

N=N |
SO3Na |
|
O Na |
Сульфаниловая кислота имеет цвиттер-ионное строение, поэтому ее сначала превращают в соль, а затем диазотируют и получают диазокомпоненту реакции. В качестве азокомпоненты используют β-нафтол, после азосочетания получают – нафтолоранж (аморфное вещество ярко-оранжевого цвета). Продукты азосочетания ярко окрашены (следствие образования сопряженной системы связей). Чем более щелочная среда, тем глубже окраска нафтолов (переход от оранжевого цвета в красный).
Азосочетание с анилинами
При рН 5-6 анилины, которые плохо растворимы в воде, протонируюся и их растворимость улучшается, это обуславливает успешное протекание реакции азосочетания. Поскольку среда слабокислая, в растворе имеется достаточно анилина для образования σ-комплекса.
Получение метилоранжа (гелиантина)
N(CH3)2
Na SO3 |
NH2 |
NaNO2 |
SO3H |
N≡N |
|
HCl |
|||||
|
|
|
pH 5-6 |
||
|
|
0 - 5°C |
|
|
SO3H
 N
N N
N
 N(CH3)2
N(CH3)2
В синтезе гелиантина в качестве азокомпоненты используют N,N- диметиланилин. Гелиантин (кристаллическое вещество оранжевого цвета) является индикатором, при подкислении оранжевая окраска раствора становится красной.
По теория цветности молекулы, содержащие хромофоры (обуславливают цвет) и ауксохромы (обуславливают глубину оттенка), а также сопряженные системы двойных связей, являются окрашенными.
Хромофоры - -N=O, -N=N, -C=O , -CH=CH2 |
||
|
|
H |
Ауксохромы |
-N(CH3)2, |
-OH, -NHR, -NH2 |
|
||
251

АРОМАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
Арены, в которых карбонильная группа непосредственно связана с ароматическим ядром, относятся к ароматическим альдегидам и кетонам. Они имеют приятные запахи и входят в состав эфирных масел растений. Бензальдегид имеет запах горького миндаля. Ацетофенон входит в состав эфирных масел черемухи и имеет выраженный запах черемухи, обладает снотворным действием. Ванилин и вератровый альдегид входят в состав запаха бобов ванили.
Номенклатура
O |
O |
O |
|
C |
|||
C H |
C CH3 |
||
|
|||
бензальдегид |
ацетилбензол, |
дифенилкетон, |
|
|
ацетофенон |
бензофенон |
|
|
O |
O |
|
C |
C |
||
H |
H |
||
|
|||
|
|
||
HO |
CH3O |
OCH3 |
|
OCH3 |
|
3-метокси-4-оксибензальдегид, |
3,4-диметоксибензальдегид, |
|
вератровый альдегид |
||
ванилин |
||
|
Методы получения
1. Формилирование (введение карбонильной группы)
а) реакция Гаттермана-Коха
|
|
|
|
|
|
CO/HCl |
|
|
|
|
|
O |
|
||
|
|
|
|
|
|
|
|
|
|
|
C |
SEAr |
|||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
AlCl3 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
бензальдегид |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
генерация Е+: |
|
|
O |
|
|
|
|
||||||||
CO + HCl |
|
|
|
H-C |
|
|
AlCl3 |
H-C=O AlCl4 |
|||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|||||||||
Cl формил-катион
252

б) Реакция Гаттермана
CH3 |
|
|
|
|
|
CH3 |
CH3 |
|||||||
|
1) HCN/HCl |
|
|
|
|
|
|
|
+ |
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
AlCl3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
2) H2O/H+ |
|
|
|
|
CHO |
|
|
||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
п-метилбензальдегид |
о-метилбензальдегид |
|||||||||||
SEAr |
|
HCl |
|
|
|
|
|
|
AlCl3 |
|||||
генерация Е+: |
H-C≡N |
|
|
|
|
|
|
|||||||
H-C NH |
|
H-C=NH AlCl4 |
||||||||||||
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
Cl |
|
иминий-катион |
||
2.Ацилирование по Фриделю-Крафтсу (см. Электрофильное замещение для бензола).
3.Окисление толуола
CH3 |
C O |
SeO2 |
|
|
H |
Реакционная способность
|
-δ |
+δ O-δ |
+δ |
O |
|
C |
C |
|
|
H |
CH3 |
-I, -M |
|
-I, -M |
Реакции идут по карбонильной группе и ароматическому ядру.
I. Реакции по карбонильной группе
Карбонильная активность ароматических альдегидов и кетонов снижена вследствие донорного влияния ароматического ядра.
253

Для бензальдегида
Бензальдегид не дает циангидрина с HCN (идет бензоиновая конденсация, в данном курсе не описывается). Циангидрин можно получить через бисульфитное производное. Остальные реакции, в основном, аналогичны реакциям алифатических альдегидов.
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
NaHSO |
|
|
|
|
|
|
|
OH |
|
H-C≡N |
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C-C≡N |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
H |
3 |
|
|
|
|
|
|
|
C-SO3Na |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
-NaHSO3 |
|
|
|
|
H |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5-NH2 |
бисульфитное |
|
|
циангидрин, нитрил |
||||||||||||||||
NH2-X |
|
|
-H2O |
|
производное |
|
|
оксифенилуксусной |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислоты |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
N-C6H5 |
+ |
H2O |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
C |
|
|
N-X |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
основание Шиффа, |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
азометин |
|
|
|
|
|
|
|
|
оксим, |
|
|
X= OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
гидразон, X= NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
фенилгидразон, X= NHC6H5 бензальдегида
|
|
|
|
|
|
C |
O |
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
NaOH |
|
|
|
|
|
|
|
C |
реакция Канниццаро |
||||
|
|
|
|
|
|
|
|
|
||||||||||||||
2 |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
+ |
|
|
|
ONa |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
бензиловый спирт |
|
бензоат натрия |
|
||||||
|
|
|
|
|
|
O |
|
Ag(NH3)2OH |
|
|
|
|
O |
|
|
|
|
|
||||
|
|
|
|
|
C H |
|
|
|
|
|
C OH |
+ Ag |
|
|||||||||
|
|
|
|
|
|
|
или Cu+2 |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
или Cu2O |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
(реактив Фелинга), |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
или О2 воздуха, 200С |
|
бензойная кислота |
|
|||||||||||||
Для ацетофенона
Отсутствуют реакции с HCN и NaHSO3, остальные реакции аналогичны описанным для кетонов.
254

|
|
|
|
|
C |
O |
|
|
|
Cl2 |
|
|
|
|
|
|
|
C |
O NH2-X |
|
|
|
N-X |
||||||||
|
|
|
|
|
CH2Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
CH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
-HCI |
|
|
|
|
|
|
|
|
|
|
|
-H2O |
|
|
3 |
||||||
|
|
|
|
|
|
|
|
|
|
3I2 |
|
|
|
|
|
|
|
|
|
||||||||||||
1-хлор-2-фенилэтанон, |
NaOH |
|
|
|
|
|
|
X= OH, оксим |
|||||||||||||||||||||||
хлористый фенацил |
|
|
|
|
|
|
|
|
|
|
|
|
C O |
|
|
|
|
|
|
X= NH2, гидразон |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ HCI3 |
X= NHC6H5, фенилгидразон |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ONa |
ацетофенона |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
бензоат натрия |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
галоформное расщепление |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O-C |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
CH |
(CH3CO)2O |
|
|
|
C CHCH3 |
||||||||
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
CH2-H |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
- CH COOH |
|
|
|
2 |
|||||||
|
|
|
|
|
|
|
|
|
|
доля енольной формы |
3 |
|
|
1-фенилвинилацетат |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
достаточно велика |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
Cl-C OCH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
||||||||
|
|
|
метиловый эфир |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O-C OCH3 |
|
|
|
|
|
|
|
|
|||||||
|
|
|
хлоругольной кислоты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C CH |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
метил 1-фенилвинилкарбонат |
|
|
|
|
||||||||||||||||
O |
O |
|
O |
OH |
C CH2-H + |
C |
|
C-CH-CH |
|
H |
Al2O3 |
|||
CH3O |
|
|
- H2O |
|
|
|
|
H |
|
кротоновая конденсация |
|
|
|
|
O |
|
|
|
OCH3 |
C CH=CH |
OCH |
|
|
|
|
|
3 |
|
|
1-фенил-3-(п-метоксифенил)пропенон, халкон (α,β− непредельный ароматический альдегид)
255

II. Реакции электрофильного замещения
Формильная и ацетильная группы являются электроноакцепторными, поэтому новый заместитель будет направляться преимущественно в мета- положение.
Для бензальдегида
Чтобы избежать окисление бензальдегида, при его нитровании вместо концентрированной HNO3 используют ее соль. Бромирование идет в присутствии железа. Сульфирование, алкилирование и ацилирование не приводит к удовлетворительным результатам и не является препаративным синтезом.
|
|
|
|
C |
O |
KNO3 |
|
|
O |
Br2 |
|
|
|
C |
O |
|||
|
|
|
|
|
|
C |
|
|
|
|
||||||||
H2O + |
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
H + HBr |
|
|
|
|
H2SO4 |
|
|
Fe |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
0oC |
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
Br |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
м-нитробензальдегид |
|
|
|
|
|
|
м-бромбензальдегид |
|||||||||||
Для ацетофенона
Ацетофенон в отличие от бензальдегида более стабилен по отношению к окислителям, нитруется и сульфируется аналогично замещенным аренам. Бромирование ацетофенона проводят в два этапа, что позволяет избежать реакции по метильной группе.
|
|
|
|
|
|
O |
|
|
|
|
|
O |
олеум |
|
|
|
|
|
|
|
|
|
|
O |
|||||
|
|
|
|
|
|
|
|
|
|
|
C CH |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
C |
HNO3 |
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
+ H2O |
|||||||
H |
O + |
|
|
|
|
CH3 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||
2 |
|
|
|
|
|
H2SO4 |
|
|
|
|
|
|
t0C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
0oC |
|
|
|
|
|
|
|
|
|
|
|
|
|
SO3H |
|
|
|
|||||
|
|
|
NO2 |
|
|
|
AlCl3 |
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
м-нитроацетофенон |
|
|
|
|
|
|
м-ацетилбензолсульфокислота |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
O ....AlCl3 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1) Br2 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C CH |
|
|
|
|
|
|
|
C CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
2) H3O |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- HBr, |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-Al(OH)3, |
|
|
|
||||||||
-HCl м-бромацетофенон
256

Многие из альдегидов и кетонов обладают приятными запахами, входят в состав эфирных масел растений и используются в составлении парфюмерных композиций.
O
C
H
бензальдегид(маслянистая жидкость), запах горького миндаля
O
C CH3 ацетофенон (маслянистая жидкость), запах черемухи, снотворное действие
|
|
|
|
|
C |
O |
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
3 |
п-метилацетофенон (маслянистая жидкость), запах мимозы |
CH3 |
|
|
|||||
|
|
|
|
|
C |
O |
|
|
|
|
|
|
|
CH3 п-метоксиацетофенон (маслянистая жидкость), запах цветов |
|
|
|
|
|
|
|
||
CH3O |
|
гелиотропа |
|||||
|
|
||||||
БЕНЗОЙНЫЕ КИСЛОТЫ
К бензойным кислотам относятся арены, в которых карбоксильная группа связана с ароматическим ядром.
Номенклатура
Одноосновные кислоты
|
|
|
C O |
|
|
|
C O |
|
|
|
OH |
|
|
|
OH |
|
|
|
|
X |
|||
бензойная кислота |
Х =донорные и акцепторные группы, |
||||||
|
|
|
|
||||
|
|
|
|
расположенные в о-, м-, п-положениях |
|||
257

Двухосновные кислоты
|
|
|
COOH |
|
|
|
COOH |
|
COOH |
|||
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
COOH |
|||
|
|
|
|
|
|
|
|
|
|
|||
1,2-бензолдикарбоновая |
1,3-бензолдикарбоновая |
|
1,4-бензолдикарбоновая |
|||||||||
кислота, |
кислота, изофталевая |
|
кислота, терефталевая |
|||||||||
фталевая кислота |
кислота |
|
кислота |
|||||||||
Методы получения
CH3 |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|||||||||
|
|
O2, воздух |
|
|
|
|
|
|
C |
+ H2O |
|
|
|
|
|||||||||||
|
|
|
|
t0C |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
бензойная кислота |
|
|
|
|
||||||||||||||
CH3 |
|
|
|
|
|
|
|
O |
O |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
C |
|
|
COOH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
CH3 O2, воздух |
|
|
|
|
C O H3O |
|
|
|
COOH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
V2O5, 4500C |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
-2H2O |
|
|
|
|
фталевый ангидрид |
фталевый кислота |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
CH3 |
|
|
|
|
COOH |
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
O2, воздух |
|
|
|
|
|
|
+ |
2H2O |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
Co+2, t0C |
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
CH3 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
терефталевая кислота |
|
|
|
|
|||||||||||||
258

Реакционная способность
-δ
-δ +δC O OH
+δC O OH
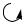 -δ
-δ
Для бензойных кислот характерны реакции по карбоксильной группе и ароматическому ядру.
I. Реакции по карбоксильной группе
Бензойная кислота по своей силе находится между муравьиной и уксусной кислотой (рКа 43,26). ОН-Кислотность замещенных бензойных кислот зависит от природы и расположения заместителя в ароматическом ядре, как правило доноры электоронов приводят к ослаблению кислотности, акцепторы усиливают кислотность.
Бензойные кислоты образуют соли, хлорангидриды, амиды, сложные эфиры по обычным схемам. Особенностью хлорангидрида бензойной кислоты (хлористого бензоила) является его устойчивость к гидролизу, на этом основана реакция бензоилирования по Шоттен-Бауму в присутствии водного раствора щелочи.
|
O |
OH |
O |
|
C Cl |
C |
|
|
OC6H5 |
||
|
|
NaOH |
|
|
|
- NaCl |
|
-NaCl |
,NaOH |
фенил бензоат |
|
N |
|
|
|
|
H |
пиперидин |
|
N
COC6H5
N-бензоилпиперидин
259
