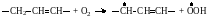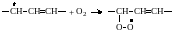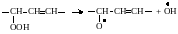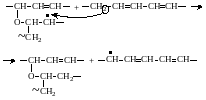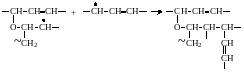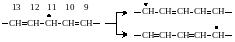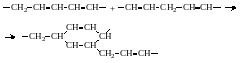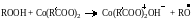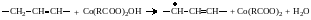- •Введение
- •2. Пленкообразование, осуществляемое
- •2.2.1. Формирование покрытий из водных дисперсий
- •2.2.2. Формирование покрытий из органодисперсий полимеров
- •Пленкообразование из органодисперсий
- •2.3. Формирование покрытий из порошковых
- •3. Пленкообразование, осуществляемое
- •3.1.2. Отверждение олигоэфирмалеинатов
- •3.2. Пленкообразование фенол-, карбамидо- и меламино-
- •3.2.2. Карбамидо- и меламиноформальдегидные олигомеры
- •4. Классификация полимерныхпокрытий
- •5. Свойства полимерных покрытий и
- •5.1. Реологические свойства лакокрасочных систем
- •Методы определения вязкости
- •Прямые методы:
- •5.2.2. Укрывистость
- •Методы определения укрывистости
- •5.2.4. Растекаемость (разлив)
- •5.2.5. Жизнеспособность лакокрасочных материалов
- •5.2.6. Толщина покрытий
- •5.2.7. Степень отверждения покрытий
- •Методы определения степени отверждения покрытий
- •1) Метод стеклянных шариков
- •5.3.1. Химический метод
- •5.4.2. Вторая группа свойств
- •Метод определения эластичности пленки при изгибе
- •Методы определения адгезионной прочности покрытий
- •Метод решетчатых надрезов
- •5.7. Антикоррозионные свойства покрытий
- •Категория коррозивности атмосферы
- •5.7.3. Водо - и влагостойкость покрытий
- •5.7.4. Определение химической стойкости покрытий
- •5.8. Атмосферостойкость лкп
- •Оглавление
3. Пленкообразование, осуществляемое
В РЕЗУЛЬТАТЕ ХИМИЧЕСКИХ ПРЕВРАЩЕНИЙ
Этот вид пленкообразования предусматривает проведение химических реакций между олигомерами или олигомеров с мономерами в тонком слое на подложке. Олигомеры и мономеры при этом должны иметь реакционные центры, способные под действием тепла, облучения или отвердителей вступать в различные химические взаимодействия. На основе таких реакционных систем можно получать линейные, разветвленные или трехмерные полимеры.
Использование подобных пленкообразующих систем имеет ряд преимуществ.
В отличие от высокомолекулярных полимеров олигомеры хорошо растворяются в большинстве органических растворителей. Невысокая молекулярная масса дает возможность получать растворы с достаточно высоким содержанием олигомера от 40 до 90 % (в зависимости от молекулярной массы олигомера, а в ряде случаев и 100 %-ные пленкообразующие системы, такие как “олигомер-мономер”).
Олигомеры, содержащие в достаточном количестве гидрофильные группы (-СООH и -ОH), используются для приготовления водоразбавляемых материалов.
Твердые олигомеры с относительно высокой температурой размягчения (>70 0С) могут быть использованы также для получения термореактивных порошковых материалов.
Таким образом, олигомеры используются в пленкообразующих системах растворного типа, водоразбавляемых, а также в 100 %-ных (жидких или в виде порошка) композициях.
Наибольшее распространение в качестве пленкообразующих для получения покрытий нашли олигомеры с реакционноспособными группами или связями. Отверждение таких олигомеров может проходить за счет функциональных групп самого олигомера (самоотверждение) или за счет взаимодействия функциональных групп олигомера со специально добавленными веществами – отвердителями.
Образование полимеров может происходить за счет реакций гомо- и сополимеризации, поликонденсациии полиприсоединения.
Скорость пленкообразования зависит от молекулярной массы олигомера, его реакционной способности, удельной функциональности, присутствия ускоряющих агентов (катализаторов, инициаторов).
Продолжительность формирования покрытий во всех случаях определяется скоростью протекания химических реакций, а их свойства – степенью завершенности процесса.
Адгезионная прочность таких покрытий, как правило, высокая.
Характер процессов отверждения (перевода олигомера в сшитое, трехмерное состояние) в значительной мере обусловлен исходной структурой олигомеров. Различают три основных типа олигомеров.
1. Олигомеры разветвленной структуры с неупорядоченным расположением активных функциональных групп. Их получают из мономеров с функциональностью ƒ>2 по ступенчатым реакциям поликонденсации или полиприсоединения, не доводя реакцию до точки гелеобразования (Р<Рr). Также олигомеры содержат функциональные группы различных типов, способные реагировать между собой. Поэтому подобные олигомеры могут образовывать сетчатые структуры без дополнительного введения в реакционную систему полифункциональных отверждающих веществ (отвердителей). Можно лишь использовать катализаторы, ускоряющие те же реакции, по которым был получен олигомер. Следовательно, процесс отверждения таких олигомеров, является как бы продолжением реакции синтеза олигомера, протекающей на подложке в тонком слое после точки гелеобразования т.е. Р>Рr.
Отверждение происходит под действием тепла (термореактивные олигомеры), кислорода воздуха. Примером могут служить алкидные, карбамидо-, фенолформальдегидные (резольные) и др. олигомеры.
2. Олигомеры с активными функциональными группами, расположенными по концам полимерных линейных цепей, которые получают из бифункциональных мономеров (ƒ=2). При проведении реакции синтеза подобных олигомеров до больших степеней превращения, образующиеся полимеры продолжают оставаться линейными. Поэтому для превращения их в сетчатые, трехмерные полимеры необходимо использовать полифункциональные отвердители с ƒ≥3.
К подобным олигомерам можно отнести простые и сложные линейные полиэфиры, эпоксиды (когда активными функциональными группами являются эпоксидные).
3. Олигомеры линейного строения с активными функциональными группами, или реакционными центрами расположенными регулярно (возможно, и неупорядоченно) вдоль цепи. Такими олигомерами является поливиниловый спирт и линейные ненасыщенные полиэфиры.
Для отверждения подобных олигомеров достаточно использовать дифункциональные отвердители.
В таблице 3.1. приведены наиболее часто встречающиеся функциональные группы олигомеров или олигомеров и отвердителей, используемых в пленкообразующих системах.
Таблица 3.1.
Некоторые реакции, происходящие при отверждении реакционноспособных олигомеров
Типы функциональных групп учас-твующих в отверждении |
Температура отверждения, 0С |
Основная химическая реакция |
Тип взаимодействия (реакция) |
Тип образующейся группы (связи) |
Олигомеры или их композиции с отвердителями |
|
180...200 |
|
Поликонденсация |
Сложно-эфирная |
Олигоэфиры |
|
20*...140
|
|
то же |
Простая эфирная |
Фенол-, карбамидо- и меламиноформальдегидные олигомеры |
|
100*...180
|
|
Полиприсоединение |
Сложно- эфирная |
Композиции эпоксидных олигомеров с кислотным отвердителем |
|
20...180 |
|
то же |
Третичная аминная |
Композиция эпоксидных олигомеров с полиами-нами и полиамидами |
|
20...100 |
|
Полиприсоединение |
Уретано-вая |
Полиуретаны, композиции эпоксидных олигомеров с изоционатами |
радикал |
20...70 |
|
Радикальная полимеризация |
Углерод-углерод- ная |
Олигоэфир-акрилаты, олигоэфир-малеинаты, олигоуре-танакрилаты |
*нижний предел температуры при использовании катализаторов отверждения.
3.1. Пленкообразование лакокрасочных материалов, модифицированных маслами, жирными ненасыщенными кислотами или содержащими двойную связь в молекулярной цепи
К таким лакокрасочным материалов относятся алкидные материалы, олифы, олигоэфирмалеинаты, олигоэфиракрилаты, большая группа меламино-, карбамидо– и фенолформальдегидных материалов, которые содержат алкиды в качестве второго пленкообразователя, полибутадиеновые пленкообразователи и ряд других.
3.1.1. Отверждение алкидных материалов
Алкидные пленкообразователи представляют собой продукты взаимодействия спиртов и карбоновых кислот с функциональностью ƒ≥2, модифицированные растительными маслами, свободными жирными кислотами или кислотами талового масла.
Общая формула алкида может быть представлена в следующем упрощенном виде:
|
(3.1) |
где - ОН, - СООН – кольцевые функциональные группы
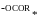 гидроксильная
и карбоксильная
гидроксильная
и карбоксильная
– остатки жирных кислот, входящих в состав
алкида (зависит от типа используемого модификатора)
Исходя из наличия указанных реакционных центров, пленкообразование алкида проходит по двум типам реакций: поликонденсации и полимеризации.
Вклад того или иного механизма определяется химическим составом исходных продуктов, а также условиями отверждения модифицированных олигомеров.
1. Поликонденсация концевых карбоксильных и гидроксильных групп с образованием сложноэфирной связи:
|
(3.2) |
Молекулярная масса исходных олигомеров растет. Для отверждения за счет поликонденсации нужны высокие температуры (не менее 150оС).
2. Полимеризация
При пленкообразовании алкидов имеет место, как правило, окислительная полимеризация.
Кислоты-модификаторы с объемными углеводородными остатками придают алкидам способность хорошо растворяться в неполярных растворителях (ксилоле, уайт-спирите и др.).
Количество двойных связей в молекуле алкида определяет их способность «к высыханию» в пленке. По способности к высыханию различают высыхающие и невысыхающие алкиды.
Хорошо отверждаются олигомеры, в молекулах которых содержится не менее 6…7 двойных связей. Это означает, что, если для модификации олигоэфира использовать высыхающее масло (например, льняное), то в молекуле достаточно ввести 2…3 жирнокислотных остатка. При модификации полувысыхающими маслами (подсолнечное, хлопковое) необходимо ввести не менее 6-ти жирнокислотных остатков.
Окислительная полимеризация относительно легко протекает уже при комнатной температуре и может быть в еще большей степени ускорена добавлением сиккативов.
Окислительная полимеризация является ценным процессом, протекает по радикальному механизму (т.е. гомолитическому механизму разрыва связи) и включает 3 стадии: инициирование, рост и обрыв цепи.
Процесс формирования покрытия начинается индукционным периодом, во время которого трехмерный продукт практически не образуется. Этот период характеризуется быстрым поглощением пленкой кислорода и взаимодействием его с α-метиленовыми группами жирнокислотных остатков.
|
(3.3) |
Двойные связи в жирнокислотных остатках активируют метиленовые группы, находящиеся в α-положении по отношению к ним. При этом энергия разрыва связи С-Н в α-метиленовой группе будет иметь минимальное значение по сравнению со всеми остальными связями в жирнокислотном остатке.
Е ще
большей активностью обладают атомы
водорода метиленовой группы расположенные
между двумя двойными связями
ще
большей активностью обладают атомы
водорода метиленовой группы расположенные
между двумя двойными связями
Образовавшийся радикал (3.3) присоединяет вторую молекулу кислорода:
|
(3.4) |
На этом заканчивается радикальная реакция замещения водорода на кислород.
Поскольку продуктом замещения вновь является радикал, он вступает в следующую реакцию, при которой отщепляется атом водорода α-метиленовой группы другого жирнокислотного остатка:
|
(3.5) |
Образовавшийся гидропероксид неустойчив и разлагается гомолитически на два радикала, инициирующих цепь последующих превращений.
|
(3.6) |
Поскольку в ходе реакции 3.3…3.6 происходит накопление свободных радикалов, рассматриваемый процесс представляет разветвленную цепную реакцию.
При накоплении в пленке активных радикалов начинается стадия роста цепи. В жидких пленках (до начала гелеобразования) рост цепи идет по нескольким типам процессов, например:
|
(3.7) |
|
(3.8) |
С этими реакциями конкурируют реакции передачи цепи:
|
(3.9) |
а также обрыва цепи, например за счет рекомбинации радикалов:
|
(3.10) |
В период близкий к точке гелеобразования в пленке происходит резкое увеличение вязкости, при этом содержание трехмерного продукта еще невелико не > 3 %. На стадии образования сетчатого полимера диффузия кислорода в пленку затруднена, поэтому рост полимерной цепи может протекать по следующим вариантам (схемам):
|
(3.11) |
|
(3.12) |
В ходе процесса пленкообразования происходит постепенное обогащение трехмерного продукта структурными фрагментами, в которых жирнокислотные остатки связаны посредством -С-С- связей и не содержат кислорода.
В связи с этим структура трехмерного покрытия, образующегося при пленкообразовании, неоднородна по толщине, что обусловлено разными условиями формирования пленки в разных слоях. Верхние (наружные) слои обогащены сетчатым полимером, в котором преобладают кислородосодержащие связи -С-О-С- , а внутренние слои полимером со связями -С-С- .
Наряду с указанными процессами может проходить также изомеризация двойных связей:
|
(3.13) |
Следует отметить, что сопряженная система двойных связей отличается пониженной свободной энергией по сравнению с такой же системой изолированных связей. Поэтому изолированные двойные связи в подходящих условиях достаточно легко превращаются в сопряженные.
Наличие в реакционной системе сопряженных двойных связей может привести к протеканию пленкообразования по механизму реакций Дильса-Альдера:
|
(3.14) |
Толщина пленок, в которых идет пленкообразование в среднем составляет 10…60 мкм. Чем больше толщина формирующейся пленки, тем в большей степени полимеризация преобладает над окислительной полимеризацией, что связано и с затрудненностью диффузии кислорода внутрь толстой пленки.
Увеличение температуры также способствует увеличению доли полимеризации в результате повышения активности двойных связей. Следует помнить, что процесс пленкообразования неизбежно сопровождается окислительной деструкцией, в результате которой образуются низкомолекулярные кислородосодержащие продукты распада (спирты, альдегиды, кислоты и др.). Роль этих процессов особенно велика в наружных слоях пленки, поскольку они формируются в условиях большего доступа кислорода.
Процессы деструкции при пленкообразовании:
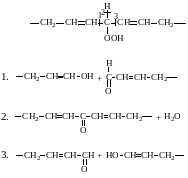
Выделение низкомолекулярных продуктов и, следовательно, протекание химических реакций наблюдается и после завершения процесса пленкообразования. Так в случае масляных покрытий холодной сушки в первые 20…30 суток эксплуатации количество летучих продуктов (альдегидов, кислот, спиртов) достигает 4 ∙ 10-2 %/сут, а к концу третьего месяца 2,5 ∙ 10-3 %/сут.
Степень окисления при пленкообразовании зависит от строения псириокислотных остатков. Наибольшее количество легколетучих низкомолекулярных продуктов деструкции образуется при пленкообразовании кислот с низкой степенью ненасыщенности (олеиновая кислота, масла – оливковое, рапсовое и др.), а наименьшее – в случае высоконенасыщенных кислот (линолевой, элеостириновой). Это объясняется большей продолжительностью индукционного периода кислот с низкой степенью ненасыщенности, в течение которого доступ кислорода в формирующуюся пленку практически неограничен. Поэтому глицериды олеиновой кислоты, неспособной к высыханию в тонких пленках, претерпевают глубокое окисление.
К моменту завершения формирования покрытия степень использования двойных связей никогда не достигает 100 %, поэтому пленка остается потенциально реакционноспособной.
Процесс окислительной полимеризации ускоряется при введении в лакокрасочные материалы сиккативов, которые представляют собой растворимые в маслах соли некоторых тяжелых металлов переменной валентности (RCOO)хMe, где Ме – металл (Со, Мn, Рb, Fe и др.), R–алифатический или алициклический углеводородный радикал.
Наибольшее распространение в качестве сиккативов получили соли нафтеновых кислот (нафтенаты), смоляных кислот канифоли (резинаты), жирных кислот льняного масла (линолеаты) и др.
В процессе окислительной полимеризации присутствие сиккатива, например соли двухвалентного кобальта Со(RCOO)2, приводит к образованию окислительно-восстановительной системы «гидропероксид – Ме», значительно ускоряющей процесс распада гидропероксидов:
|
(3.15) |
|
(3.16) |
Помимо ускоряющего действия на разложение гидропероксидов, сиккативы этой группы могут также ускорять и процесс их образования.
Один из возможных механизмов такого действия заключается в непосредственном взаимодействии ионов металла (в состоянии высшей валентности) с α-метиленовой группой жирнокислотных остатков с образованием радикала:
|
(3.17) |
Далее процессы пленкообразования протекают аналогично ранее представленным реакциям (3.4 и 3.5).


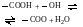



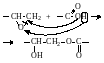
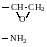
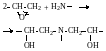
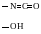
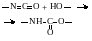
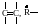 свободный
свободный