Тема – 47: Углеводы
Углеводы служат источником энергии, являются «строительным материалом» клеточных стенок растений и некоторых организмов, а также определяют защитные (иммунные) свойства млекопитающих. Углеводы получают главным образом из растительных источников. Это связано с тем, что углеводы являются первичными продуктами фотосинтеза, осуществляемого растениями из оксида углерода(IV) и воды.
Углеводы объединяют разнообразные соединения — от низкомолекулярных, построенных всего из нескольких атомов углерода, до полимеров с молекулярной массой в несколько миллионов. Поэтому трудно дать строгое определение класса углеводов. Название «углеводы» возникло потому, что многие представители этого класса (например, глюкоза С6Н12О6, сахароза С12Н22О11) имеют общую формулу Сn(Н2О)m и формально могут быть отнесены к «гидратам углерода». Известно множество углеводов, не отвечающих этой формуле, тем не менее термин «углеводы» употребляется до настоящего времени.
В углеводах выделяют три самостоятельных класса:
1. моносахариды,
2. олигосахариды (дисахара)
3. полисахариды.
47.1. Моносахариды
471.1. Классификация
Моносахариды — это гетерофункциональные соединения, содержащие оксогруппу и несколько гидроксильных групп, т. е. полигидроксиальдегиды и полигидроксикетоны.
Если моносахариды содержат альдегидную группу, то они назы ваются альдозами, если кетонную группу — то кетозами. Для названии моносахаридов характерен суффикс -оза, например глюкоза, рибоза, фруктоза.
В зависимости от длины углеродной цепи моносахариды делятся на триозы (3 атома углерода), тетрозы (С4), пентозы (C5), гексозы (С6) и т. д., из которых наиболее распространены пентозы и гексозы.
15.1.2. Стереоизомерия
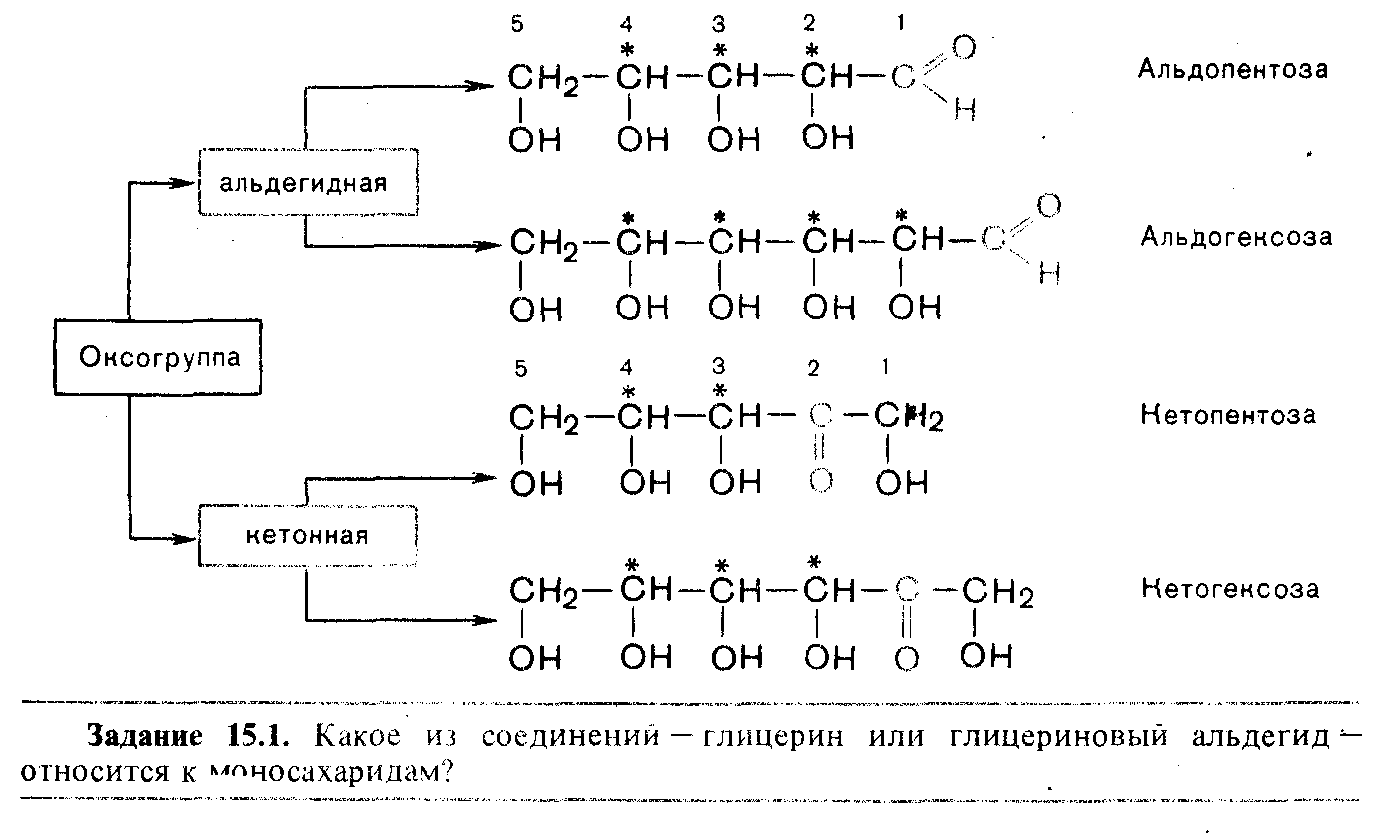
Моносахариды содержат несколько асимметрических атомов углерода, и поэтому одной и той же структурной формуле соответствуют несколько стереоизомеров. Например, в альдопентозе таких центров три (в формуле они отмечены звездочками). У альдогексоз будет уже 16 стереоизомеров, т. е. восемь пар энантиомеров, так как углеродная цепь содержит на один асимметрический атом больше.
Углеродная цепь в моносахаридах нумеруется с того конца, ближе к которому находится старшая функциональная группа — карбонильная.
Моносахариды записывают в виде проекционных формул Фишера, располагая углеродную цепь вертикально так, чтобы наверху находился атом С-1.
Расположение гидроксильной группы у «определяющего» хирального центра слева говорит о принадлежности моносахарида к L-ряду, справа —к D-ряду, т. е. отнесение проводится по стереохимическому стандарту — глицериновому альдегиду. Большинство природных моносахаридов принадлежит к D-ряду. В приведенных примерах не была отражена конфигурация остальных центров хиральности. Понятно, что конфигурация каждого из асимметрических атомов может быть обозначена по D, L-системе. Однако это привело бы к слишком громоздким названиям. Поэтому в химии углеводов продолжают применяться тривиальные названия, признанные и международной номенклатурой.

Если два стереоизомера отличаются конфигурацией всех атомов углерода, то они относятся друг к другу, как предмет и его зеркальное отражение и являются энантиомсрами. Пример энантиомеров — D-глюкоза и L-глюкоза, имеющие одинаковые химические и физические свойства (кроме знака оптического вращения).
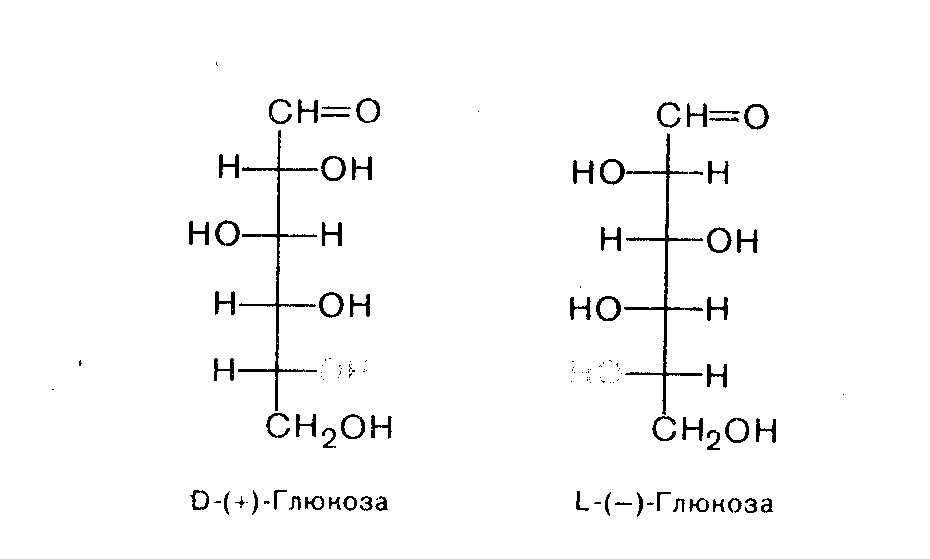
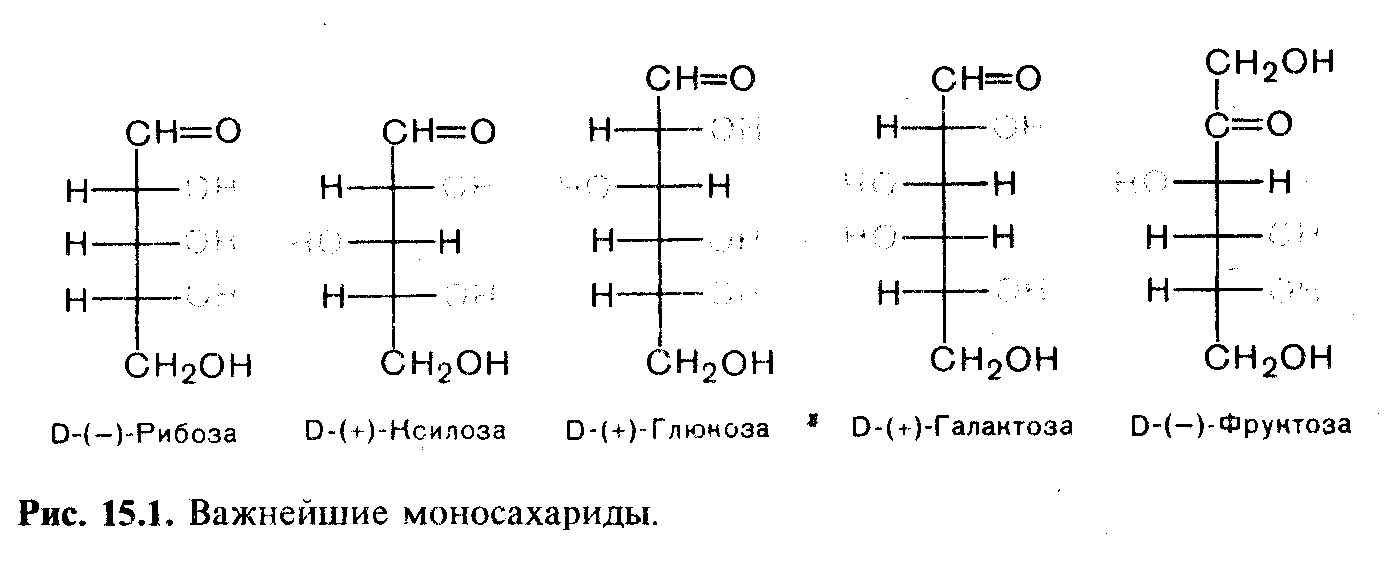
15.1.3. Циклические формы
До сих пор моносахариды были представлены как соединения с открытой (незамкнутой) цепью. Однако давно было известно, что ряд свойств моносахаридов не согласуется с подобной структурой. Так, по-особому ведет себя одна из многих гидроксильных групп, изменяется величина оптического вращения во времени. В поисках объяснения этих фактов было высказано предположение о циклическом строении моносахаридов. Впервые идея циклического строения была выдвинута русским химиком А. А. Колли (1870), а затем развита Б. Толленсом (1883).
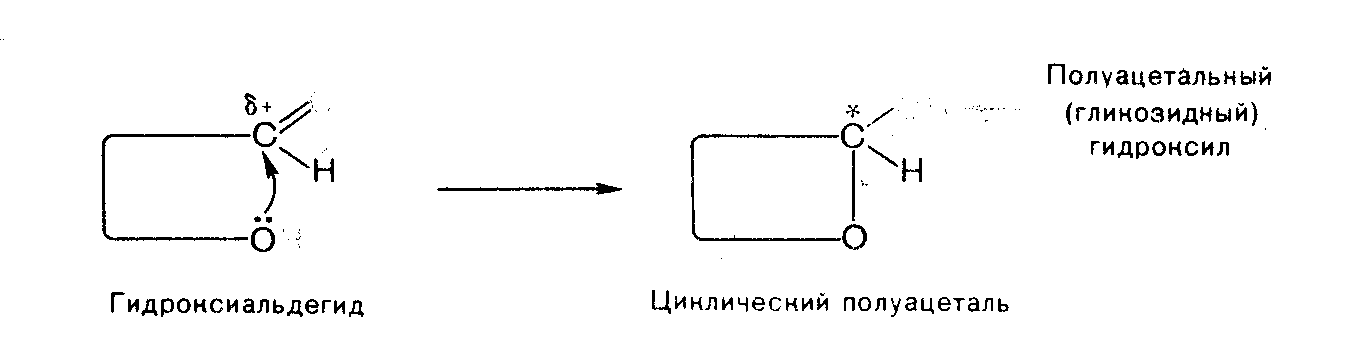
Возможность циклизации моносахаридов обусловлена двумя факторами. Во-первых, цепи из пяти и более атомов углерода могут принимать клешневидную конформацию, в результате чего оказываются сближенными карбонильная и гидроксильные группы при С-5 или при С-4. Во-вторых, взаимодействие гидроксильной и карбонильной групп, приводящее к полуацеталям, протекает в случае моносахаридов внутримолекулярно. Продуктом такого превращения является циклический полуацеталь (для наглядности этот процесс изображен схематически).
Если в образовании циклической формы принимает участие гидроксильная группа при С-5 альдоз, то образуется шестичленный
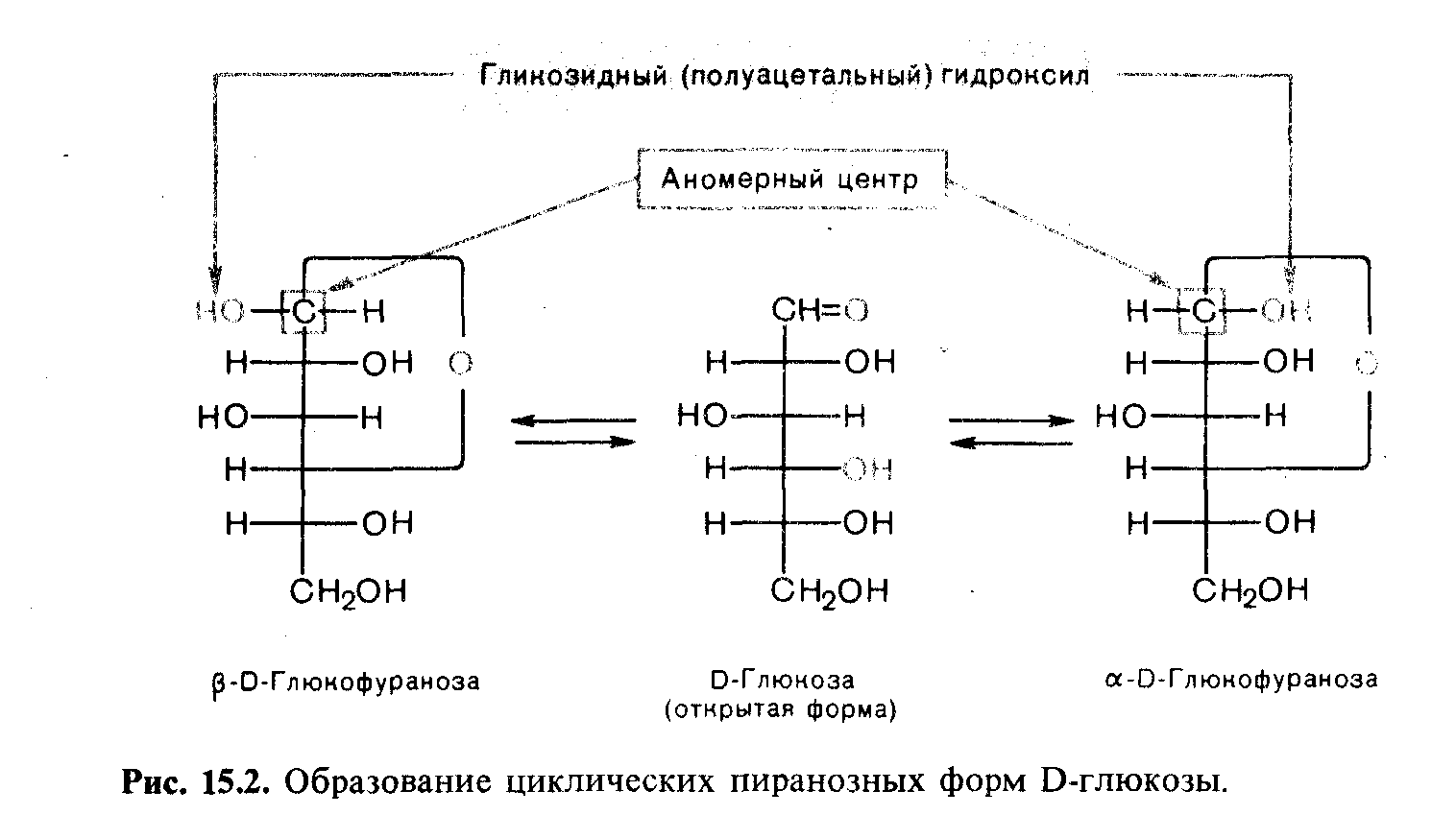
цикл, называемый пиранозным (от шестичленного гетероцикла пирана, рис. 15.2). Образовавшаяся в результате циклизации полуацетальная гидроксильная группа называется гликозидной.
В циклической форме уже нет альдегидной группы, и атом С-1 становится ,sp3-гибридизованным. При взаимодействии оксогруппы с гидроксильной группой при С-4 альдоз замыкается пятичленный цикл, называемый фуранозным. Приведенные на рис. 15.2 и 15.3 изображения циклических форм моносахаридов называются формулами Колли —Толленса.
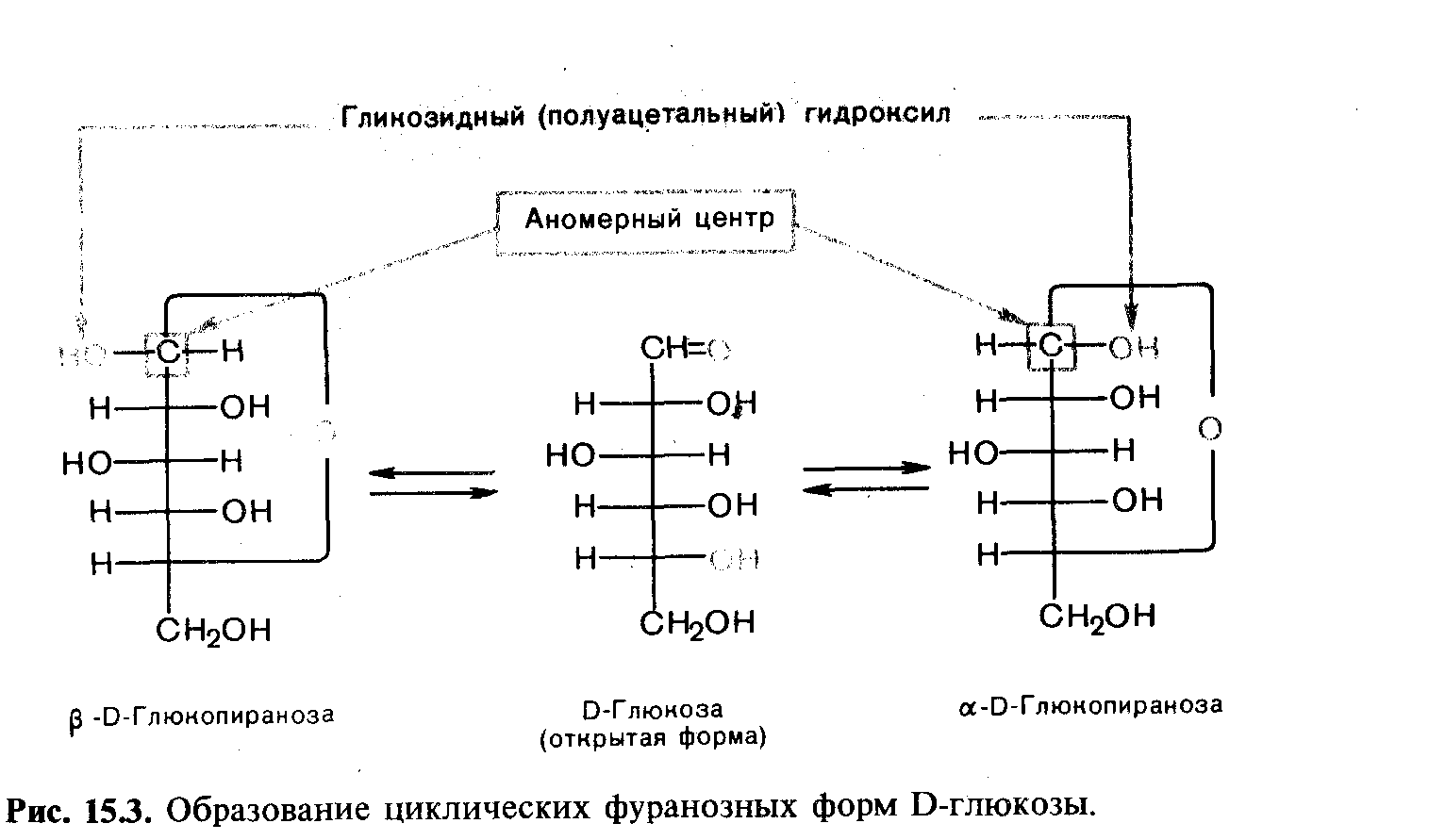

Формулы Хеуорса. Формулы Колли — Толленса громоздки и плохо отражают реальную форму моносахаридов. Более наглядными являются формулы Хеуорса, в которых пиранозные и фуранозные циклы изображаются в виде плоских многоугольников, лежащих перпендикулярно плоскости рисунка. Атом кислорода в цикле располагается за плоскостью рисунка, причем для пираноз —в правом углу. Заместители располагаются над и под плоскостью цикла. Символы
атомов углерода, как это и ранее делалось при написании формул циклических соединений, обычно опускаются.
Для перехода от проекционных формул Фишера или формул Колли —Толленса к формулам Хеуорса можно пользоваться следующими упрощенными правилами.
1.У пираноз D-ряда группа СН2ОН располагается над плоскостью цикла.
2.Заместители, находящиеся справа от вертикальной линии углеродной цепи, в формуле Хеуорса оказываются под плоскостью цикла, и наоборот. Это значит, что у моносахаридов D-ряда полуацетальный гидроксил.
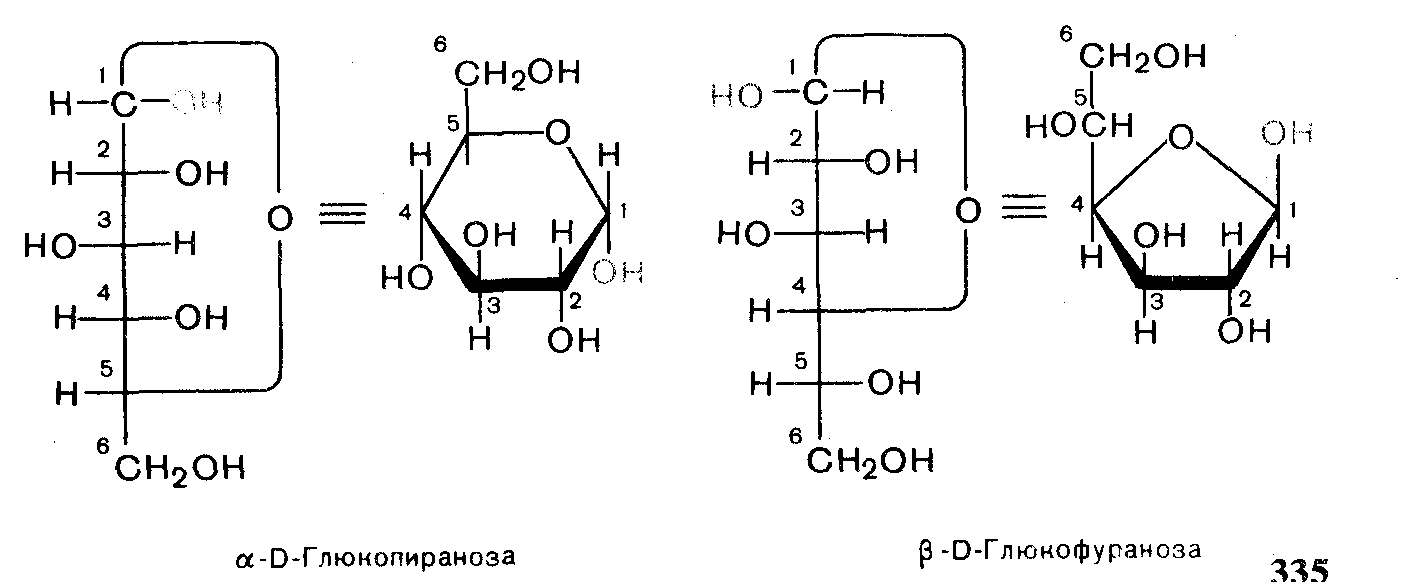
α-аномеров находится под плоскостью цикла, а Р-аномеров — над нею.
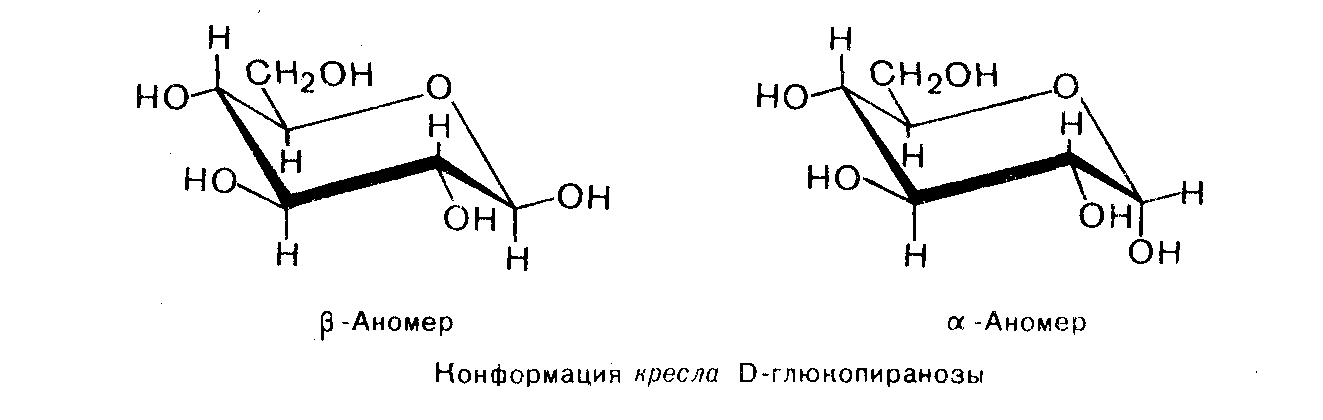
Несмотря на то, что в формулах Хеуорса моносахариды изображаются в виде плоского многоугольника, в действительности они не имеют плоского строения. Например, шестичленный пиранозный цикл, подобно циклогексану, принимает наиболее выгодную конформацию кресла. В наиболее распространенных моносахаридах объемная первичноспиртовая группа СН2ОН и большинство гидроксильных групп занимают энергетически выгодные экваториальные положения. Надо указать, что D-глюкопираноза—единственная гексоза, в которой все заместители расположены экваториально
Высокой энергетической устойчивостью D-глюкопиранозы, обусловленной ее конформационным строением, объясняется тот факт, что D-глюкоза — самый распространенный в природе моносахарид.