
8.2 Электрохимическая коррозия
Самопроизвольное разрушение металла в среде электролита, которое сопровождается возникновением электрического тока за счет работы микро- или макро-гальванических пар, называется электрохимической коррозией.
Коррозия состоит из двух одновременно протекающих процессов - анодного и катодного. На анодных участках происходит ионизация металла, а на катодных - присоединение электронов окисляющими ком-понетами электролита. Разрушение металла, следовательно, идет только на анодных участках.
К электрохимической коррозии относят все случаи коррозии металла в водных растворах или во влажной атмосфере (суда, трубопроводы, и т.д.). Металл разрушается на воздухе, так как вследствие конденсации паров воды на нем появляется тонкая пленка влаги. В образовавшейся пленке растворяются кислород и другие газы, содержащиеся в воздухе (С02, SO2, H2S, NH3), с образованием соответствующих электролитов.
Причиной электрохимической коррозии могут быть следующие явления.
1. Химическая и физическая неоднородность металла. Она может быть при наличии в металле микровключений из других металлов, неодно родности сплавов, оксидной пленки на поверхности металла, наличия в конструкции узлов из разных металлов.
Неоднородность электролита, контактирующего с металлом. Она может заключаться в разной концентрации ионов металла в отдельных частях электролита, различном рН, в неравномерной аэрации металла, различной скорости обтекания металла водой.
Неоднородность физических условий. Она выражается в разной температуре на отдельных участках металла, неравномерном распределении лучистой энергии или электрического поля, в наличии механических напряжений в металлической конструкции. Эти причины могут изменять поверхностный электродный потенциал металла.
Термодинамика
электрохимической коррозии. Более
активные металлы (при контакте разных
металлов), либо участки поверхности
одного и того же металла с меньшими
потенциалами являются анодами. На них
происходит разрушение металла. Анодный
процесс в
общем виде: Me
- n ё
= Меn+
ё
= Меn+
Менее активные металлы (при контакте разных металлов), либо участки поверхности одного и того же металла с большими потенциалами играют роль катодов, на них происходит присоединение электронов окислителем. Катодные процессы зависят от состава электролита, его рН и от величины электродного потенциала металла. Рассмотрим возможность протекания некоторых катодных процессов.
Восстановление
ионов водорода. Коррозия
с участием ионов Н+
называется
коррозией с выделением водорода или
коррозией с водородной деполяризацией.
Она наблюдается в кислых и нейтральных
средах. Термодинамическая вероятность
процесса определяется соотношением:
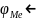 0,059 рН (при рн2=1).
0,059 рН (при рн2=1).
Коррозия
металла с восстановлением водорода Н"
будет происходить в том случае, если
равновесный потенциал металла будет
меньше, чем у водорода в данной среде.
Следовательно, если
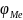
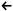 0,059 рН, то возможна коррозия металла с
участием ионов водорода, а катодный
процесс в кислой среде выразится
уравнением:
0,059 рН, то возможна коррозия металла с
участием ионов водорода, а катодный
процесс в кислой среде выразится
уравнением:
2Н+ +2ё = Н2
Таким образом, в сильнокислых средах (рН=1) могут корродировать все металлы, имеющие потенциал меньше -0,059 В.
В нейтральной среде (рН=7) равновесный потенциал водорода равен -0,41В; значит, металлы, потенциалы которых меньше этой величины, могут корродировать в нейтральных растворах с выделением водорода:
2Н20+ 2ё = Н2 + 2ОН-
Восстановление
кислорода.
Коррозия
с участием кислорода называется
коррозией с поглощением кислорода или
коррозией с кислородной деполяризацией.
Восстановление кислорода возможно в
разных типах сред. Его термодинамическая
возможность определяется соотношением:
 1,228 - 0,059рН (при pO2=l)-
1,228 - 0,059рН (при pO2=l)-
В
нейтральной среде (рН=7) в присутствии
кислорода (во влажном воздухе, морской
воде и т.п.) равновесный потенциал
кислорода равен
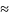 0,8В.
В таких средах могут корродировать
металлы, имеющие потенциал меньше,
чем
0,8B.
Процесс описывается уравнением:
0,8В.
В таких средах могут корродировать
металлы, имеющие потенциал меньше,
чем
0,8B.
Процесс описывается уравнением:
02 + 4ё + 2Н20 = 40Н-
В щелочных средах (рН=14) в присутствии кислорода могут корродировать металлы, имеющие потенциал меньше 0,4В. Катодный процесс выражается тем же уравнением:
02 + 4ё + 2Н20 - 40Н-
Наиболее агрессивными являются кислые среды, содержащие растворенный кислород. В этом случае разрушаются практически все металлы, имеющие потенциал меньше 1,2В. Катодный процесс описывается уравнением:
02 + 4ё + 4Н+ = 2Н20.
Виды электрохимической коррозии. При контакте металлов с разными потенциалами в среде электролита происходит контактная коррозия, протекающая с образованием макро - гальванических элементов. Разрушению подвергается металл с меньшим потенциалом (анод), а на металле с большим потенциалом (катод) идет процесс восстановления окислителя из среды.
Например, рассмотрим коррозию возникающую при контакте железа и никеля во влажном воздухе.
Стандартные потенциалы железа и никеля:
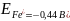

Процесс протекает по стадиям:
 анодный
анодный
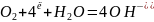 катодный
катодный
Схема образовавшейся гальванопары:
Fe/ Fe2+ | Н20, 02 | (Ni) 2Н20, 02/ 40Н-
В электролите ионы Fe + и ОН- взаимно осаждают друг друга в виде нерастворимого Fe(OH)2 :
2Fe2+ + 40H- = 2Fe(OH)2
Затем атмосферный кислород окисляет часть Fe(OH)2 до FeO(OH):
4Fe(OH)2 + 02 = 4FeO(OH) + 2Н20
Получившийся метагидроксид железа FeO(OH) с Fe(OH)2 при высыхании образуют ржавчину:
2FeO(OH) + Fe(OH)2 = (Fe" Fe'"2) 04 + 2H20
Образовавшийся бурый рыхлый осадок (ржавчина) не создает на поверхности железа плотной пленки и не защищает его от коррозии. Наоборот, способствует дальнейшему разрушению металла, так как участки покрытые ржавчиной имеют потенциал больше, чем потенциал стали.
Если коррозия пары железо - медь протекает в кислой среде, то происходят следующие процессы:
Fe - 2ё = Fe + анодный
2Н+ + 2 ё = Н2 катодный
Схема образовавшейся гальванопары:
Fe/ Fe2+ | HCl | (Сu) 2Н+ / Н2
Ионы железа Fe2+ будут оставаться в растворе электролита, т.е. образуется раствор соли железа.
Следует учесть, что контакт с менее активным металлом обычно усиливает коррозию более активного металла. Коррозия металла с более положительным потенциалом замедляется.
Аналогично контактной коррозии протекает примесная коррозия. Например, стальные изделия корродируют за счет образования на их поверхности множества микрогальванических элементов, в которых анодом является железо, а катодом - легирующие добавки.
Различают неметаллические примеси (С, Si, P, S) и металлические (Mn, Ni, Сг; реже V, W, Mo, Ti, Co). Неметаллические примеси поляризуются катодно (поскольку их потенциал больше), а металлические – в зависимости от величины потенциала по отношению к железу - анодно или катодно.
Неоднородность состава электролита, соприкасающегося с металлом может стать причиной коррозии. Если металл омывается электролитом разного состава, то появляются условия для работы концентрационных гальванических элементов. Коррозия возникает также, когда металл соприкасается с электролитом, рН которого отличается на отдельных участках поверхности металла.
Коррозия вследствие неравномерной аэрации (насыщения кислородом). Исследования показали, что даже на однородной поверхности металла могут образоваться локальные гальванические элементы, если разные ее участки неравномерно снабжаются кислородом. В местах с большей концентрацией кислорода металл не окисляется (катодные участки), а в местах с меньшей концентрацией кислорода происходит коррозионное разрушение металла (анодные участки). Это служит причиной таких видов коррозии, как точечная (питгинг) коррозия в грунтах, коррозия, вызванная проточной водой.
Рассмотрим пример точечной коррозии. Она наблюдается там, где анодами служат небольшие участки поверхности металла. Для ее возникновения достаточно, чтобы небольшие частички или пузырьки какого-либо газа прилипли на длительное время к поверхности металла. Под такими частицами кислород быстро иссякает, а в результате диффузии его поступает гораздо меньше, чем к остальной поверхности металла. Участок, плохо снабжаемый кислородом, становится анодом, и металл здесь разрушается. В результате образуется каверна, на дне которой снабжение кислородом еще меньше, что усиливает коррозию; в металле появляются маленькие дырочки.
Протекающие процессы:
Fe - 2ё = Fe2+ анодный
02 + 4ё + 2Н20 = 40Н- катодный
Схема образовавшейся гальванопары:
Fe/ Fe2+ | Н20, 02 | (Fe) 2H20, 02 / 40Н-
[02]меньше [02]больше
При протекании катодного процесса среда подщелачивается и поверхность стали пассивируется, скорость коррозии на этих участках снижается (см. рис. 17).
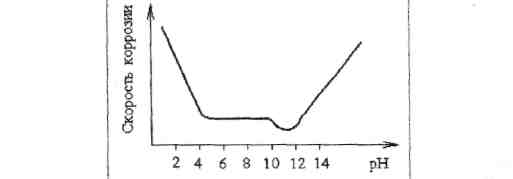
Рис.17. Зависимость скорости коррозии железа и его сплавов от рН раствора
Железо и его сплавы интенсивно корродируют в сильнокислых и сильнощелочных средах. В области рН 4 - 8,5 скорость коррозии низка и постоянна. При рН 10 скорость коррозии падает из-за образования пассивирующих пленок.
