
- •Методичні вказівки
- •Зміст модуля II
- •7. Розчини
- •7.1 Загальна характеристика розчинів
- •7.2 Концентрація розчиненої речовини
- •7.3 Властивості розчинів
- •7.3. Питання та задачі для самоконтролю
- •8.Розчини електролітів
- •8.1. Загальна характеристика розчинів електролітів
- •8.2.Реакції в розчинах електролітів
- •8.3. Запитання для самоконтролю
- •8.4. Задачі для самоконтролю
- •9. Комплексні сполуки
- •9.1.Загальна характеристика комплексних сполук
- •9.2.Номенклатура комплексних сполук
- •9.3.Природа координаційного зв’язку
- •9.4.Класифікація комплексних сполук.
- •9.5.Дисоціація комплексних сполук у розчинах. Стійкість комплексних іонів.
- •9.6.Ізомерія комплексних сполук
- •9.7.Властивості комплексних сполук
- •9.8.Основні способи одержання комплексних сполук.
- •9.9.Значення та застосування комплексних сполук
- •9.10.Запитання та задачі для самоконтролю
- •8. Номенклатура комплексних сполук.
- •10. Окисно-відновні реакції
- •10.1.Загальна характеристика процесів окислення та відновлення
- •10.2.Складання рівнянь окисно-відновних реакцій
- •10.3. Запитання та задачі для самоконтролю
- •11. Загальні та електрохімічні властивості металів
- •11.1. Загальні властивості металів
- •11.2. Гальванічні елементи. Корозія металів
- •11.3. Електроліз
- •11.4. Запитання та задачі для самоконтролю
- •Список рекомендованої літератури
7.2 Концентрація розчиненої речовини
Концентрація - одне із важливих понять у теорії розчинів. Під концентрацією розуміють кількісну оцінку вмісту речовини (компонента) в системі.
На практиці найчастіше використовують такі способи вираження концентрації: масова доля, молярна доля, об'ємна доля, масова концентрація, молярна концентрація, моляльність, еквівалентна молярна концентрація (раніше називалась нормальна концентрація).
Розглянемо деякі способи вираження концентрації розчиненої речовини:
І)масова доля ω(Х) - безрозмірне відношення маси компоненту m(Х) до маси розчину ( Х – формульне позначення частки речовини):
![]() ;
;
![]()
Приклад. Обчислити масову долю NaCl, якщо відомо, що 20 г хлориду натрію розчинено у 180 г води.
Рішення:
![]() або 10%
або 10%
2)молярна
доля N(Х)
- відношення кількості
речовини компонента
![]() до
загальної кількості речовини всіх
компонентів розчину:
до
загальної кількості речовини всіх
компонентів розчину:
![]() ,
,
де:
![]() m(X) –
маса компонента (X);
m(X) –
маса компонента (X);
M(X) – молярна маса компонента (X).
Приклад. Обчислити молярну долю глюкози у розчині, одержаному при розчиненні 18 г глюкози у 180 г води.
Рішення:
![]()
![]()
![]() Цей
спосіб вираження концентрації широко
використовується при термодинамічних
розрахунках.
Цей
спосіб вираження концентрації широко
використовується при термодинамічних
розрахунках.
3)масова концентрація T(X) – відношення маси компонента т(X) до об'єму розчину (раніше називалась титр розчину):
![]()
Приклад. У 200 мл розчину знаходиться 10 г хлориду натрію. Обчислити масову концентрацію розчину.
Рішення:
![]()
4)молярна концентрація С(Х) - відношення кількості речовини компонента до об'єму розчину
![]()
Приклад. У 500 мл розчину знаходиться 10,6 г Na2CO3.
Обчислити молярну концентрацію розчину.
Рішення:![]()
5)молярна концентрація еквівалента СЕ(Х) (еквівалентна концентрація) - це відношення еквівалентної кількості розчиненої речовини до об'єму розчину.
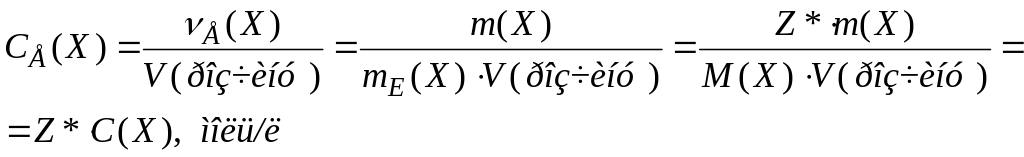 де mE(Х)
– молярна маса еквівалента розчиненої
речовини. Величину Z*
називають числом(фактором) еквівалентності.
Число еквівалентності для елемента
дорівнює його валентності в сполуці,
для кислоти - основності, для основи -
кислотності, або валентності металу;
для речовин, які беруть участь в
окисно-відновних реакціях
- числу електронів, які приймають або
віддають атоми окислювача або
відновника.
де mE(Х)
– молярна маса еквівалента розчиненої
речовини. Величину Z*
називають числом(фактором) еквівалентності.
Число еквівалентності для елемента
дорівнює його валентності в сполуці,
для кислоти - основності, для основи -
кислотності, або валентності металу;
для речовин, які беруть участь в
окисно-відновних реакціях
- числу електронів, які приймають або
віддають атоми окислювача або
відновника.
Приклад. У 200 мл розчину знаходиться 4,9 г сірчаної (сульфатної) кислоти. Обчислити молярну концентрацію еквівалентів сульфатної кислоти.
Рішення.
![]()
Між об'ємом розчину і його молярною концентрацією еквівалента існує обернено пропорційна залежність:
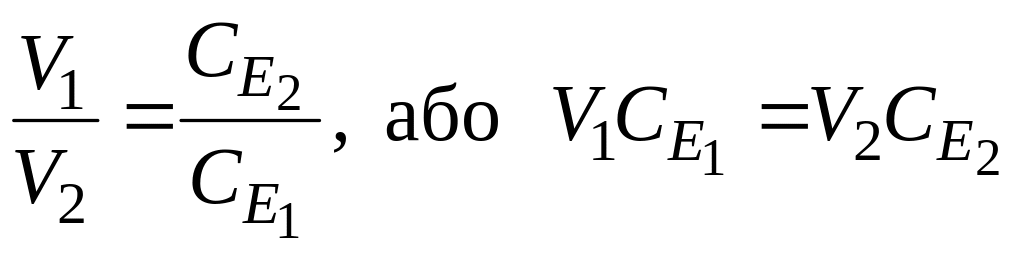
За цією залежністю можна не тільки обчислювати об'єми розчинів, потрібні для проведення реакцій, а й за об'ємами розчинів, що беруть участь у реакції, знаходити їхні концентрації.
6)моляльна концентрація (моляльність розчину)Сm(Х) - це відношення кількості розчиненої речовини до маси розчинника (кг). Вона показує кількість молів розчиненої речовини, що припадає на 1 кг розчинника:
![]()
Приклад. 18 г глюкози розчинено у 500 г води. Розрахувати моляльність одержаного розчину.
Рішення:![]() Моляльність
використовують при фізико-хімічних
дослідженнях розчинів, наприклад, при
кріоскопічних та ебуліоскопічних
визначеннях.
Моляльність
використовують при фізико-хімічних
дослідженнях розчинів, наприклад, при
кріоскопічних та ебуліоскопічних
визначеннях.
