
- •Подставляя это выражение в (11), получим
- •Разделив полученное выражение на cvpdV и введя обозначение , получим
- •Характеристики измерительных приборов
- •Описание экспериментальной установки и вывод расчётных формул
- •Решая систему уравнений (14) и (16), получим
- •Расчёт погрешностей
- •Контрольные вопросы
- •Первое начало термодинамики математически записывается в виде
- •Подставляя это выражение в (11), получим
- •Разделив полученное выражение на cvpdV и введя обозначение , получим
Решая систему уравнений (14) и (16), получим
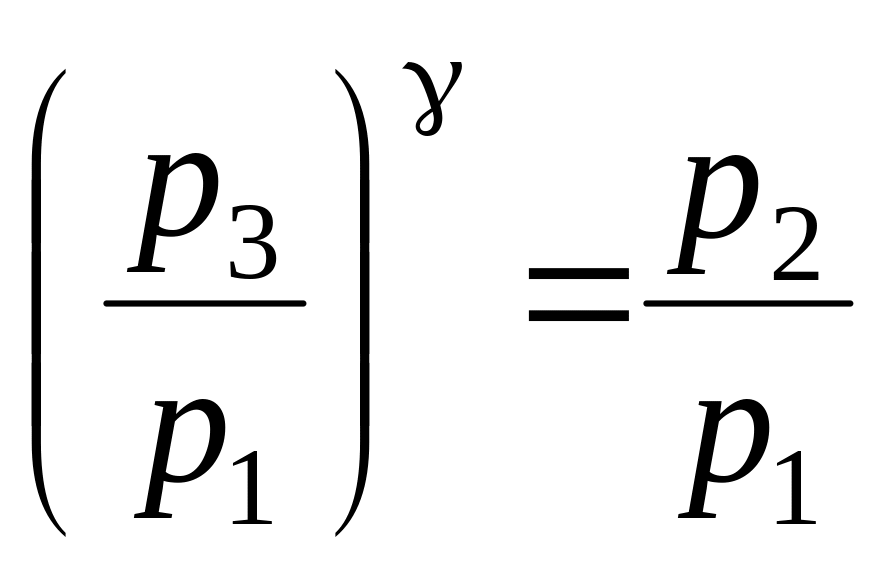 .
.
После логарифмирования имеем
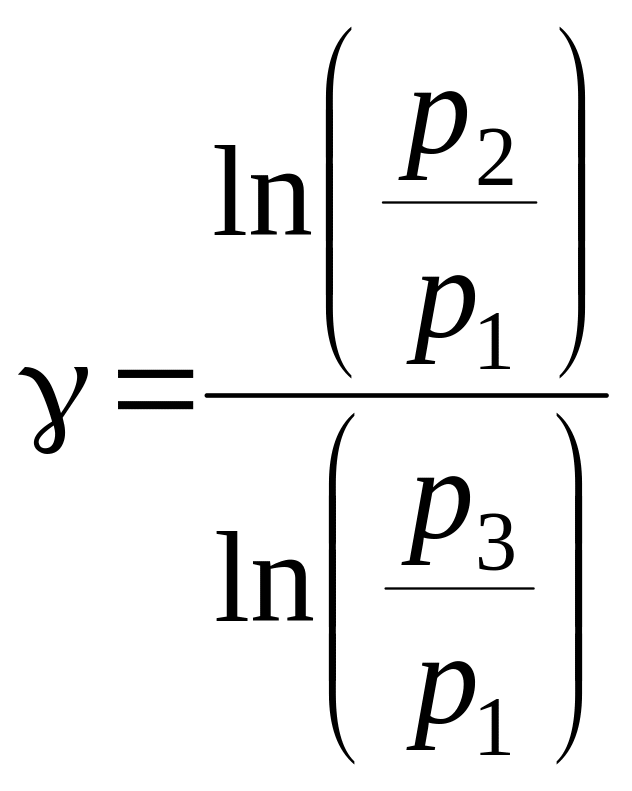 .
(17)
.
(17)
С учётом равенств (13) и (15) можно записать
p = p0 = p1 - gh1,
p = p1 – (gh1 - gh2).
После подстановки этих выражений в уравнение (17) получаем следующее выражение для показателя адиабаты:
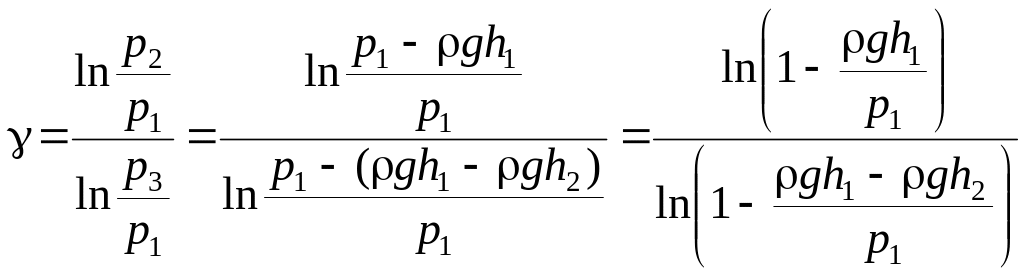 .
.
Как известно из курса высшей математики, функцию ln(1+x) можно разложить в ряд Маклорена следующим образом:
![]() .
.
При условии x << 1 можно ограничиться первым членом ряда и принять, что ln(1+x) x. В нашем случае при выполнении условия
![]() (18)
(18)
выражение для показателя адиабаты принимает следующий вид:
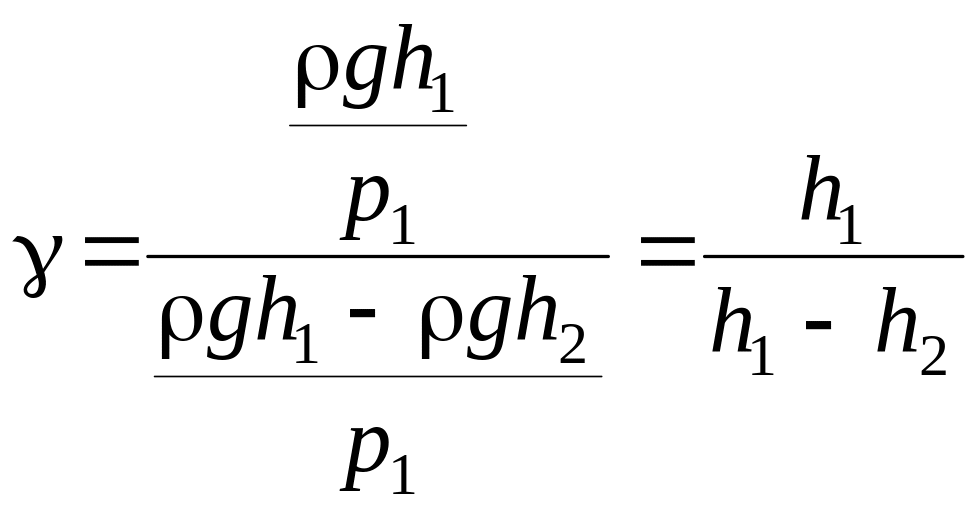 ,
(19)
,
(19)
которая и является расчётной для экспериментального определения .
Таблица результатов измерений
№ |
h1, мм |
h2, мм |
i |
i |
(i)2 |
1 2 3 4 5 6 7 8 |
170 185 215 185 190 180 200 195 |
55 65 70 60 65 55 70 65 |
1,48 1,54 1,48 1,48 1,52 1,44 1,53 1,50 |
0,02 0,04 0,02 0,02 0,02 0,06 0,03 0 |
0,0004 0,0016 0,0004 0,0004 0,0004 0,0036 0,0009 0 |
Пример расчета
; I = 170/170-55= 1,48
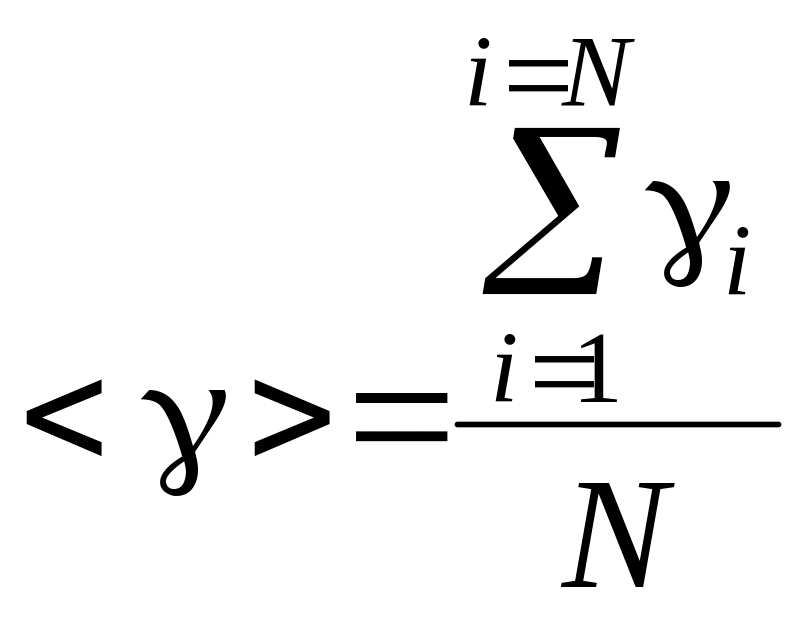 ;
i
= |<>
- i|;
;
i
= |<>
- i|;
Расчёт погрешностей
Среднее арифметическое: , где N – число опытов.
i = |<> - i|.
Среднее квадратическое отклонение:
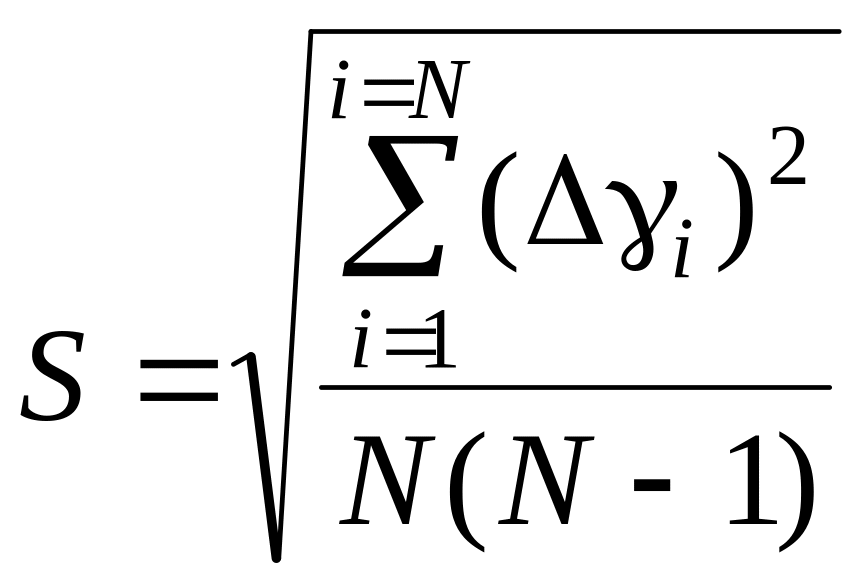 .
.
Коэффициент Стьюдента t, n определить из таблицы, приняв доверительную вероятность = 0,95.
Абсолютная погрешность: = t, nS.
Относительная
погрешность:
![]() .
.
Контрольные вопросы
1. Сформулировать первое начало термодинамики словесно в общем виде и записать его в виде формулы для всех изопроцессов.
Первое начало термодинамики математически записывается в виде
Q = dU + A, (1)
где Q – теплота, сообщаемая системе; dU – изменение внутренней энергии системы; A – работа, совершенная системой в процессе.
Важнейшими тепловыми характеристиками однородных тел являются их удельная c и молярная C теплоёмкости. Удельная теплоёмкость тела равна количеству теплоты, необходимому для изменения температуры 1 кг тела на 1 К:
.
2. Какой процесс называется адиабатным? Записать уравнение адиабатного процесса.
Адиабатным называется процесс, протекающий без теплообмена с окружающей средой (Q = 0). Первое начало термодинамики для адиабатного процесса можно записать в виде
.
3. Каков физический смысл молярной и удельной теплоёмкостей?
Молярной теплоёмкостью называется физическая величина C, численно равная теплоте, которую нужно сообщить 1 молю вещества для изменения его температуры на 1 К:
, (3)
где = m/ - количество вещества, моль; - молярная масса, кг/моль. Единица измерения молярной теплоёмкости Дж/(мольК).
Удельная теплоёмкость тела равна количеству теплоты, необходимому для изменения температуры 1 кг тела на 1 К:
. (2)
Единица измерения удельной теплоёмкости тела Дж/(кгк)
4. От чего зависит значение показателя адиабаты? Чему равно его значение для водяного пара?
Если открыть полностью вентиль и закрыть его в тот момент, когда давление воздуха в баллоне сравняется с атмосферным, то выбранный нами «объём» при этом увеличится до значения V2, а температура воздуха в баллоне понизится до значения T2, так как при своём расширении воздух совершает работу против атмосферного давления. Итак, в момент закрытия вентиля параметры воздуха в «объёме» p2, V2, T2. Считая процесс перехода из состояния 1 в состояние 2 адиабатным, можем записать
.
Показатель адиабаты Q = 0
5. Записать теоретические соотношения между Сp и CV.
Дифференцируя уравнение Клапейрона-Менделеева получим
или .
