
Диаграмма Латимера для азота:
а) в кислой среде
 б)
в щелочной среде
б)
в щелочной среде
-0,86 + 0,88 -0,46 +0,76 +0,94 -3,4
N O3-
N2O4
NO2-
NO N2O
N2
N3-
O3-
N2O4
NO2-
NO N2O
N2
N3-
 (NO2)
(NO2)
+0,16 +0,73 -2,86

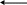 NH3
N2H4
NH2OH
NH3
N2H4
NH2OH
- Укажите соединения азота, проявляющие
а) только окислительные свойства………
б) только восстановительные свойства…….
в) двойственные окислительно-восстановительные свойства…….
- Укажите и сравните окислительные свойства в ряду кислот:
– H3PO4 ……………..– HNO2 ……..………. - HNO3……...
Опыт 1. Свойства гидроксида аммония и его солей
а) В пробирку внести 2-3 капли раствора соли аммония и добавить 2-3 капли 2 н раствора гидроксида натрия. Слегка нагреть пробирку и над ее отверстием подержать влажную универсальную индикаторную бумажку.
- По запаху и по изменению цвета индикаторной бумажки убедитесь в выделении газа…..……….
- Написать в молекулярной и ионной форме уравнения реакций:
NH4Cl + NaOH →
- Отметить и объяснить изменение цвета индикатора, указав, что собой представляет водный раствор аммиака.
- Написать уравнения диссоциации гидроксида аммония:
NH4OH → …..…… + ……
- Составьте выражение для константы диссоциации.
K1 =
- Значение константы диссоциации из таблицы.
K1 = 1,76 10-5
- Сделайте вывод о свойствах гидроксида аммония.
б) На предметное стекло поместить три кусочка универсальной индикаторной бумаги и нанести на них по 1 капле растворов солей: хлорида аммония, нитрата аммония и ацетата аммония. Определить pH растворов солей.
- рН в растворах солей
- Написать в молекулярной и ионной форме уравнения реакций гидролиза солей.
NH4Cl + H2O →
NH4NO3 + H2O →
CH3COONH4 + H2O →
- Объясните результаты
Опыт 2.Получение и свойства оксида азота (III)
Внести в пробирку 3-4 капли насыщенного раствора нитрита калия, охладить в бане со льдом и добавить в пробирку 1 каплю 2 н раствора серной кислоты.
- отметить, какие изменения происходят в пробирках,
- выделяется газ……………. учитывая, что появление в растворе голубой окраски N2O3, который является ангидридом неустойчивой азотистой кислоты
- Объяснить образование над раствором бурого газа
- Составить уравнение реакции взаимодействия нитрита калия с серной кислотой в молекулярном и ионном виде:
KNO2 + H2SO4
- Составить уравнение реакции разложения азотистой кислоты:
HNO2
- Составить уравнение реакции разложения оксида азота(III):
N2O3
- Сделать вывод о свойствах азотистой кислоты, оксида азота(III)
Опыт 3.Окислительно–восстановительные свойства нитритов
а) Налить в пробирку 2-3 капли раствора иодида калия, подкислить его 1 каплей разбавленной H2SO4 добавить несколько капель раствора NaNO2.
- Отметить происходящие изменения в растворе.
- Составить уравнение реакции нитрита натрия с йодидом калия
NaNO2 + KI + H2SO4
- Указать окислитель………………….., восстановитель ………………….
- Указать, какие свойства проявляет нитрит - ион.
б) К 2-3 каплям раствора KMnO4 , подкисленного 1 каплей разбавленной H2SO4, прилить 2-3 капли NaNO2.
- Отметить происходящие изменения в растворе.
- Составить уравнение реакции нитрита натрия с перианганатом калия, учитывая, что обесцвечивание происходит в результате перехода ионов MnO4- в Mn2+
NaNO2 + KMnO4 + H2SO4
- Указать окислитель………………….., восстановитель ………………….
- указать, какие свойства проявляет нитрит – ион…………………………...
- Вывод об окислительно-восстановительных свойствах нитрит – иона:
Опыт 4. Окислительные свойства азотной кислоты – взаимодействие с металлами (см. также лабораторные работы №9 – 15)
а) Взаимодействие металлов – Mg, Fe, Cu – с разбавленной азотной кислотой (показательный)
В три пробирки налить по 2-3 мл разбавленной азотной кислоты. Осторожно опустить в первую пробирку пластинку меди, во вторую – железа, в третью – магния. Если реакция идет слабо, слегка нагреть пробирки, после охлаждения в пробирку с Fe добавить 1 каплю тиоцианата калия (KSCN)
отметить, какие изменения происходят в каждой из пробирок, с каким металлом реакция идет наиболее энергично;
составить уравнения возможных реакций Mg с разбавленной азотной кислотой, учитывая, что образуется нитрат магния, вода и продукт восстановления азота (V)
Mg + HNO3(разб.) → NO + … + …
Mg + HNO3(разб.) → NH4NO3 + … + …;
составить уравнения реакции Fe с разбавленной азотной кислотой, учитывая, что образуются нитрат железа (III), вода и оксид азота (II):
Fe + HNO3(разб.) → …;
ответить, действием какого реактива можно доказать образование соли железа (III);
составить уравнение реакции меди с разбавленной азотной кислотой, учитывая, что образуются нитрат меди (II), вода и оксид азота (II).
Cu + HNO3(разб.) → NO + … + …
б). Взаимодействие металлов – Al, Fe, Cu – с концентрированной азотной кислотой (показательный)
В три пробирки налить по ~1 мл концентрированной азотной кислоты. Осторожно опустить в первую пробирку пластинку меди, во вторую – железа, в третью – алюминия. Наблюдать за изменениями в пробирках в течение ~2 минут. Пробирки с железом и алюминием нагреть.
Отметить, какие изменения происходят в каждой из пробирок при комнатной температуре; при нагревании;
ответить, с каким металлом при комнатной температуре реакция идет наиболее энергично, какие металлы "пассивируются" концентрированной азотной кислотой;
составить уравнение реакции меди с концентрированной азотной кислотой, протекающей при комнатной температуре с образованием нитрата меди (II), оксида азота (IV) и воды:
Cu + HNO3 → NO2↑ + … + …;
(конц.) бурый
составить уравнение реакции железа с концентрированной азотной кислотой, протекающей при нагревании с образованием соли – нитрата железа (III), оксида азота (IV) и воды:
Fe + HNO3(конц.) → NO2↑ + … + …;
составить уравнение реакции алюминия с концентрированной азотной кислотой, протекающей при нагревании с образованием соли – нитрата алюминия, оксида азота (IV) и воды:
Al + HNO3(конц.) → NO2↑ + … + …
Опыт 5. Получение оксидов фосфора реакцией горения (показательный)
На металлической ложке внести в стакан горящий красный фосфор. Стакан закрыть стеклянной конической воронкой.
- Охарактеризовать внешний вид красного фосфора
- отметить, как протекает реакция
- охарактеризовать внешний вид продуктов реакции
- составить уравнения реакций горения фосфора:
P + O2(недост.) →…
Р + О2(изб.) →…
- Вывод
Опыт 6. Взаимодействие оксидов фосфора с водой. Получение раствора ортофосфорной кислоты
Обмыть стеклянную воронку и стенки стакана (опыт 3) дистиллированной водой. Добавить индикатор – метиловый оранжевый:
- охарактеризовать растворимость оксидов фосфора
- составить уравнения реакции оксидов фосфора с водой:
P2O5 + H2O →…
P2O3 + H2O →…
- объяснить изменение окраски индикатора в растворе и среда в полученном растворе…………..
- составить уравнения электролитической диссоциации ортофосфорной кислоты:
1 стадия: H3PO4
![]() …
…
2 стадия: H2PO4- …
3 стадия: HPO42- …
- составить выражения для констант диссоциации (К1; К2; К3), привести значения констант
К1 = К2 = К3 =
- в каком направлении смещены равновесия диссоциации первой, второй и третьей стадии;
- какая стадия диссоциации осуществляется лучше
- назвать все полученные соединения и ионы, содержащие фосфор
- охарактеризовать кислотно-основные свойства оксидов фосфора и ортофосфорной кислоты.
Опыт 7. Гидролиз солей ортофосфорной кислоты
На предметное стекло поместить три кусочка универсальной индикаторной бумаги и нанести на них по 1 капле растворов солей: ортофосфата натрия, гидрофосфата натрия и дигидрофосфата натрия. Определить pH – растворов солей, сравнив окраску индикаторной бумаги со шкалой.
- Записать уравнения процессов, протекающих в растворах указанных солей в молекулярной и ионной форме
Na3PO4 + H2O →…
Na2HPO4 + H2O →…
NaH2PO4 + H2O →…
- Рассчитать константы гидролиза и сравнить их с константами диссоциации
Кгидр(PO43-) =
Кгидр(НPO42-) = Кдисс(НPO42-) =
Кгидр(Н2PO4-) = Кдисс(Н2PO4-) =
- Объяснить, почему растворы имеют разную кислотность
Опыт 8.Осаждение фосфатов железа (III) и алюминия
В две пробирки внести по 3-4 капли растворов солей: в первую – хлорида железа (III), во вторую – хлорида или сульфата алюминия. Добавить в каждую пробирку по 2-3 капли растворов ацетата натрия и гидрофосфата натрия Na2HPO4 .
- Отметить цвета выпавших осадков.
- Написать уравнения реакций, учитывая, что в присутствии ацетата натрия образуются средние соли: фосфат железа (III) и фосфат алюминия, нерастворимые в уксусной кислоте.
FeCl3 + Na2HPO4 + CH3COONa →…
AlCl3 + Na2HPO4 + CH3COONa →…
- Вывод
