
- •Контрольная работа №1
- •1. Параметры состояния.
- •2. Уравнение состояния идеального газа.
- •3. Смеси идеальных газов.
- •4. Теплоёмкость.
- •5. Первый закон термодинамики.
- •6. Термодинамические процессы идеальных газов.
- •7. Второй закон термодинамики.
- •8. Газовые циклы.
- •9. Теплопередача.
- •10. Тепловая защита зданий. Теплоснабжение и горячее водоснабжение.
- •12. Газоснабжение жилых и промышленных объектов. Принципиальные схемы и оборудование.
4. Теплоёмкость.
4.11. Продукты сгорания топлива поступают в газоход парового котла при температуре газов t1 = 1000оС и покидают газоход при температуре t2 = 700оС. Состав газов по объему: СО2 = 11%; О2 = 6%; Н2О = 8%; N2 = 75%. Определить, какое количество теплоты теряет 1 кг дымовых газов. Зависимость средней теплоемкости от температуры считать линейной.
Решение:
Количество
теплоты
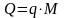 ,
где
,
где
удельное
количество теплоты
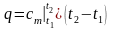 ,
массовая теплоемкость
,
массовая теплоемкость
 (т.к. зависимость средней теплоемкости
от температуры – линейная).
(т.к. зависимость средней теплоемкости
от температуры – линейная).
СО2: С'vm=1.3540+0.00004756*(t1+t2)=1.434852 (кДж/м3○С).
О2: С'vm=0,9337+0,00018183*(t1+t2)=1.241961 (кДж/м3○С).
H2O: С'vm=1.1091+0.00023551*(t1+t2)=1.509467 (кДж/м3○С).
N2: С'vm=0,9123+0.00010492*(t1+t2)=1.090664 (кДж/м3○С).
Теплоёмкость смеси газов в зависимости от способа задания смеси:
С см= r1С1+ r2 С2+…+ rnСn=Σni=1 rgiСi, где
r1, r2 ,… rn –объёмные доли компонентов смеси.
Найдем теплоемкость смеси газов, зная теплоемкость компонента 4%ое содержание компонентов в смеси.
Сm
| =0,11*1,434852+0,06*1,241961+0,08*1,509467+0,75*1,090664=
=0,11*1,434852+0,06*1,241961+0,08*1,509467+0,75*1,090664=
=1,17110674 (кДж/м3○С)=1171.10674 (Дж/м3○С).
q=1171.10674/(-300)= -3.9 (Дж).
Q= -3.9*1= -3.9 (Дж).
Общая задача №2. Газ в количестве 6 м3 при избыточном давлении 9 бар и температуре 175 ○С нагревается при постоянном давлении до 500 ○С. Определить количество подведенной к газу теплоты, считая зависимость средней теплоёмкости газа от температуры нелинейной.
Решить задачу в 2 случаях:
-используя массовую теплоемкость;
-используя объемную теплоемкость.
Решение:
Удельное
количество теплоты
 ,
где теплоемкость
,
где теплоемкость
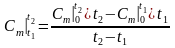 .
.
Сm| =(0.9555*500-0.8836*175)/(500-175)=1.05 (Дж/м3○С).
q= Сm| *(t2 - t1)= 1.05 *(500-175)=341.30 (Дж/м3○С) - удельное количество теплоты.
Количество теплоты: , где М – масса сернистого газа при нормальных условиях (р = 105 Па, Т = 273,15 К).
M=PV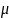 /R0T=105*6*
64.054*103/(8.31469*273.15)=16.922
(кг).
/R0T=105*6*
64.054*103/(8.31469*273.15)=16.922
(кг).
Qm=q*M=341.30*16.922=5775.48 (кДж).
1) Используем объемную теплоемкость:
Сm| =(1.05*500-1,7351*175)/(500-175)=0.6811 (Дж/м3○С).
Удельное количество теплоты:
q= Сm| *(t2 - t1)= 0,6811*(500-175)=221,36 (кДж/м3).
QV=q*V=221.36*6=1328.15 (кДж) - количество подведенной к газу теплоты.
5. Первый закон термодинамики.
Общая задача №1. В железнодорожной цистерне, содержащей 120 т масла с теплоемкостью см = 2,2 кДж/(кг°С) при температуре -7○С, помещен электронагреватель мощностью 2,7 МВт. Определить время разогрева масла до температуры 55○С. Потери теплоты в окружающую среду составляют 4%.
Решение:
Мощность - это работа в единицу времени.
N=A/t.
Работа электронагревателя идет на нагрев масла, т. е. можем запсиать N=A/t.
C=Qn/t*M - из определения теплоемкости.
В данном случае теплота нагревания расходуется на нагревание масла и на теплоту потерь.
Согласно первому закону термодинамики:
Q=Qn+Qпот.
По условию потери теплоты составили 4%, т. е. 0,96Q=Qn.
Из определения теплоемкости Qn=CМ*tM=2200*(55+7)*120*103=
=16368*106 (Дж).
Q=Qn/t; t=Q/N=17050*106/2.7*106=6314.86=1.75 (часа).
5.10. Электрочайник мощностью 2,1 кВт нагревает 1,7л воды от комнатной температуры (20°С) до температуры кипения за 5мин 30с. определить тепловые потери и к.п.д. чайника.
Решение:
Теплоемкость воды:
С=4200 Дж/кг*○С.
Плотность воды 1000 кг/м3.
M=V* ρ=0.0017*1000=1.7 (кг) - масса воды в чайнике.
N=Q/τ→Q=cδtM=4200*80*4.7=571200 (Дж) - количество воды, необходимое на нагревание воды.
Чайник сообщает воде следующее количество теплоты:
N=Qч/τ→Qч=N*τ=2100*330=693000 (Дж).
Qпот=Qчайн-Q=693000 -571200=121800 (Дж).
КПД чайника:
η=Qпот/Qчайн=(121800/693000)*100%=17,6 %.
