
Ханты-мансийский автономный округ – ЮГРА
ДЕПАРТАМЕНТ ПО ОБРАЗОВАНИЮ И НАУКЕ
Сургутский государственный университет
кафедра интегративной медицины
«Утверждаю»
Зав. кафедрой
Д.м.н., проф. Коваленко Л.В.
-------------------------------------
Методические указания по биохимии
для преподавателей по 2 курсу
медицинского факультета
ЗАНЯТИЕ 33
БИОХИМИЯ ПЕЧЕНИ
СУРГУТ 2004
ЗАНЯТИЕ 33
БИОХИМИЯ ПЕЧЕНИ
Время занятия (продолжительность) - 4 учебных часа
Место занятия- учебная комната
Материальное оснащение - набор тематических таблиц, слайдов, диапроектор, лабораторная посуда, набор хим. реактивов, аппарат «Reflotron»
Цель занятия: Студент должен знать:
основные механизмы обезвреживания метаболитов и ксенобиотиков; химический канцерогенез; роль печени в обмене углеводов, липидов и белков.
Мотивация.
Тесная взаимосвязь крови со всеми тканями организма позволяет обнаруживать (путем исследования крови больного) патологические изменения в организме, следить за развитием патологического процесса и судить об эффективности терапевтических мероприятий.
Основные вопросы темы
Причины гипербилирубинемий.
Детоксицирующая функция печени.
Химический канцерогенез.
Роль печени в углеводном обмене.
Роль печени в липидном обмене.
Роль печени в белковом обмене.
Лабораторный практикум
“Определение содержания билирубина в сыворотке крови методом ²сухой химии² на аппарате ²Reflotron²
Распределение времени ( хронокарта)
1 час |
I.. ВВЕДЕНИЕ Проверка присутствия студентов Выяснение причин пропусков Рекомендации к отработке задолженностей Цель и план занятия |
10 мин
|
1-2-3-4 час |
II. КОНТРОЛЬ УСВОЕНИЯ ТЕОРЕТИЧЕСКОГО МАТЕРИАЛА
|
140 мин |
4 час |
III. ЗАКЛЮЧЕНИЕ
|
10 мин |
Основные учебные и практические навыки, необходимые к усвоению (овладению) на данном занятии.
Знание биологических констант - общего билирубина и его фракций в сыворотке крови (пределы физиологических колебаний).
Знакомство с унифицированным методом определения общего билирубина и его фракций в сыворотке крови.
Навыки работы с биохимической лаборатории с целью подготовки к самостоятельному выполнению простейших биохимических анализов
- работа с лабораторной посудой
- работа с хим. реактивами
- работа на аппарате «Reflotron»
Вопросы для самоконтроля (письменные упражнения)
I. В эксперименте через 1-2 часа после экстирпации (полного удаления) печени концентрация каких из перечисленных веществ в крови уменьшится? 1. Глюкоза. 2. Аммиак. 3. Аминокислоты. 4. Мочевина. 5. Прямой билирубин. 6. ЛПОНП. 7. Креатин. 8. Белки свертывания крови. 9. Альбумин.
II. Какие из перечисленных процессов происходят только в печени? 1. Синтез гликогена. 2. Синтез холестерина. 3. Синтез альбумина. 4. Синтез мочевины. 5. Синтез инсулина. 6. Синтез глюкозы. 7. Синтез кетоновых тел. 8. Синтез фосфолипидов.
III. При лечении хронического алкоголизма применяют тетурам, в результате чего происходит накопление в организме ацетальдегида.
А. Напишите схему метаболизма этанола до стадии образования уксусной кислоты.
Б. Какой фермент ингибируется при лечении тетурамом?
IV. Пациент длительное время употреблял алкоголь.
А. Какие системы обезвреживания алкоголя будут при этом активироваться?
Б. Изменится ли и как у данного пациента эффективность наркотических средств при хирургическом вмешательстве?
Теоретический материал причина гипербилирубинемий
Известно, что способность печени образовывать глюкурониды и выделять их в желчь в 3-4 раза превышает их образование в физиологических условиях.
При гемолитической желтухе гипербилирубиемия возникает за счет непрямого билирубина. В результате усиленного гемолиза происходит интенсивное образование непрямого билирубина из разрушающегося гемоглобина. В то же время печень оказывается неспособной к образованию столь большого количества билирубинглюкуронидов, что приводит к накоплению непрямого билирубина в крови и тканях (Рис. Б).
Известно, что непрямой билирубин не проходит через почечный порог, поэтому билирубин в моче при гемолитической желтухе, как правило не определяется.
При паренхиматозной желтухе наступает деструкция печеночной ткани, нарушается экскреция прямого билирубина в желчные капилляры и он попадает непосредственно в кровь, где содержание его значительно увеличивается. Поражение гепатоцитов сопровождается нарушением их способности разрушать до моно- и дипироллов всосавшийся из тонкого кишечника мезобилирубиногена (уробилиногена). Последний попадает в большой круг кровообращения и выделяется почками с мочой.
При обтурационной желтухе нарушено желчевыделение, что приводит к резкому увеличению содержания прямого билирубина в крови. Несколько повышается в крови концентрация и непрямого билирубина. Резко снижается содержание стеркобилиногена в кале. Полная обтурация желчного протока сопровождается отсутствием желчных пигментов в кале (ахолический кал).

Детоксицирующая функция печени
Детоксикация реализуется путем химической модификации веществ, которая включает две фазы. В первой фазе вещество подвергается гидроксилированию. Во второй фазе к гидроксильной группе присоединяется какое-либо вещество - глюкуроновая кислота, серная кислота, глутамин (реакция конъюгации). В результате этой серии реакций ксенобиотики становятся более гидрофильными и выделяются с мочой. Вещества, более гидрофобные или обладающие большой молекулярной массой (300 кД), чаще выводятся с желчью в кишечник и затем удаляются с фекалиями.
I фаза – гидроксилирование. Гидроксилирование заключается в окислительном превращении субстрата, в результате чего в его молекулу внедряется гидроксильная группа, придающая субстрату более лучшую растворимость в воде и делающая его доступным ко второй фазе обезвреживания - конъюгации.
Реакция гидроксилирования катализируется микросомальными ферментами, содержащие в своем составе цитохром Р-450. Он представляет собой комплекс белка с гемом, обеспечивающим присоединение кислорода. Цифровой индекс (450) отражает тот факт, что гем в восстановленной форме, связанной с окисью углерода, отличается максимум поглощения света при 450 нм.
Цитохром Р450 принимает электроны из цепи промежуточных переносчиков и передает их на кислород. Далее кислород соединяется с водородом и образуется вода.

Система микросомальных ферментов индуцибельна. В роли индукторов могут выступать гормоны, лекарственные средства, инсектициды, канцерогены, этанол и др.
Окисление веществ может снижаться конкуренцией за микросомальные ферменты. Все это имеет важное значение при лекарственной терапии. Так одновременное применение конкурирующих препаратов приводит к тому, что обезвреживание одного из них замедляется и он накапливается в организме.
Также надо учитывать, что при выборе дозировки лекарственные вещества могут индуцировать активацию микросомальных ферментов. Это приводит к быстрой инактивации других лекарственных препаратов.
Превращение этанола в ацетальдегид и далее в уксусную кислоту протекает с участием микросомальных оксидаз. При алкоголизме активность Р450 повышена. Поэтому у алкоголиков в трезвом состоянии детоксикация барбитуратов ускорена и они мало эффективны. Напротив большой прием дозы алкоголя тормозит инактивацию фенобарбитала так как этанол конкурирует с ним за энзим. К токсическому действию этанола на ЦНС присоединяется действие фенолбарбитала, что может привести к смерти.
Конъюгационная фаза необходима для образования нетоксических и легко выводимых продуктов метаболизма ксенобиотиков. По механизму реакции конъюгации делятся на два типа.
I тип реакций. Сначала активируются конъюгирующие вещества, а затем они переносятся на ксенобиотики с образованием конъюгата. Этот тип наблюдается во всех тканях и органах организма.
II тип реакций. Сначала активируется ксенобиотик, который затем переносится на конъюгирующую биомолекулу. Это редкий тип конъюгации. Он наблюдается только в печени и почках.
В I типе реакций выделяются глюкуронидная, сульфатная, ацетильная, метильная, а во II типе глициновая и глутаминовая.
Глюкоронидная конъюгация. Донатором глюкуроната служит УДФ-глюкуронат. Глюкуронидной конъюгации подвергаются природные соединения (билирубин, стероидные гормоны, витамины группы D, продукты гниения аминокислот), а также ксенобиотики.
Сульфатная конъюгация. Донатором серной кислоты является – 3-фосфоаденозин-5-фосфосульфат (ФАФС). Сульфатной конъюгации подвергаются природные соединения (стероиды, токоферолы, нафтохиноны, продукты гниения аминокислот), а также ксенобиотики. Пример глюкуронидной и сульфатной конъюгация - обезвреживание скатола (продукта гниения триптофана).

Ацетильная конъюгация. Источником ацетильных групп является ацетил-КоА. Ацетилированию подвергаются природные вещества и ксенобиотики имеющие свободную NH2 – группу.
Метильная конъюгация. Донором метильных групп является активная форма метионина (S-аденозилметионин). Метилированию подвергаются природные вещества и ксенобиотики имеющие свободную NH2 – группу или ОН- и SH-группы.
Все рассмотренные превращения сводятся к повышению гидрофильности обезвреживающего продукта, что облегчает его выведение из организма.
Особое место среди ферментов, участвующих в обезвреживании ксенобиотиков, нормальных метаболитов и лекарств, занимают изоферменты глутатионтрансферазы. Коферментом ее является трипептид глутатион (Глу-Цис- Гли) (Остаток Глу присоединяется к цистеину карбоксильной группой радикала).

Глутатион (G-SH)
Обезвреживание ксенобиотиков с участием глутатионтрансферазы происходит тремя путями:
Конъюгация субстрата (R) с гутатионом:
![]()
Нуклеофильные замещения:
![]()
Например 1–хлор–2,4–динитробензол обезвреживается следующим образом:
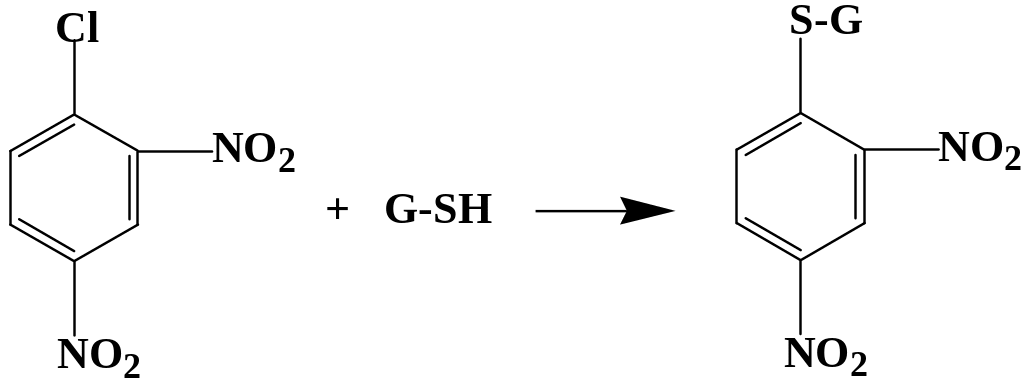
3. Восстановление органических пероксидов до спиртов:
![]()
ХИМИЧЕСКИЙ КАНЦЕРОГЕНЕЗ
Канцерогенез или онкогенез - это развитие рака. Различают следующие причины:
Онкогенные вирусы
Ультрафиолетовые и космические лучи
Врожденные генетические дефекты
Химические, т.н. кацерогенные вещества
Канцерогенные вещества по химической структуре и происхождению разнообразны. Имеются как природные, так и антрогенные соединения. Рассмотрим наиболее известные канцерогены.
Ароматические амины. Они используются в больших количествах в производстве анилиновых красителей, У детей они вызывают рак мочевого пузыря в печени.
Афлактоксины. Они являются метаболитами некоторых плесеней и вызывают рак печени. Плесени продуцирующие афлатоксины заводятся на зерне и других пищевых продуктах при плохом хранении.
Нитрозамины индуцируют злокачественные опухоли в печени, почках, легких, желудке, пищеводе. Источником их в организме могут быть алифатические амины, которые при взаимодействии с нитратами образуют нитрозамины. Алифатические амины и нитраты постоянные компоненты пищи: первые содержатся в рыбе, в ароматических добавках к пище; вторые применяются как консерванты мяса, рыбы и содержатся в растениях,
Индукция развития опухолей требует, как правило, длительных и неоднократных контактов с канцерогенами.
РОЛЬ ПЕЧЕНИ В УГЛЕВОДНОМ ОБМЕНЕ
Печень занимает ключевые позиции в углеводном обмене: ей принадлежит главная роль в поддержании стабильной концентрации глюкозы в крови.
Эта стабильность в значительной мере обеспечивает синтез и расходование гликогена. Гликоген не только важен для поддержания гликемии, он представляет собой также мощный источник энергии.
Считают, что основная роль печени - сводится прежде всего к запасанию метаболитов - предшественников, необходимых для биосинтеза жирных кислот и глицерина и в меньшей степени к окислению их до СО2 и Н2О.
В реакциях пентозофосфатного пути в печени образуется НАДФН2, используемый для восстановительных реакций в процессе синтеза жирных кислот, холестерина и стероидных гормонов. Кроме того, при этом образуются пентозофосфаты необходимые для синтеза нуклеиновых кислот.
Наряду с утилизацией глюкозы в печени, происходит и ее образование. Непосредственным источником глюкозы в печени служит гликоген. Кроме того, глюкоза в печени образуется также в процессе глюконеогенеза и главным образом из гликогеновых аминокислот.
Центральную роль в превращениях углеводов и саморегуляции углеводного обмена в печени играет глюкозо-6-фосфат. Он резко тормозит фосфорилитическое расщепление гликогена, активирует ферментативный перенос глюкозы с уридиндифосфоглюкозы на молекулу синтезирующегося гликогена, является субстратом для дальнейших гликолитических превращений, а также окисления глюкозы, в том числе по пентозному пути. Наконец расщепление глюкозо-6-фосфата фосфатазой обеспечивает поступление в кровь свободной глюкозы, доставляемой током крови во все органы и ткани.
